1型糖尿病(
T1D
)是一种复杂的T细胞介导的自身免疫性疾病,导致产生胰岛素的β细胞破坏和胰岛素分泌不足。在1921年发现胰岛素之前,T1D患者在确诊后一两年内就会死亡;然而,自从胰岛素的发现和大规模生产以来,T1D不再是一种绝症,然而,随着时间的推移,许多患者依然会出现并发症,包括心血管疾病、视网膜病变、神经病变和肾病。
T1D是遗传风险、环境触发因素以及B细胞和T细胞对β细胞及其产物的自身反应发展的综合结果。T1D临床分期可以分为3个阶段:第1阶段表现为血糖正常的两个或多个的胰岛自身抗体,第2阶段表现为血糖异常的两个或更多个的胰岛自身抗体,第3阶段是具有症状性T1D的临床诊断。
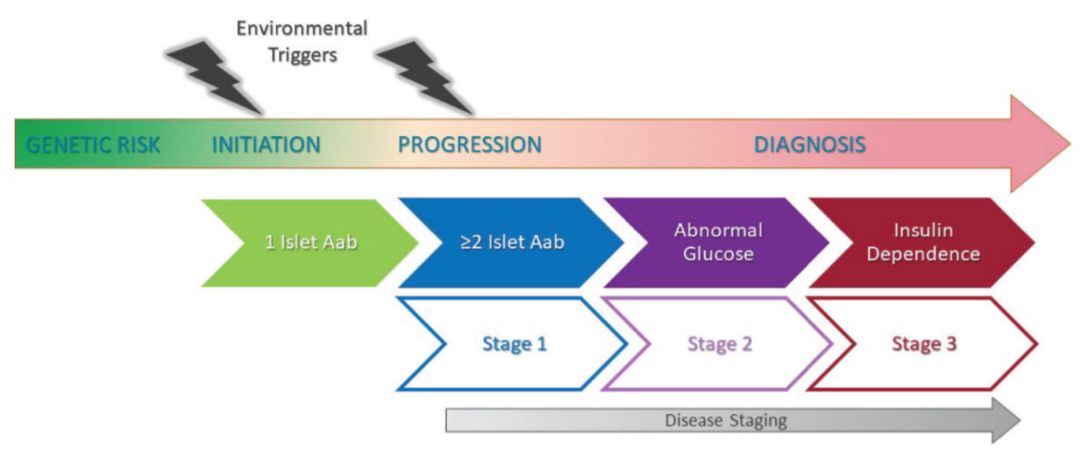
基于T1D大鼠模型的成功实验,早期的免疫调节尝试包括使用钙调神经磷酸酶抑制剂环孢霉素。在确诊后6周内接受治疗的30名患者中,16名恢复到正常的C肽水平,并成为胰岛素独立型,这是一个前所未有的结果。皮质类固醇加每日硫唑嘌呤的使用在新发T1D中也显示出有益的结果,尽管由于有副作用,这些方法没有被采用,但这些试验在证明T1D免疫调节的潜力方面仍然很重要。
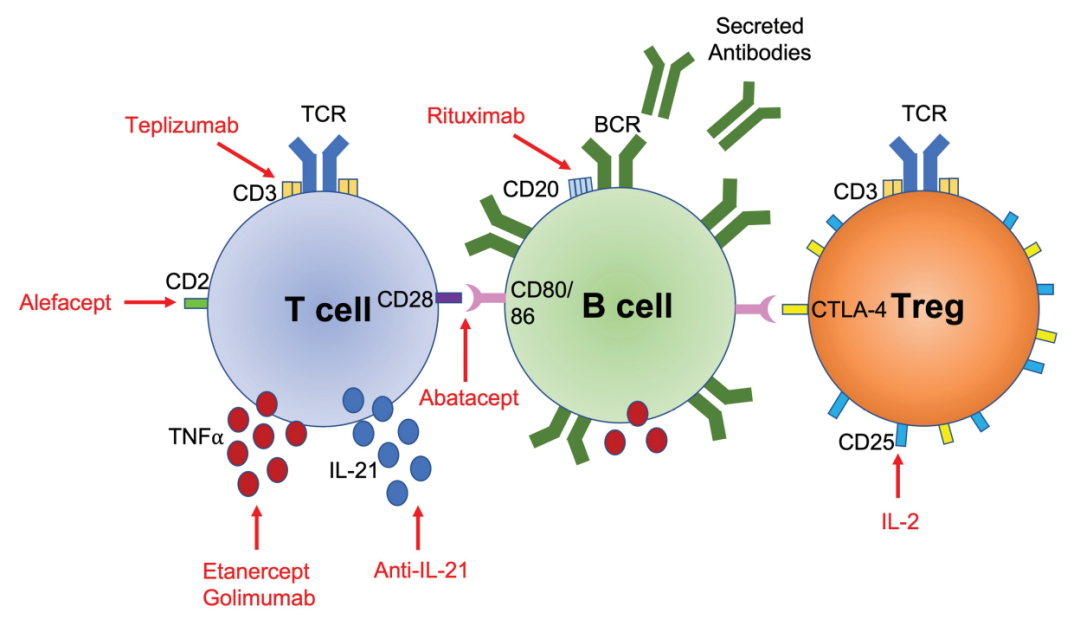
此后,已有多项免疫治疗研究旨在通过针对参与疾病过程的关键免疫细胞以及它们产生的细胞因子来减少β细胞的丢失。一些成功的非抗原特异性免疫疗法,在保护β细胞功能甚至延缓T1D发展方面展现出富有希望的前景。
遗传、年龄和抗体
-
抗原特异性都是
T1D
的危险因素,其中易感因素包括对胰岛抗原的
T
细胞和
B
细胞反应更高、免疫调节受损以及损害免疫调节和稳态的异常先天炎症。
遗传学是T1D发病机制和进展的关键因素
尽管85%的T1D患者没有疾病家族史,但有充分证据表明,遗传因素有助于T1D易感性。遗传学的证据来自家族史研究和全基因组关联研究(
GWAS
)。在有T1D成员的家庭中,兄弟姐妹的平均终生风险为6-7%,而普通人群的风险为0.4%。此外,同卵双胞胎中T1D的风险大于70%。
6号染色体短臂上的HLA区域占T1D基因关联的50%。HLA区域对应于主要组织相容性复合体(
MHC
),并编码向T细胞呈递抗原的细胞表面受体。对于T1D,HLA-II类等位基因、HLA-DR和HLA-DQ与最高风险基因型DR3-DQ2和DR4-DQ8以及保护性基因型DQ*0602的关联性最强。具体而言,T1D患者是HLA-DR3、DQB1*0201(
DR3-DQ2
)或DR4、DQB1*0302(
DR4-DQ8
)的携带者。此外,GWAS还发现了60多个与T1D易感性相关的HLA区域外单核苷酸多态性(
SNP
)。
病原学
随着T1D发病率的上升,高危HLA单倍型的贡献降低,这表明单凭遗传学不足以驱动T1D的发展。肠道病毒感染和早期体重快速增加都是危险因素。肠道微生物组也被认为是一个危险因素;微生物多样性的缺乏和/或微生物组的变化似乎会增加T1D的风险。
免疫病理学
研究表明,与T1D相关的一些免疫特征在疾病发展过程中始终存在,而一些其他免疫特征仅在疾病的特定阶段存在。常规CD4+T细胞对IL-2的反应降低、过渡B细胞的扩增和NK细胞裂解功能的增加是在首次出现单一自身抗体时观察到的固定免疫特征的例子,并在整个疾病进展过程中出现。相反,滤泡T辅助细胞和外周T辅助细胞的频率增加是在固定免疫干扰后随着疾病进展而获得的,而效应T细胞对Treg介导的抑制的抵抗力增加和更多的末端NK分化是获得性免疫特征,发生于向显性临床糖尿病的过渡阶段。
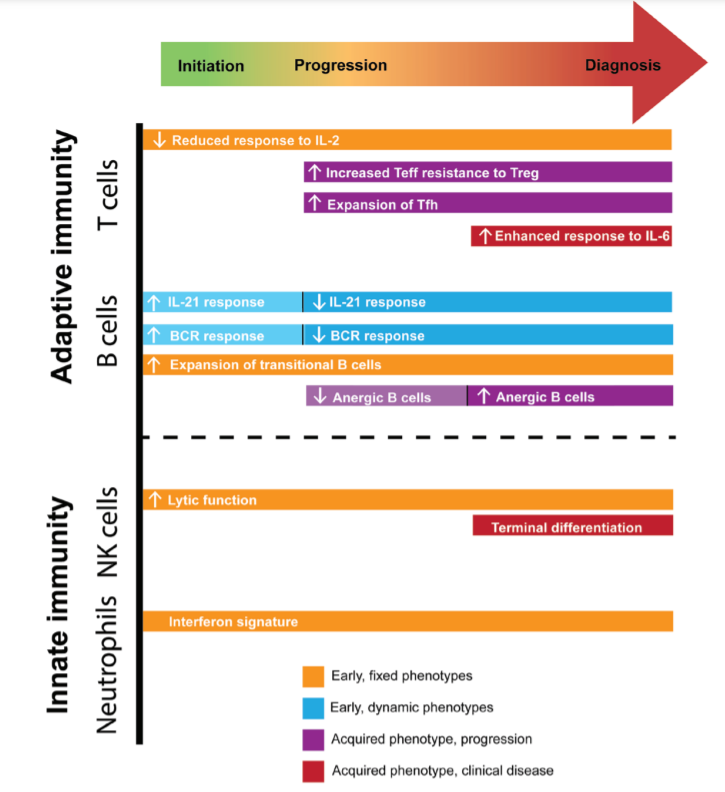
类似地,增强的T细胞对IL-6的反应和无反应的B细胞的扩增也是获得的,但仅在临床疾病发作后获得。有趣的是,B细胞对IL-21或BCR信号的反应变化是动态的,自身抗体阳性的高危受试者的反应增强,但进展到临床诊断和已确定的T1D受试者中的反应减弱。无反应B细胞的频率也是动态的,发病前的频率降低,T1D中的频率增加。因此,某些免疫改变可能出现在疾病开始时或接近疾病开始时,并影响总体疾病风险。
CD4+和CD8+T细胞协调炎症过程,最终破坏胰岛β细胞,导致T1D的发生。
许多与1型糖尿病易感性相关的基因在T细胞中是非常活跃的。
T细胞浸润糖尿病患者的胰岛,在小鼠模型中,通过过继转移T细胞,糖尿病可以从一种动物转移到另一种动物。
因此,针对T细胞的免疫疗法已经得到了广泛的关注。
抗CD3免疫疗法
1979年,Orthoclone(
OKT3
)被开发出来,靶向CD3受体的ε链。1981年,第一批患者服用OKT3,被证明能成功逆转同种异体移植排斥反应。1985年,OKT3开始商业化用于移植,使其成为第一个获批的单克隆抗体。然而,由于副作用,OKT3在临床上的应用受到限制。Teplizumab是一种改良的OKT3抗体,与OKT3具有相同的结合区域,但去掉了ADCC的功能。
临床前研究表明,短期抗CD3治疗能够诱导高达80%的新近诊断的糖尿病非肥胖糖尿病(
NOD
)小鼠病情缓解,这与短暂和部分T细胞耗竭有关。鉴于NOD小鼠抗CD3治疗的临床前研究取得了成功,Teplizumab在24名新诊断的T1D患者中进行了临床研究,在治疗12个月后,三分之二的Teplizumab治疗组的C肽反应相当于或高于研究开始时,而12名对照组参与者中有10人的C肽反应下降。类似地,对80例新发T1D患者进行的另一种人源化抗CD3抗体(
Otelixizumab
)的II期研究也显示,接受抗CD3治疗的患者的β细胞功能恶化较慢。
此外,胰岛自身抗体在糖尿病发生前多年产生的事实为治疗干预提供了机会。人们开始利用这一窗口,向患有血糖异常且存在2种或2种以上胰岛自身抗体但尚未被诊断为T1D的高危人群服用Teplizumab,这项研究成功地延缓了这些个体的T1D发展,与安慰剂组的28%相比,Teplizumab组的57%无糖尿病。一项长期随访研究(
中位数为923天
)发现,与安慰剂组的22%相比,Teplizumab治疗组的50%仍无糖尿病。这些数据改变了T1D免疫治疗的前景,提供了第一个证据,证明在高危人群中使用T细胞导向疗法可以改变未来的疾病进程。
这种干预在延缓T1D发展方面的成功是开创性的,Teplizumab很可能成为第一种获准用于延缓甚至预防T1D发展的免疫疗法。然而由于未积累足够的数据,FDA拒绝了2021年7月对Teplizumab批准的请求。但是,免疫疗法在T1D环境中获得批准的势头正在明显增强,而Teplizumab仍然处于领先地位。
抗胸腺细胞球蛋白(ATG)
ATG是一种多克隆IgG,靶向多种T细胞抗原并介导细胞耗竭。在NOD小鼠中,与抗CD3给药类似,ATG治疗能够逆转新近发病小鼠的糖尿病。对新近发病的T1D患者进行的初步小型研究表明,服用ATG可能有助于保护β细胞功能。
然而,在一项II期随机多中心安慰剂对照试验中,58名受试者在T1D诊断后100天内参与试验,ATG不能保留β细胞功能。这种失败与ATG治疗个体在基线到6个月之间的Treg与T效应记忆细胞比率下降有关。随后对25名T1D患者进行的一项试验使用了较低剂量的ATG,并结合粒细胞集落刺激因子(
GCSF
)治疗,这种方法似乎能保护β细胞,接受安慰剂治疗的受试者在一年内C肽减少39%,而接受ATG/GCSF治疗的受试者在同一时间段内C肽增加4.3%。
因此,低剂量ATG仍然是一个有趣的候选者。值得注意的是,在多个临床试验中比较β细胞保护干预的尝试发现,低剂量ATG和抗CD3免疫疗法是对C肽保护影响最大的治疗方法。
Abatacept





