美国FDA近期暂停了Verve的主导项目Verve-101,在上个月提交IND报告后,暂停了该生物技术公司在美国的努力。去年夏天,Verve启动了Ib期试验,从7月开始在新西兰和英国给三名患者服用药物。
Verve于10月提交了IND,并于上周五收到FDA的通知,首席执行官Sekar Kathiresan在发布中表示。生物技术公司预计将在30天内收到概述该机构问题的正式暂停函,并将“尽快”解除暂停。
VERVE-101是一种单碱基编辑分子,旨在永久关闭杂合性家族性高胆固醇血症患者的PCSK9基因,以降低危险的高胆固醇水平。研究人员于7月给第一名患者注射了剂量,这标志着首次在人体中使用碱基编辑。
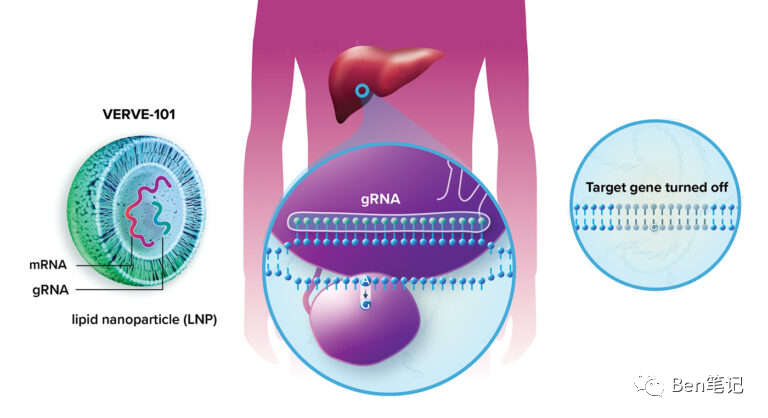
与传统的CRISPR不同,碱基编辑不会在DNA中进行双链切割,而是使用改变目标基因中特定碱基的化学修饰。
根据生物技术公司的说法,到目前为止,三名患者都对这种疗法耐受良好。到目前为止,没有出现与药物相关的副作用,所有副作用都很轻微(1级)。如果一切顺利,Verve打算在明年下半年公布所有剂量递增队列的早期数据。
该公司计划招募40名患者,第二剂队列的招募仍在美国以外地区进行。Verve最初在五月份获得了新西兰监管机构的许可来测试这种疗法。





