用生物材料重塑适应性微环境为解决有助于脊髓损伤(SCI)修复的慢性炎症提供了一条有前途的途径。
水凝胶已被广泛用于增强 SCI 后的组织再生。
此外,锌(Zn)离子可有效调节中枢神经系统的免疫调节。
然而,制备将生物活性 Zn
2+
与生物功能相结合的水凝胶用于创伤性SCI修复仍然存在重大挑战。
利用双膦酸盐修饰的海藻酸盐(Alg-BP)和Zn2+之间的动态金属-配体相互作用
,
南通大学赵亚红/杨宇民教授/WuBingxin团队
报道了一种具有自修复性能和可控Zn
2+
释放的水凝胶(Alg-Zn)。丝素蛋白(SF)上谷胱甘肽(GSH)和甲基丙烯酰(MA)基团之间的巯基点击反应进一步在水凝胶(Alg-Zn/SF)内建立了互穿聚合物网络(IPN)(方案1)。
相关研究成果以
“Zinc-Directed Coordination Network Hydrogels for A20-Mediated Inflammation Modulation and Enhanced Axonal Regeneration in Spinal Cord Injury”
为题于2025年3月7 日发表在《
Advanced Functional Materials
》上。
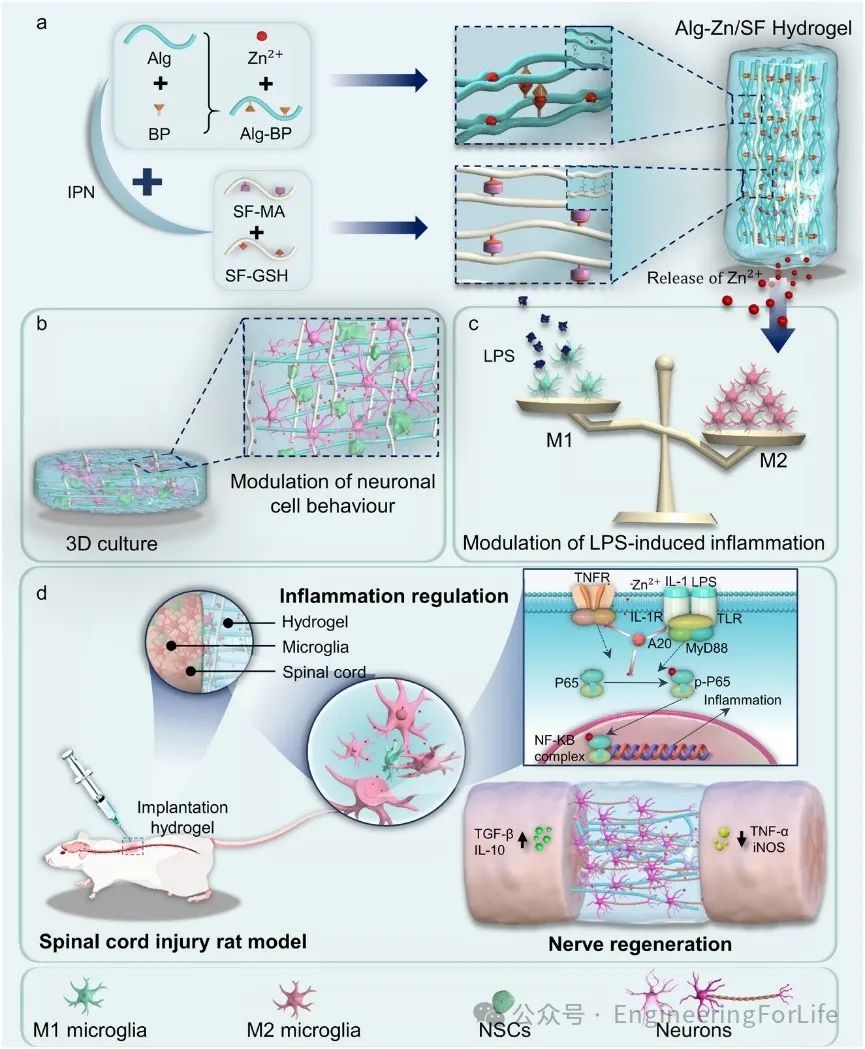
方案1 锌导向配位网络水凝胶的示意图及其在SCI修复中的应用
1. 离子控制释放动态水凝胶的合成设计
首先,通过碳二亚胺化学合成方法合成双膦酸盐修饰的海藻酸钠(Alg-BP);然后,通过建立锌离子浓度梯度来培养原代皮质神经元,发现
轴突长度随锌离子浓度变化,40 μm时达到峰值,且锌离子浓度在0-80 μm范围内对神经元存活有益
(图1a-d)。随后,通过将甘氨酸锌和柠檬酸锌以不同比例混合为交联剂,以及通过调整锌离子的总量来有效
控制凝胶化时间
(图1e)。Zn
2+
的释放速率与水凝胶中的总离子浓度正相关(图1f)。值得注意的是,将SF结合到水凝胶基质中致密了内部网络结构,从而减缓了Zn
2+
的释放(图1g)。
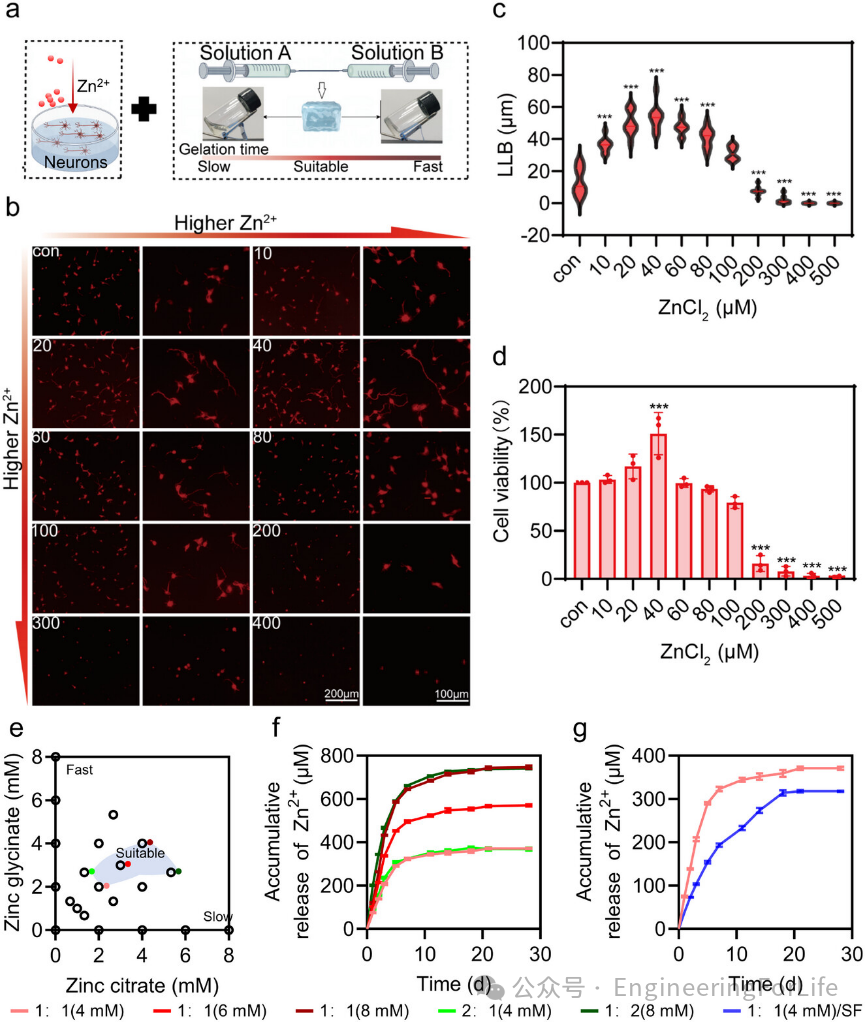
图1 Alg-Zn/SF水凝胶的合成设计
2. 动态水凝胶的表征
通过SEM观察到所有水凝胶均具有多孔结构,其中Alg-Zn/SF和Alg-Ca/SF水凝胶的孔径更小,表明
Zn
2+
与BP的配位作用以及SF中的非共价相互作用共同形成了更致密的网络结构
(图2a)。此外,Alg-Zn、Alg-Zn/SF和Alg-Ca/SF水凝胶片段能够自主融合成整体,且Alg-Zn和Alg-Zn/SF水凝胶在多次应变循环后仍能恢复初始模量,显示出优异的
自愈合性能
(图2c)。流变测试进一步验证了水凝胶的自愈合能力(图2d–g);得益于金属离子和BP之间的可逆动态交联,水凝胶表现出良好的
可注射性
(图2h)。
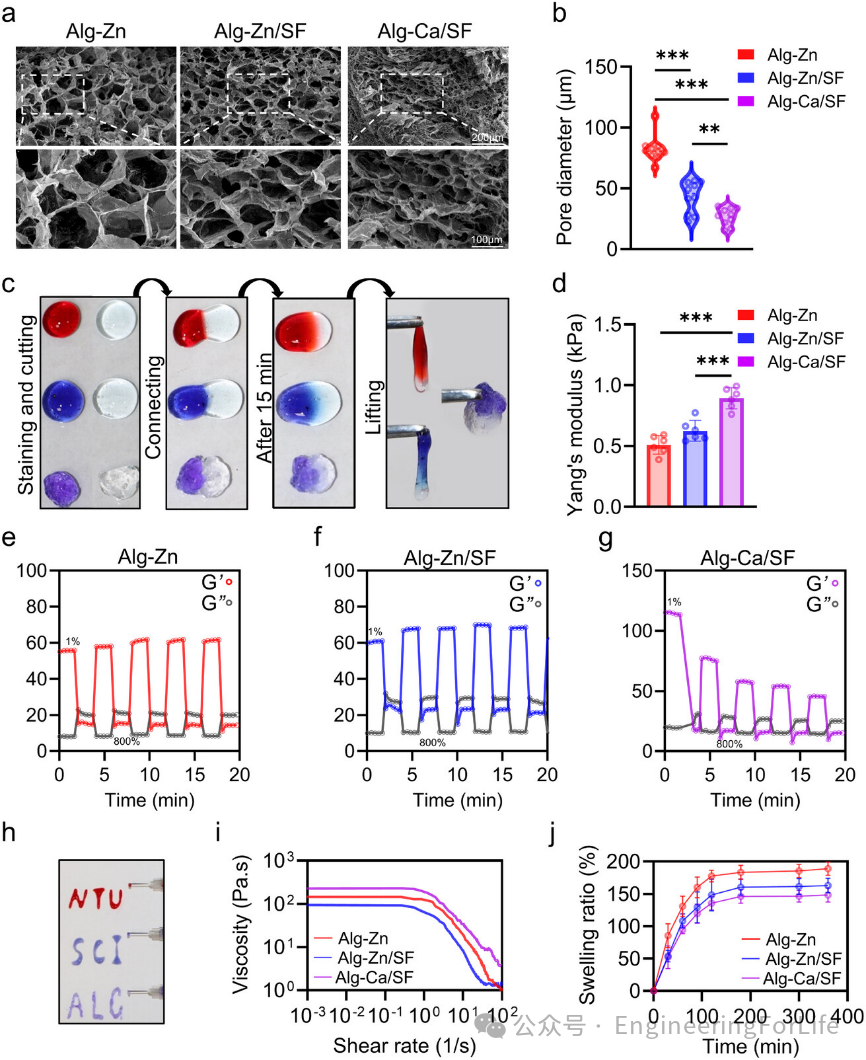
图2 Alg-Zn/SF水凝胶的结构和机械性能
3. 动态Alg-Zn/SF水凝胶促进神经突生长并调节神经干细胞命运
原代皮质神经元被封装在不同水凝胶中进行3D培养(图3a),通过免疫荧光染色发现,与Alg-Ca/SF水凝胶相比,Alg-Zn/SF水凝胶显著
增强了神经元轴突的延伸能力
,表现为更长的神经突起和更多的分支(图3b)。量化分析显示,Alg-Zn/SF水凝胶中的神经元具有更长的最长分支长度(LLB)和更多的总分支数(NTB)(图3c-d)。此外,Alg-Zn和Alg-Zn/SF水凝胶显著
提高了NSCs的增殖活性
,且在培养7天后,Alg-Zn/SF水凝胶组的增殖速度最快(图3f-g)。通过TUBB3免疫荧光染色评估神经元分化情况,结果显示
Alg-Zn/SF水凝胶组的NSCs分化为神经元的比例最高,且神经突起的长度和分支数显著增加
(图3h-j)。
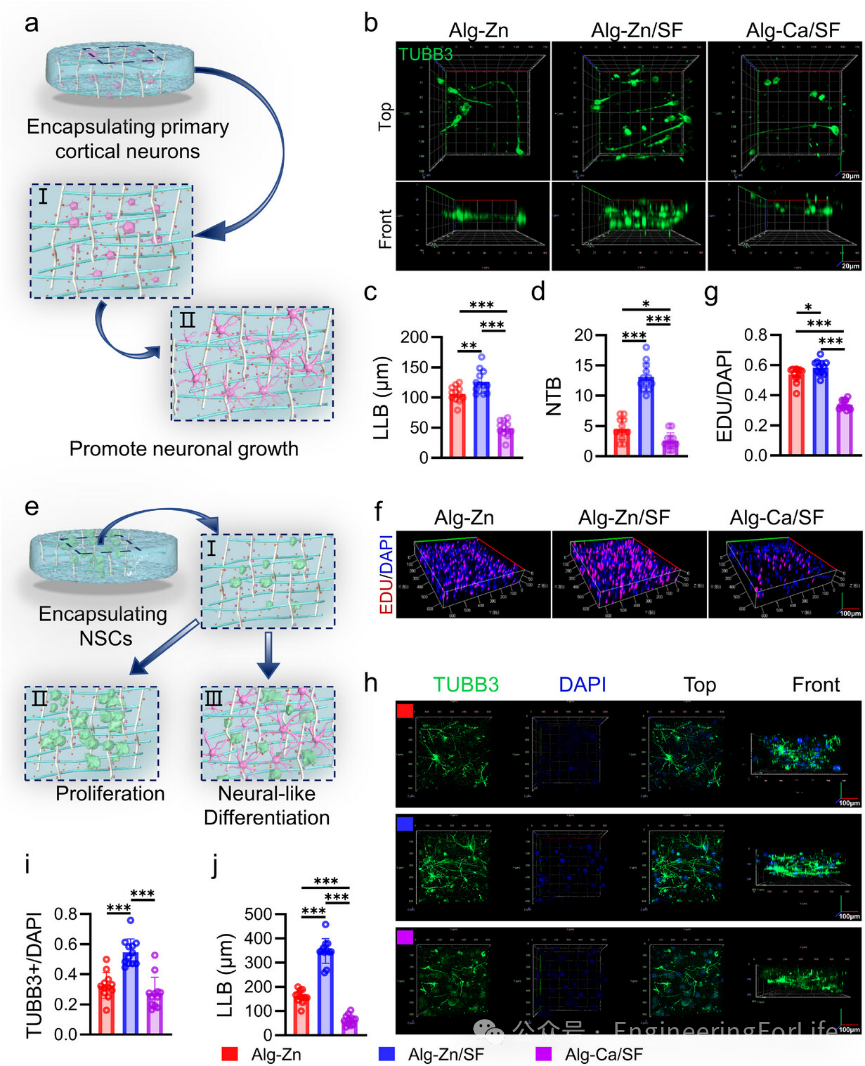
图3 Alg-Zn/SF水凝胶促进NSCs的神经元分化和神经突生长
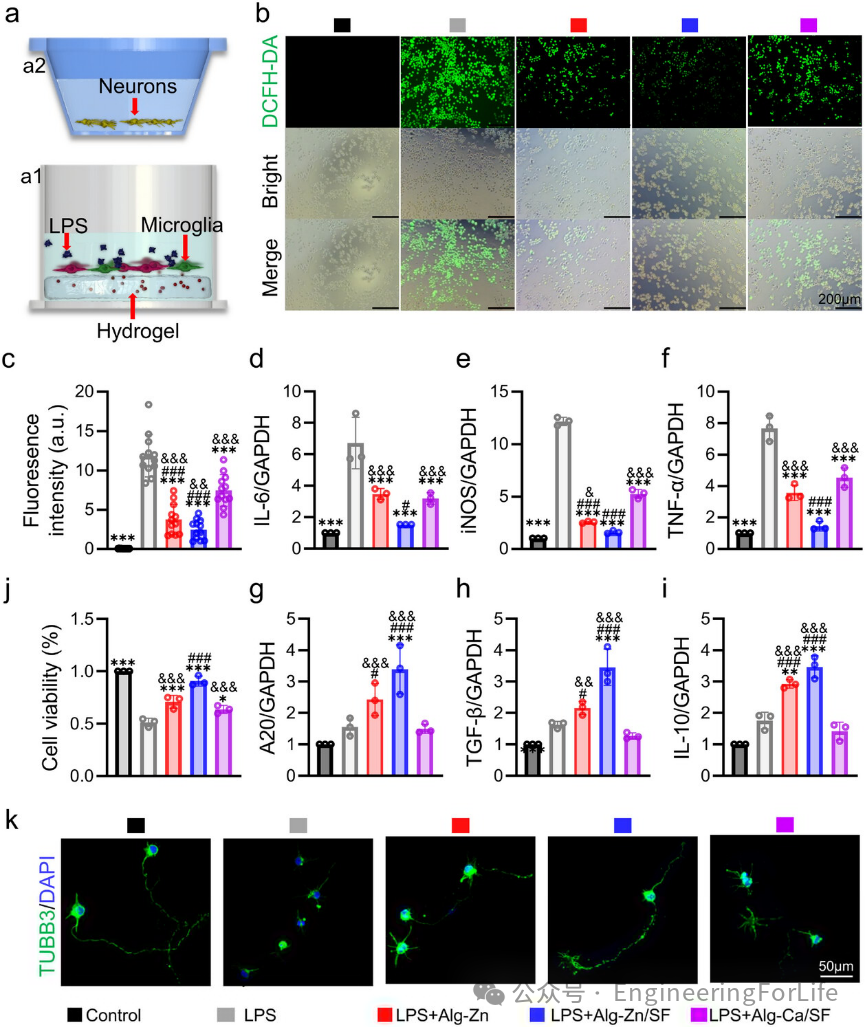
4. 动态Alg-Zn/SF水凝胶抑制炎症反应并拯救对抗神经炎症的神经元存活
然后,研究者将小胶质细胞(BV2)封装在水凝胶中并用脂多糖(LPS)刺激以模拟炎症环境,发现Alg-Zn和Alg-Zn/SF水凝胶能够显著降低细胞内活性氧(ROS)水平,抑制促炎细胞因子的表达,并增加抗炎细胞因子的表达(图4a–i)。此外,通过与LPS激活的BV2细胞共培养原代皮质神经元,发现Alg-Zn/SF水凝胶能够
显著提高神经元的存活率,减轻炎症对神经元生长的抑制作用
(图4j-k)。