
2024年1月上旬,一家致力于开发肿瘤细胞因子疗法的临床阶段的免疫生物学公司Simcha Therapeutics宣布,已与J&J旗下Janssen Biotech达成了一项许可和选择权协议
,Janssen将利用Simcha的新型专有诱饵抗性IL-18(DR-18)为其候选CAR-T细胞疗法“装甲”。该协议由Johnson & Johnson Innovation促成。
Simcha目前唯一公开的候选药
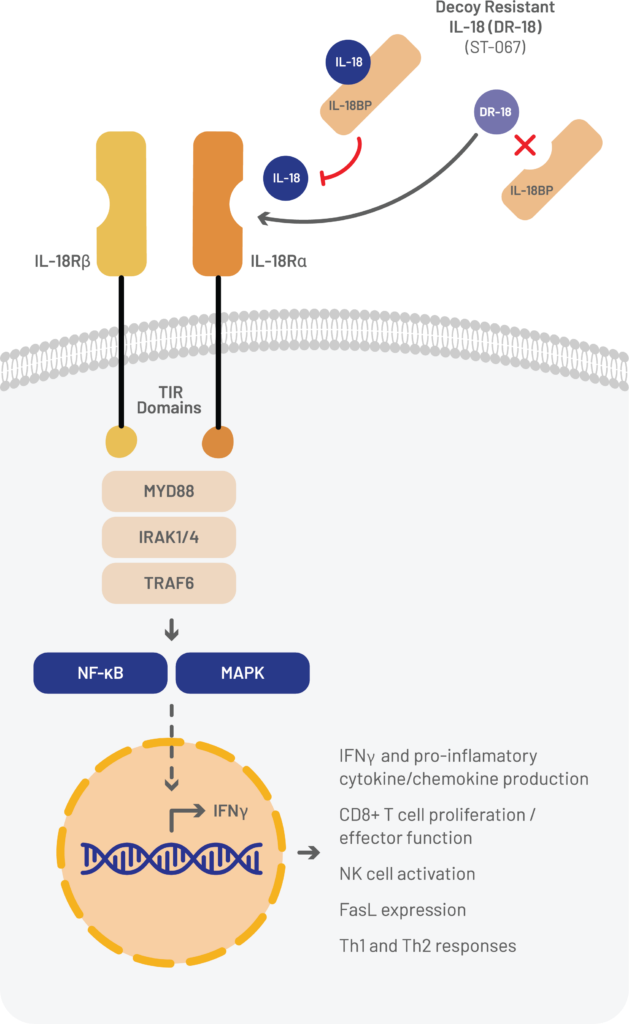
物就是ST-067,是Simcha设计的一种“抗诱饵”的工程化IL-18变体(DR-18)。在临床前研究中,DR-18单独使用以及与抗PD-1等免疫检查点抑制剂联合使用时表现出强大的抗肿瘤活性。
IL-18的功能和挑战
免疫功能:
IL-18作为一种IL-1家族的促炎细胞因子,和IL-12、IL-15一样具有活化记忆样NK细胞的功能。
IL-18调节Th1和Th2细胞的反应,
也作用于非极化T细胞、NK/NKT细胞、B细胞、DC和巨噬细胞,在IL-12存在的条件下产生IFN-γ。
不含IL-12但含有IL-2的IL-18则可诱导CD4 NKT细胞、NK细胞甚至已分化的 Th1细胞产生Th2细胞因子。
IL-18和IL-3还能诱导肥大细胞和嗜碱性粒细胞产生IL-4和IL-13。
Int J Mol Sci.
除了免疫功能,IL-18还参与维持能量稳态和神经稳定性。
例如,IL-18是肝脏和棕色脂肪组织中脂质代谢所必需的。在小鼠中,缺乏IL-18会导致海马细胞线粒体功能障碍,表达出抑郁样症状和认知障碍。
IL-12/IL-15/IL-18三联激动剂是IL-18在候选药物中最常见的出场方式。
IL-18及其受体亚基(IL-18Rα/Rβ)在激活和功能障碍的肿瘤CD8+T细胞中均有
丰富
的表达,表明IL-18激动剂可以有效地刺激抗肿瘤反应。
在第四代CAR-T
设计中,TRUCK CAR也会诱导促进包括IL-18在内的细胞因子分泌,从而增强免疫细胞活化。
IL-18的应用问题
尽管理论上IL-18可以在“热”肿瘤以及“冷”肿瘤中发挥其广泛的免疫刺激活性,但实际药物开发中却发现,采用和其他细胞因子相同策略的重组IL-18疗法对于各类适用免疫疗法的肿瘤基本都无效。
天然IL-18抗癌活性较弱,是由于
肿瘤会产生高水平的IL-18“诱饵受体”
(
decoy receptor)
作为干扰信号
,也就是
IL-18结合蛋白(IL-18BP)
。
IL-18BP是一种分泌性拮抗剂,能以极高的亲和力结合IL-18。在接受rIL-18治疗的患者中,IL-18BP的血清浓度增加了10倍至100倍。IL-18BP也是IFNγ活性的重要生物标志物。
在
肿瘤微环境
中
,IL-18和IL-18BP均高度表达,并且IL-18可以通过分泌IFN-γ进一步增加IL-18BP蛋白的浓度。IL-18Rα则主要表达在肿瘤内的T和NK细胞上,少数髓系细胞也有低表达。
IL-18BP表达的增加还和
激活的CD8+ T细胞
的存在有关,在人和动物模型中观察到CD8+ T细胞比其他 IL-18反应性淋巴细胞更优先活化。
在NSCLC患者血清中,
在抗PD-1或者PD-L1治疗之后,IL-18BP的表达还会进一步增加。
Simcha技术的优势
其设计的DR-18能通过IL-18受体保留完整的信号能力,但不受IL-18BP的抑制,并且可以在肿瘤微环境中保持强大的免疫刺激。
其结构是通过使用酵母表面展示的定向进化来筛选超过2.5亿个mIL-18变体而得的,这些变体在13个受体接触位置被随机分配给那些与IL-18Rα结合但不与IL-18BP结合的变体。
最后其获得了一个特异性结合IL-18Rα的群体。对这个群体的测序揭示了11个独特的序列,从中创建了两个“共识序列”,并对其进行重组表达,用表面等离子体共振法测定了它们与IL-18R、α和IL-18BP的亲和力。所有选定的突变体都保留了IL-18Rα结合,与IL-18BP的结合则可忽略不计(Kd>10μM)。
临床前小鼠模型显示:
DR-18和IL-18相关突变体CS1对IL-18Rα的亲和力相似。
用DR-18治疗结直肠癌和黑色素瘤肿瘤显示出强烈的肿瘤生长抑制作用、小鼠存活率提高,部分小鼠实现肿瘤完全消退。
肿瘤内P14+ CD8+ T细胞的频率、数量和产生IFN-γ的功能显著增加。
此外,XCR1+cDC1细胞的耗尽在治疗期间不影响DR-18的疗效。
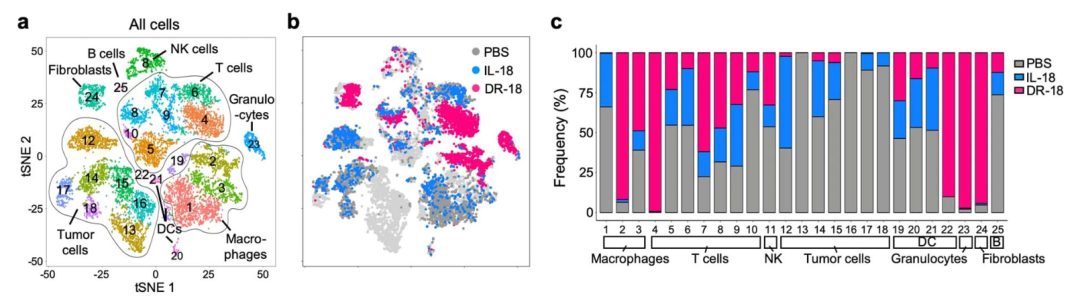
从TME整体情况而言,DR-18诱导了淋巴细胞、巨噬细胞、粒细胞和成纤维细胞簇的显著变化,造成
TME免疫重塑
。此外,DR-18还表现出增加多功能TIL水平、扩增瘤内干细胞样T细胞和NK细胞抗肿瘤功能的效果。
该小鼠模型所使用的DR-18经过人源化后,在人和食蟹猴外周血单核细胞中验证了相同的IFN-γ产生能力。
ST-067目前正在1/2期临床试验中作为单一疗法和与KEYTRUDA®(帕博利珠单抗)联合治疗,用于实体瘤患者和在其他免疫治疗药物上取得进展的患者。

根据Simcha官网的描述,他们在细胞因子研究中的一个主要努力方向是设计具有量身定做的生物学活性的“设计者”细胞因子,以精确地激活抗肿瘤免疫程序,一定程度上可以理解为符合“精准治疗”的行业风向。
小结
IL-18在多种炎症性疾病中均起到重要作用,从机制上说是一个比较有潜力的激动剂靶点。Simcha的技术如果真的能突破IL-18结合蛋白造成的有效性问题同时提高精准杀伤能力,确实能给强生带来新的CAR-T组合策略。
不过,IL-18的多效性作用取决于其细胞因子环境,经过CAR结构竞争性拮抗后究竟还保留多大的免疫作用还未可知。
不敢定论IL-18BP会不会带来强有力的效力,不过可以看出的是大药企的偏好和“广撒网”战略。类似亘喜生物被阿斯利康收购,足够差异化的技术平台是现在这些国际巨头药企收缩投资力度之后的首要目标,尤其是在CAR-T这个越来越“卷”的领域。
相关文章:
构建肿瘤免疫微环境的15个细胞因子
参考文献:
1.https://www.biospace.com/article/releases/simcha-therapeutics-announces-license-and-amp-option-agreement-to-develop-novel-decoy-resistant-il-18-for-use-in-cell-therapy-applications/?s=86
2.Landy, E., Carol, H., Ring, A. et al. Biological and clinical roles of IL-18 in inflammatory diseases. Nat Rev Rheumatol 20, 33–47 (2024). https://doi.org/10.1038/s41584-023-01053-w
3.Yamanishi K, Hata M,et al. Molecular Mechanisms of IL18 in Disease. Int J Mol Sci. 2023 Dec 6;24(24):17170. doi: 10.3390/ijms242417170.
4.Zhou, T., Damsky, W., Weizman, OE. et al. IL-18BP is a secreted immune checkpoint and barrier to IL-18 immunotherapy. Nature 583, 609–614 (2020). https://doi.org/10.1038/s41586-020-2422-6
5.Yasuda K, Nakanishi K, Tsutsui H. Interleukin-18 in Health and Disease. Int J Mol Sci. 2019 Feb 2;20(3):649. doi: 10.3390/ijms20030649.
6.Chmielewski M, Abken H. TRUCKS, the fourth-generation CAR T cells: Current developments and clinical translation. Adv Cell Gene Ther. 2020; 3:e84. https://doi.org/10.1002/acg2.84


本周好文推荐
如需转载请联系佰傲谷并在醒目位置注明出处


















