

作者:Celia
代号:小C
关键词:苏大、妹子、植物百科图鉴
qPCR想必很多人都不陌生。小C之前做了长达一年的相对定量,也还是迷迷糊糊的。但是做实验怎么可以迷迷糊糊的呢?所以小C特此整理了一些相对定量法的要点。今天就和大家分享一下。
RT-PCR就是逆转录或称反转录PCR(reverse transcription PCR),是聚合酶链式反应(PCR)的一种广泛应用的变形,基本概念就是一条RNA链被逆转录成为互补DNA,再以此为模板通过PCR进行DNA扩增。
qRT-PCR(Quantitative Real-time PCR)是实时定量PCR,指的是PCR过程中每个循环都有数据的实时记录,由此可以对起始模板数量或最终复制数量进行精确分析。
Real-time PCR 比qRT-PCR稍微宽泛一点的概念。Bio-Rad公司主页对Real-time PCR和qPCR的定义是这样的:
也就是说Real-time PCR的结果可以是定性的(qualitative),也可以是定量的(quantitative)。定量的就是我们常说的实时定量PCR。
那么qRT-PCR是如何实现定量的呢?在PCR的反应中,引入一种荧光化学物质。随着PCR反应的进行,PCR反应产物不断积累,荧光信号也会等比例增加。每经过一个循环,收集到一个荧光强度信号,这样我们就可以通过荧光强度的变化检测产物量的变化,从而我们可以得到一条荧光扩增曲线图(如下图)。
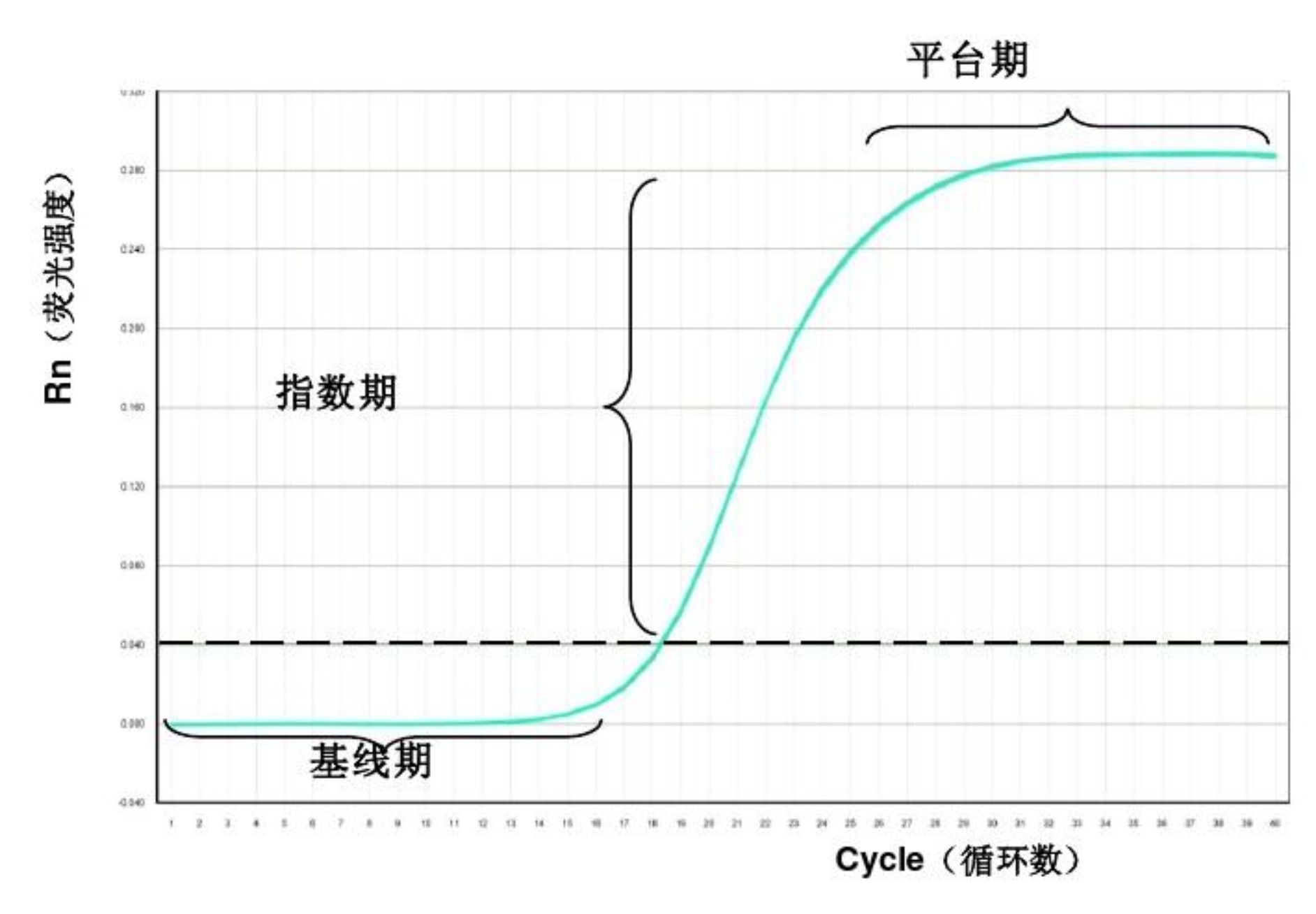
分析Real-time PCR数据的方法可以分为绝对定量和相对定量。
绝对定量(Absolute Quantification,AQ)是为了计算在未知样本中,某个核酸序列的实际拷贝数量,这样计算需要先制作标准曲线,找到荧光强度和产物数量的线性关系。
相对定量(Relative Quantification,RQ)是测定在测试样本中目标核酸片段与校对样本中同一序列片段的相对比例,而不需要知道它们在每个样本中的拷贝数。
相对定量不是像绝对定量那样精确的定量方法,而是计算样本基因含量对参考/标准样本的改变倍率,精确的拷贝数量是不需要计算出来的。因此qPCR相对定量分析法特别适合表述细胞内基因表达量的变化情况,也是十分常见的qPCR数据分析法。
下面小C来介绍三种定量分析的具体操作方法:
ΔCt Algorithms
这个算法是Ct差值基本法。那么首先我们要知道什么是Ct,Ct就是Threshold Cycle,即在每个反应中划定的荧光强度所对应的PCR周期循环数。如下图:
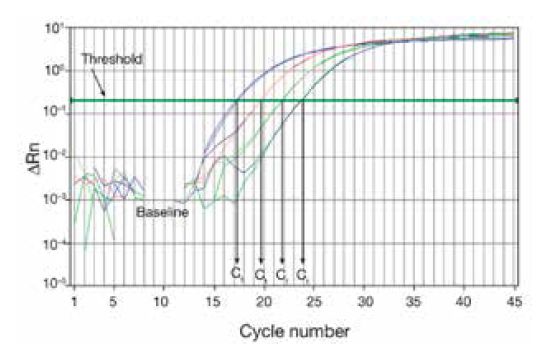
这个划定的荧光强度就是我们的阀值(a.k.a.,threshold),即图中那条横向的绿线,下面对应的四个C值就是每个样本对应的Ct值。
如何确定阀值呢?根据Thermo-Fisher的定义:
选取的阀值需要显著高于荧光扩增曲线图的基线,软件通常将阀值设定为基线标准差的10倍位置处。显然,Ct值取决于阈值,阈值取决于基线,基线取决于实验的质量,Ct值是一个完全客观的参数。Ct值越小,模板DNA的起始拷贝数越多;Ct值越大,模板DNA的起始拷贝数越少。正常的CT值范围在18-30之间,过大和过小都将影响实验数据的精度。
现在都清楚这些基本概念了,那么怎么算呢?你的实验样本即处理组(Gene of Interest,代号GOI)有个Ct值,对照样本即非处理组/自然组(Calibrator,代号CAL)有个Ct值。
ΔCt=Ct
(GOI)
-Ct
(CAL)
;
PCR的产物量以指数函数增长,实验样本的产量为2^Ct(GOI),对照样本的产量为2^Ct(CAL)。
那么GOI对CAL的改变倍率就是2^
ΔCt
那么公式表述如下

这个方法十分基础简单,但这种计算方法是不能准确表述改变倍率的,而且误差很大,只能描述趋势,算是让我们初步理解
Ct差值法的基本原理。
-ΔΔCt Algorithms
小C愿意叫这个为Ct差值比较法,也是现在最流行的算法之一。在这个方法里面我们要引进一个内参基因(Normaliser,代号NOR),一般使用看家基因作为内参(house-keeping gene),因为看家基因在所有细胞中均表达,其产物是维持细胞生存所必须,且在细胞中的表达量或基因组的拷贝数恒定,受环境影响小。那么进行real-time PCR后,内参的CT值也被记录下来,被称为Ct
(NOR)
.
那么
ΔCt
(GOI)
=Ct
(GOI)
-Ct
(NOR●sample)
而且
ΔCt
(CAL)
=Ct
(CAL)
-Ct
(NOR●control)
所以
ΔΔCt=
ΔCt
(GOI)
-
ΔCt
(CAL)
对
ΔΔCt做个负运算变成-
ΔΔCt
那么样本组基因量就是对照组基因量的2^-
ΔΔCt
写成公式就是

但这个方法有一大缺点,我们必须默认目标基因和看家基因在PCR扩增的过程中的反应效率是一致的。而且我们可以看到这个方法也是进行幂运算,幂运算通常会扩大误差,而采取相对定量的算法本身就会产生扩大的情况,所以Ct差值基本法也只能说是看看趋势,并不能说绝对准确。
那么用这个方法产生的数据能否被相信呢?我们可以验证一下
ΔCt
(GOI)
随起始RNA/DNA浓度的增加而发生什么样的变化。理想情况下,不论起始浓度是多少,这个
ΔCt
(GOI)
应该是一致的,这样才能表明
目标基因和看家基因在PCR扩增的过程中的反应效率是一致的,这样的数据才是可信的。
还有一种不采用幂运算,而是log运算的Ct差值法,这里就不多做陈述了,有兴趣的童鞋可以去了解一下。
Standard Curve Method
双标准曲线法是小C最常用的方法。由于目的基因与内参基因一般来说扩增效率是不同的,首先需要对内参和目的基因分别制备描述起始反应浓度和Ct值关系的标准曲线,如图所示(图片和方法介绍来自ThermoFisher官网[3]):
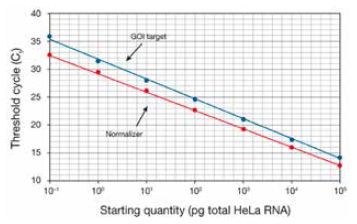
红色标准曲线是内参基因的起始RNA和CT值之间的关系,蓝色标准曲线为目标基因的起始RNA和CT值之间的关系。两条曲线会得出两条斜率,我们分别称为slope-NOR 和slope-
GOI。
最终的计算公式是:
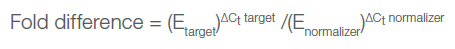
其中
ΔCt
(target)
=
Ct
(GOI●Control)
-Ct
(GOI●sample)
ΔCt
(normalizer)
=
Ct
(NOR●Control)
-Ct
(NOR●sample)
E
(target)
=10^[-1/
slope-GOI]
E
(normalizer)
=
10^[-1/slope-NOR]
关于qPCR数据分析的方法还有很多细节上的处理,比如Ct值取定范围,每个样本的重复次数,标准品的稀释梯度,以及溶解曲线分析等等等等。除此以外还有其他的相对定量法,或者你有什么计算的小窍门,以后有时间我们再聊吧~
[1] Schmittgen T D, Livak K J. Analyzing real-time PCR data by the comparative C(T) method.[J]. Nature Protocols, 2008, 3(6):1101.
[2] Larionov A, Krause A, Miller W. A standard curve based method for relative real time PCR data processing[J]. Bmc Bioinformatics, 2005, 6(1):1-16.
[3] https://www.thermofisher.com/uk/en/home/life-science/pcr/real-time-pcr/qpcr-education/real-time-pcr-handbook.html?cid=rtpcrhandbook-rtpcr

BioEngX
BioEngX---
活跃在移动端的无国界学术圈
持续推送生化工程领域科普文章
、
科研动态
,分享
实验技术及实验经验。点击原文,加入我们!
官方网站:
http://www.bioengx.com/





