
自2016年开始,食药监总局便拉开了优先审评审批的序幕。如今,优先审批审评已有一年之余,头几批的优先审评的药物早已获得批件。2017年马上就要过完一半了,优先审评公示名单也已经公布了十六批。我们从第十三批,也就是2017年获得优先审评资格的仿制药品进行分析,看一看这些获得优先资格药品,一旦上市,对未来市场的影响到底有多大。
二甲双胍可谓是治疗糖尿病领域的老司机了,此次石药集团欧意药业也能获得优先审评资格,确实让业内人士大开眼界,食药监总局给出的理由是“同一生产线生产,已在美国上市,申请国内上市的仿制药”。
不过,石药的二甲双胍早在2013年便在美国上市,现在已然2017年,才进入优先审评名单,也就是说,美国患者都使用上的药品,我国患者还尚未能使用到,这时间跨度,有点儿令人不解。或许,石药集团正是看到了国内药品审评改革前的无奈,转战国际市场,反而在当下迎来了更强的竞争力。
继续深挖,早在2002年,石药的二甲双胍原料药已经在国内上市,国内市场竞争非常激烈。在艾美达全国样本公立医院数据库中显示,在2016年,二甲双胍销售额为近5亿元人民币,其中便有43家企业生产二甲双胍,除原研厂家施贵宝占据了95%以上的份额外,其他企业的市场份额相当分散。
在这样的大环境下,想要分得一本羹,实在是吃力不讨好的活儿。如此一来,转战国际市场能够转移竞争力,这在2013年或许是一个非常有挑战的决定。据了解,在2016年,石药集团的二甲双胍在美国获得了500万美元左右的销售额。
若不是2016年仿制药一致性评价,之后的故事也就平淡无奇了。
去年5月26日,总局发布关于落实《国务院办公厅关于开展仿制药质量和疗效一致性评价的意见》有关事项的公告,原文是这么说的:
“在中国境内用同一条生产线生产上市并在欧盟、美国或日本获准上市的药品,由受理和举报中心负责申报资料受理;一致性评价办公室通知食品药品监管总局药品审评中心对原境内、外上市申报资料进行审核,通知食品药品监管总局食品药品审核查验中心对生产现场进行检查。经一致性评价办公室审核批准视同通过一致性评价。”并且,“同品种药品通过一致性评价的生产企业达到3家以上的,在药品集中采购等方面不再选用未通过一致性评价的品种。”

对于石药的二甲双胍来说,这哪是赢在起跑线上,直接都快到终点了好不好!?在大部分企业还在为仿制药一致性评价焦头烂额的时候,石药已通过海外品种杀回国内,相当于通过了一致性评价,在未来招标过程中,将直接受到政策的青睐。
3个名额中还有两个空缺,四十余家企业争夺这两个空缺。但是,在CFDA公布的4批官方参比制剂名单中,尚未有二甲双胍的原研信息,企业也只能是热锅上的蚂蚁干着急。石药的二甲双胍上市后,将对分散的仿制药企业造成巨大冲击,在近5亿元的市场,有资格追逐的将所剩无几。
又是一个石药集团欧意药业的仿制药品种,纳入优先审评的理由为:临床急需、市场短缺、首仿。不过,在去年,恒瑞的紫杉醇(白蛋白结合型)的上市申请纳入优先审评,并且制证完毕已发批件。此次又有石药集团欧意药业的紫杉醇(白蛋白结合型)上市申请纳入优先审评名单,可见真的是临床急需、市场短缺。
在艾美达全国样本公立医院数据库中显示,紫杉醇共有7亿元左右的销售额,紫杉醇(白蛋白结合型)仅有一家有销售体现,为美国新基生物(原研),销售额高达2亿多元。小伙伴们注意,这仅是全国抽样数据哦!
紫杉烷类药物是被批准用于临床治疗肿瘤的重要新型药物,主要用于转移性乳腺癌、卵巢癌和非小细胞肺癌的治疗。然而,目前市售的溶剂型紫杉醇尽管采用适当的术前用药,仍然具有与溶剂相关的严重副作用和过敏反应。
白蛋白结合型紫杉醇是一种新型的无溶剂紫杉醇,它不需要合成的溶剂作为载体,不需要皮质类固醇或抗组胺药物等预处理,静脉滴注时间短(30min)。其利用了白蛋白的自然生物特性,通过gp-60(糖基化囊膜蛋白)介导的内皮细胞跨膜转运和一种与白蛋白结合的蛋白SPARC(一种酸性的富含半胱氨酸的分泌蛋白)的相互作用而增加肿瘤组织对紫杉醇的摄取和蓄积。临床前模型研究证实白蛋白结合型紫杉醇与溶剂型紫杉醇相比,抗肿瘤活性明显增强。
也就是说,白蛋白结合型紫杉醇是紫杉醇的升级版!
目前,新基紫杉醇(白蛋白结合型)的全国中标价中位数约为5820元/100mg,而紫杉醇注射液(质量层次:科技部颁发的“国家重点新产品”证书的药品)全国中标价约为360元,10ml:60mg。市场中尚未有紫杉醇(白蛋白结合型)的仿制药上市,造成仅有原研厂家新基生物在市场中有销售,患者用药负担非常大。
现如今,恒瑞已经获得上市批准,石药的也已经在路上,原研厂家躺着挣钱的日子已经不多了。
纳入优先审批的理由为:同一生产线生产,已在美国上市,申请国内上市的仿制药,为江苏恒瑞提交申请。本品用于手术和其他操作以及重症监护治疗。作为全麻的辅助用药或在重症监护房(ICU)起镇静作用,它可以松弛骨骼肌,使气管插管和机械通气易于进行。
在艾美达全国样本公立医院数据库中,当下市场中共有四家制药公司有销售数据,分别是江苏恒瑞、上海医药、浙江仙琚和葛兰素史克,其中葛兰素史克为原研厂家,市场份额如下表所示:
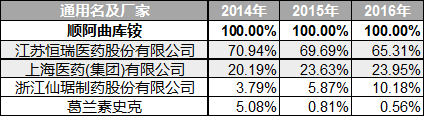
可以看出,目前市场中江苏恒瑞的顺阿曲库铵已经占据了65%以上的市场份额,而原研厂家葛兰素史克份额已经掉到1%以下。当原研退出市场后,剩下的便是国产仿制药的竞争了。
在仿制药申请方面,除江苏恒瑞的苯磺顺阿曲库铵注射液外,共有16个仿制药申请上市文号,涉及10家制药企业,并且均在审评阶段。
此次江苏恒瑞的顺阿曲库铵获得优先审批资格,并且是以“同一生产线生产,已在美国上市”为由,与石药集团的二甲双胍有异曲同工之处,留给其他仿制药的企业时间不多了。
为华海药业申报仿制药上市申请,原研厂家默沙东,为治疗艾滋病用药,纳入优先审评的理由为:临床急需、市场短缺。
早在2013年,华海药业与默沙东签订《合同加工主协议》,华海药业为默沙东生产包括国内市场在内的全球市场依非韦伦片,默沙东负责销售,相当于华海为默沙东作药品代工,利润方面与原研药相比有较大差距。
在此前,华海药业申报依非韦伦均以进口新药为名义,此次纳入优先审评的依非韦伦,则是以仿制药上市为名义,一旦上市成功,仿制药对原研药的冲击将是巨大的。目前来看,华海作为药品代工厂家,对于利润的获取无法与原研相比,但是若为自己生产的仿制药,则是另一番光景了。
在艾美达全样本公立医院数据库中显示,2014年依非韦伦销售额仅为两万四千元左右,到2016年增长到七十三万元左右,近些年复合增长率高达450%!
据小编了解,依非韦伦作为艾滋病用药,存在其特殊性,该药物可在特定人群中作为免费用药。
在2016年年底,已有上海迪赛诺生物医药有限公司获得依非韦伦片的仿制药批准文号。对于华海药业来说,虽然原研药在自家生产,但市场中仍有不少仿制药企业虎视眈眈,市场竞争仍然激烈。
入榜理由为:罕见病用药,适应症为用于各种原因引起的上运动神经元损伤所遗留的痉挛性肌张力增高状态,如脑卒中、脑外伤、脊髓损伤、脑性瘫痪、多发性脑血管硬化等,为珠海保税区丽珠合成制药有限公司申报。
在食药监总局中,仅能查到湖南迪诺制药有限公司生产的丹曲林钠胶囊。比较奇怪的是,小编不仅在艾美达全国样本公立医院数据库中没有找到丹曲林钠的销售数据,在主流药品数据查询库中也未查到该药物的销售数据及中标信息。此次竟然被纳入到优先审批中,实在是有些令人费解,了解详情的小伙伴们,能否不吝赐教?非常感谢!
入榜理由:首仿,由齐鲁制药提交申报,原研厂家为辉瑞。适应症为:降低开角型青光眼和高眼压症病人升高的眼压。目前,仍在审评审批中。
在艾美达全国样本公立医院数据库中,2016年拉坦噻吗滴眼液销售数据为近六百万元,复合增长率为27%,全国中标价中位数约为两百元左右。目前看来,尚未有国内其他企业申报拉坦噻吗滴眼液仿制药。
最后,小编想说的是,优先审批开创了审批效率的先河,使得优秀、短缺的药品能够快速完成审批流程,进入临床或上市,大大节省了审批等待时间,这绝对是利好政策。并且,能够进入优先审批名单的申请大部分也都是高质量的仿制药,一旦上市,对本领域的冲击将是巨大的。
本文转自:艾美达行业研究







