9月4日,国家食品药品监督管理局药品评审中心(CDE)在官网上发布公告,包括我国原创小分子靶向药物呋喹替尼在内的多个药品进入优先审批程序。
原文如下:
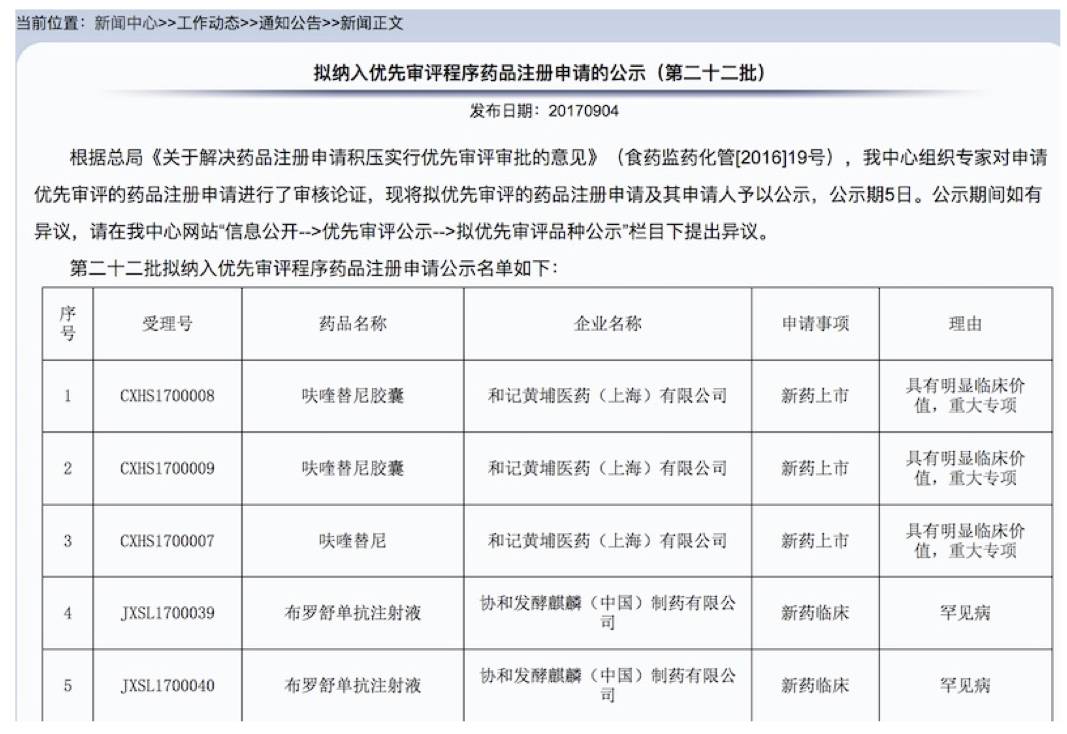
根据总局《关于解决药品注册申请积压实行优先审评审批的意见》(食药监药化管[2016]19号),我中心组织专家对申请优先审评的药品注册申请进行了审核论证,现将拟优先审评的药品注册申请及其申请人予以公示,公示期5日。公示期间如有异议,请在我中心网站“信息公开-->优先审评公示-->拟优先审评品种公示”栏目下提出异议。
第二十二批拟纳入优先审评程序药品注册申请公示名单如下:
关于呋喹替尼:
呋喹替尼是一种新型高选择性抑制血管内皮生长因子受体的小分子化合物,由和记黄埔发现,2013年10月礼来与和记黄埔达成战略合作协议,礼来与和记黄埔共同开发,礼来负责中国的市场销售。
呋喹替尼组(5mg,1次/天,服药3周停药1周)较安慰剂组可改善转移性结直肠癌患者无进展生存期(PFS)3.7个月(4.73和0.99个月,HR=0.30,双侧P<0.001,95%可信区间(CI)0.15-0.59,这意味着疾病进展的风险降低了70%)。呋喹替尼组的疾病控制率(DCR)明显高于安慰剂组(68.1%和20.8%,双侧P<0.001)。
呋喹替尼组初步的中位生存期(OS)为7.56个月,安慰剂组为5.52个月(HR=0.62,95%可信区间(CI)0.30-1.29),OS结果尚在进一步随访中。
呋喹替尼安全性与其他小分子抗VEGFR药物相似。常见不良事件为手足综合征、高血压、声音嘶哑、蛋白尿和AST升高。这些不良事件均可耐受和管理。
在另一项呋喹替尼作为3线及以上治疗转移性结直肠癌的开放式Ib期临床研究中,服用呋喹替尼5mg,1次/天,服药3周停药1周,其中位PFS为5.3个月,中位OS达8.8个月,客观缓解率(ORR)为9.5%,疾病控制率(DCR)为76.2%。
相关阅读:
【ASCO 2017】秦叔逵教授谈中国人自己的原研药
呋喹替尼开创转移性结直肠癌三线治疗新局面 ——李进教授访谈
中美专家热议FRESCO研究—呋喹替尼强力推进转移性结直肠癌三线治疗
28个肿瘤相关临床试验招募患者
点击下方图片即可查看详情





