今天是2017年7月26日
农历六月初四
医麦客:
检查点抑制剂还有待进一步研究
2017年7月26日/医麦客 eMedClub/--
昨日,Merck宣布其PD-1抗体Keytruda二线治疗头颈癌的一项三期临床试验(Keynote-040)未能达到试验终点。该试验招募了近500名对一种或多种含铂系统治疗没有充分反应的HNSCC(头颈鳞状细胞癌)患者,
尽管相比较化疗或Erbitux治疗来说,Keytruda降低了18%死亡率,但未能明显改善总生存期(OS)。

Keytruda(图片来源pharmaceutical-technology.com)
2016年8月5日,Merck就宣布美国FDA加速批准Keytruda(pembrolizumab)用于含铂类药物化疗后疾病进展复发或转移性头颈部鳞细胞癌(HNSCC)。
自此Keytruda顺利拿下了第3个适应症—头颈癌。
当时FDA对Keytruda治疗头颈癌的加速批准是基于Keynote-012研究中应答率和应答持续时间的替代终点数据,
研究结果显示,ORR为16%,其中完全缓解率为5%。
但根据FDA规定这样加速审批的药物需要在三期临床试验中证明生存优势,而此次失败的Keynote-040研究,则可能担任正式批准的验证性试验。
这似乎表明Keytruda治疗头颈癌失败已成定局。但公司可不那么认为,Leerink的Seamus Fernandez表示,
Keynote-048一线治疗头颈癌患者的研究结果如果是积极的,则可以作为确认性试验。
目前,默克公司表示, Keytruda治疗头颈癌的标签“保持不变”。除此之外,Keytrdua一线治疗头颈癌的一项三期临床也即将结束。

随着越来越多的公司涉足PD-1/PD-L1 领域,检查点抑制剂的空间可能会变得越来越拥挤,但是它的顶尖战斗一直处在Merck & Co和BMS之间。
而此次Merck的Keytruda治疗头颈癌失败,与之形成鲜明对比的则是BMS的Opdivo,
2016年11月20日,BMS公司宣布FDA批准Opdivo用于治疗晚期复发的头颈鳞癌患者,从而成为了首个唯一一个经III期临床研究证明与含铂化疗相比能够显著延长复发或转移性头颈部鳞状癌患者总生存期(OS)的免疫肿瘤治疗药物。
(在肿瘤临床研究中,OS被认为是评估治疗效果的金标准)。与此同时,
NCCN指南最新版将Opdivo作为唯一的一类推荐用药用于该类患者的单药治疗。
Opdivo(图片来源deutsche-apotheker-zeitung.de)
该适应症的批准是基于一项代号为CheckMate-141的III期临床研究结果,因疗效特别显著而提前终止,独立数据监测委员会(DMC)对研究数据进行评估后认为,与对照组相比,Opdivo治疗组在总生存期(OS)方面具有显著优越性。
使用Opdivo的患者的一年生存率是36%,中位生存期是7.5个月,有效率是13.3%。而使用化疗药物的一年生存率只有16.6%,中位生存期5.1个月,有效率只有5.8%。同时,使用Opdivo产生3-4级严重副作用的比例只有13.1%,而使用化疗药物有35.1%。
另外,其他公司的PD-1/PD-L1抑制剂在头颈癌领域也做了布局,下图是小编统计的部分登记在册的临床研究:
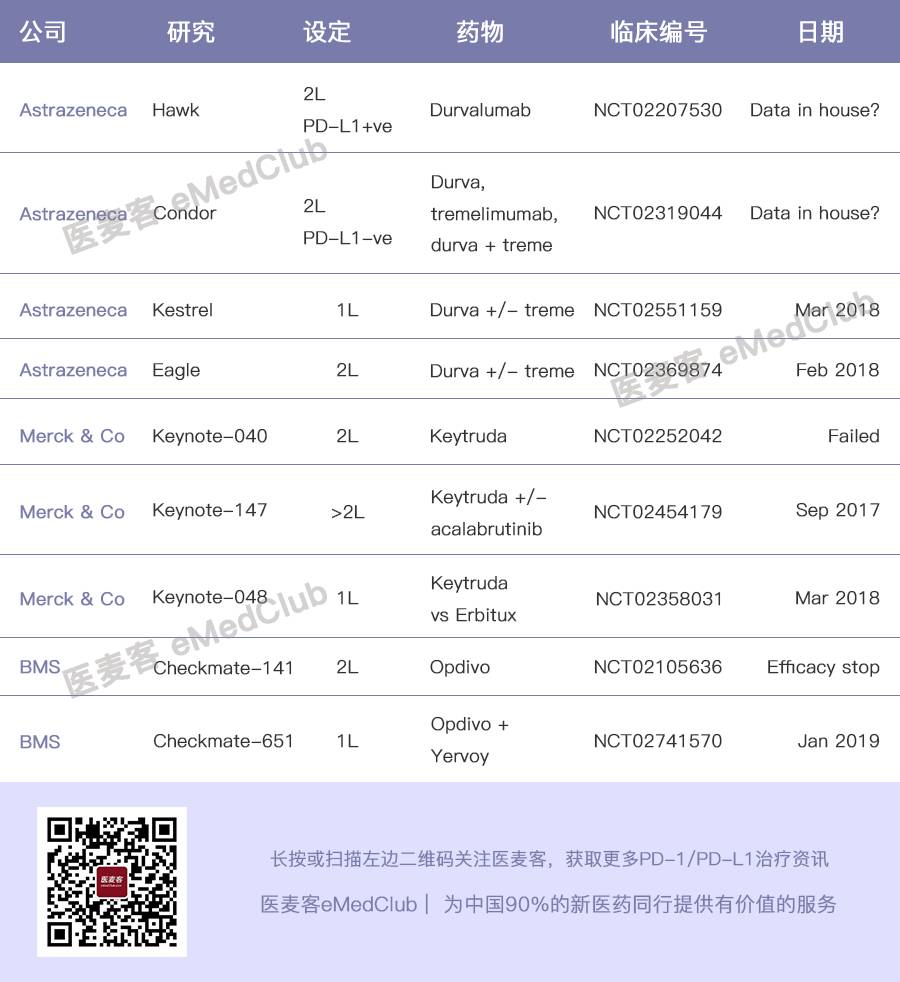
治疗头颈癌的检查点抑制剂临床研究
撇开头颈癌不说,在Opdivo一线治疗NSCLC失败、Tecentriq治疗膀胱癌失败的大背景下, Keytruda却在这些适应症上都成功了,所以业界一度认为Keytruda略胜一筹,甚至墙都不扶就服Merck。
但是最近Keytruda先是因为治疗多发性骨髓瘤的用药组死亡人数高于对照组,从而叫停了Keynote-183、Keynote-185两项III期临床试验,这次又在治疗头颈癌的III期研究中翻船
,现在的局势真是优点让人说不清了。
当然这不单单只是Keytruda本身所遭遇的挫折,客观上来说,这个事情的潜在影响还是有多方面的,
它还引发了关于检查点抑制剂试验设计的新问题,以及美国FDA在监督这些药物审批过程中所扮演的确切角色。
现如今,关于PD-1/PD-L1的作用机制已经通过了概念验证这一阶段,目前的大量临床研究则是在确定该疗法的适用范围。但却在三期临床研究上频频出现失败的现象,这不禁引人思考?
Opdivo治疗胶质母细胞瘤的一项III期研究失败
2017年4月,BMS宣布一项评估Opdivo治疗首次复发的多形性胶质母细胞瘤(GBM)疗效和安全性的临床研究未能到达主要终点,
相比贝伐珠单抗单药治疗未能显著延长患者总生存期(OS
)。
该项试验是代号为CheckMate-143的III期研究,也是是PD-1类免疫检查点抑制剂在胶质母细胞瘤中开展的第一项随机研究。除此之外,
BMS另外两项代号为CheckMate-498 和CheckMate-548的研究将继续正常进行。
Tecentriq治疗膀胱癌的一项III期研究失败

















