▎药明康德/报道
近日,诺华(Novartis)公司证实适用于严重斑块性银屑病的上市药物Cosentyx在一项3期长期扩展研究中取得里程碑性良好结果,获得了5年长的有效性和安全性数据。
银屑病是一种常见非传染性的自身免疫性疾病,全球内影响1.25亿多病人。斑块性银屑病是其最常见的疾病形式,皮肤组织呈现有覆盖白色死皮细胞的红色斑块。银屑病不仅仅是一个美容层面的问题,而且持续长期给患者带来痛苦,每天影响生活的方方面面;高达30%的银屑病患者还可能疾病进展。更严重的是,银屑病也会引起银屑病关节炎(PsA),造成疼痛、僵硬和不可逆的关节损伤。研究发现,银屑病也与糖尿病、心脏病和抑郁症等其它严重的健康状况有关。
全人源化单克隆抗体Cosentyx于2015年1月推出,是一种特异性抑制白介素-17A(IL-17A)细胞因子的靶向治疗方案。研究表明,IL-17A可能在促进银屑病、银屑病关节炎和强直性脊柱炎(AS)等疾病的自身免疫反应中的炎症状态起重要作用。Cosentyx已经在75个国家被批准用于治疗中度至重度斑块性银屑病,其中包括美国、加拿大、欧盟、日本、瑞士和澳大利亚。在欧盟,Cosentyx被批准用于中度至重度斑块性银屑病成人患者的一线全身性治疗。在美国,Cosentyx被批准用于治疗中度至重度斑块性银屑病成年患者,他们是全身性治疗或光疗方案的候选者。Cosentyx也是在70多个国家获得批准用于治疗活跃PsA和AS的首个IL-17A抑制剂。在日本,Cosentyx也被批准用于治疗PsA和脓疱性银屑病。
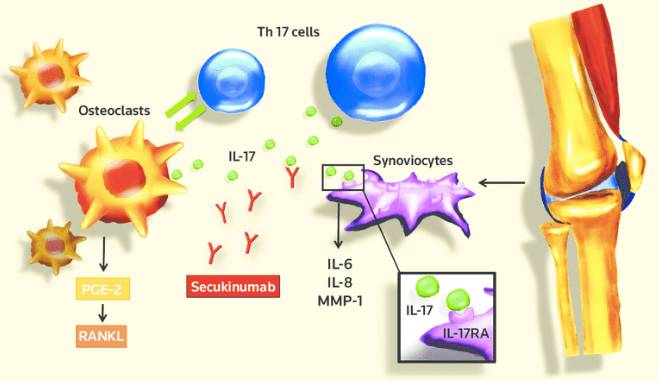
▲Cosentyx是一种特异性抑制白介素-17A细胞因子的靶向治疗方案(图片来源:《Drugs of Today》)
2016年在这同一3期研究中获得的4年数据显示,在第1至第4年的疗期中,许多患者受益于Cosentyx,获得几乎清晰健康或完全清晰健康皮肤(银屑病区域严重性指数PASI 90指标为66%,PASI 100指标为44%)。
使用Cosentyx治疗中度至重度斑块性银屑病的延伸研究(NCT01406938)旨在评估双盲期(长达4年)和5年(第260周)开放标签期间的长期安全性和有效性。Cosentyx的数据分析包括在第12周达到PASI 75反应、随后在300毫克剂量Cosentyx持续治疗直到第5年结束的所有患者。该研究包括对延长治疗的PASI 75/90/100应答率的、体表面积(BSA)和绝对PASI评分分析、BSA 1%以下的患者比例、PASI和BSA平均改善以及Cosentyx的安全性。

▲诺华公司药物开发全球负责人兼首席医学官Vas Narasimhan博士(图片来源:诺华官网)
诺华公司药物开发全球负责人兼首席医学官Vas Narasimhan博士说道:“Cosentyx一直表现出持续的疗效和安全性,为银屑病患者提供了一种新的长期护理标准。 伴随5年随访的第一批数据,Cosentyx继续证明它可以献给银屑病患者清晰健康的皮肤。”
参考资料:
[1] Novartis AG (NVS) Confirms 5 Year Data For First And Only Fully-Human IL-17A Inhibitor Cosentyx Reinforcing Sustained Efficacy And Safety Profile In Psoriasis
[2] Novartis官方网站

















