这是唐海宝老师GitHub上的JCVI工具的非官方说明书。该工具集的功能非常多,但是教程资料目前看起来并不多,因此为了能让更多人用上那么好用的工具,我就一边探索,一边写教程
这一篇文章教大家如何利用JCVI里面的工具绘制点图,展现两个物种之间的共线性关系, 用到的工具就是
jcvi
.
graphics
.
blastplot
,但是前期整理数据稍微麻烦一些。
在分析之前,你需要从PhytozomeV11 下载A.thaliana和Alyrata的CDS序列,保证文件夹里有如下内容
Alyrata_384_v2.1.cds.fa.gz Athaliana_167_TAIR10.cds.fa.gz
Alyrata_384_v2.1.gene.gff3.gz Athaliana_167_TAIR10.gene.gff3.gz
我们在做CDS相互比对的时候只需要有每个基因最长的转录本即可,因此我用我写的一个脚本
get_the_longest_transcripts
.
py
提取每个基因的最长转录本,见 基因组共线性工具MCScanX使用说明
zcat Alyrata_384_v2.1.gene.gff3.gz | python ~/scripts/python/get_the_longest_transcripts.py > aly_lst_gene.txt
zcat Athaliana_167_TAIR10.gene.gff3.gz | python ~/scripts/python/get_the_longest_transcripts.py > ath_lst_gene.txt
其中
xxx_lst_gene
.
txt
的格式如下, 第一列是基因名,第二列是mRNA编号,后面几列是位置信息。
$ head ath_lst_gene.txt
AT4G19470.TAIR10 AT4G19470.1.TAIR10 Chr4 10612993 10614339 -
AT5G43860.TAIR10 AT5G43860.1.TAIR10 Chr5 17630450 17632312 +
AT1G68650.TAIR10 AT1G68650.1.TAIR10 Chr1 25775741 25777874 +
AT1G28050.TAIR10 AT1G28050.1.TAIR10 Chr1 9775528 9777810 -
AT3G59880.TAIR10 AT3G59880.1.TAIR10 Chr3 22120969 22121700 +
AT1G22030.TAIR10 AT1G22030.1.TAIR10 Chr1 7759164 7760556
-
AT5G24330.TAIR10 AT5G24330.1.TAIR10 Chr5 8295147 8297068 -
AT5G43990.TAIR10 AT5G43990.2.TAIR10 Chr5 17697889 17702005 +
AT1G11410.TAIR10 AT1G11410.1.TAIR10 Chr1 3841286 3844432 +
AT4G32890.TAIR10 AT4G32890.1.TAIR10 Chr4 15875470 15876762 +
由于基因名和mRNA编号里有在提取CDS不需要的内容,因此要进行删除
sed -i 's/\.v2\.1//g' aly_lst_gene.txt
sed -i 's/\.TAIR10//g' ath_lst_gene.txt
之后我们就可以根据第二列进行提取CDS
seqkit grep -f cut -f 2 ath_lst_gene.txt ) Athaliana_167_TAIR10.
cds.fa.gz > ath.cds
seqkit grep -f cut -f 2 aly_lst_gene.txt ) Alyrata_384_v2.1.cds.fa.gz > aly.cds
提取的CDS编号里面也有一些不需要的内容,所以也要删除
sed -i 's/\.t.*//' aly.cds
sed -i 's/\..*//' ath.cds
此外还需要基因的位置信息的bed文件
awk '{print $3"\t"$4"\t"$5"\t"$1"\t0\t"$6}' ath_lst_gene.txt | sort -k4,4V > ath.bed
awk '{print $3"\t"$4"\t"$5"\t"$1"\t0\t"$6}' aly_lst_gene.txt | sort -k4,4V > aly.bed
最后保证有以下四个文件
$ ls ???.???
aly
.bed aly.cds ath.bed ath.cds
BLAST比对
makeblastdb -in ath.cds -out db/ath -dbtype nucl
blastn -num_threads 20 -query aly.cds -db db/ath -outfmt 6 -evalue 1e-5 -num_alignments 5 > aly_ath.blast
用
jcvi
.
compara
.
blastfilter
对结果进行过滤
python -m jcvi.compara.blastfilter aly_ath.blast --sbed ath.bed --qbed aly.bed
运行过程中有如下输出信息
19:59:15 [base
] Load file `aly.bed`
19:59:16 [base] Load file `ath.bed`
19:59:16 [blastfilter] Load BLAST file `aly_ath.blast` (total 49887 lines)
19:59:16 [base] Load file `aly_ath.blast`
19:59:16 [blastfilter] running the cscore filter (cscore>=0.70) ..
19:59:16 [blastfilter] after filter (42023->26531) ..
19:59:16 [blastfilter] running the local dups filter (tandem_Nmax=10) ..
19:59:16 [blastfilter] after filter (26531->24242) ..
最后输出
aly_ath
.
blast
.
filtered
用于做图
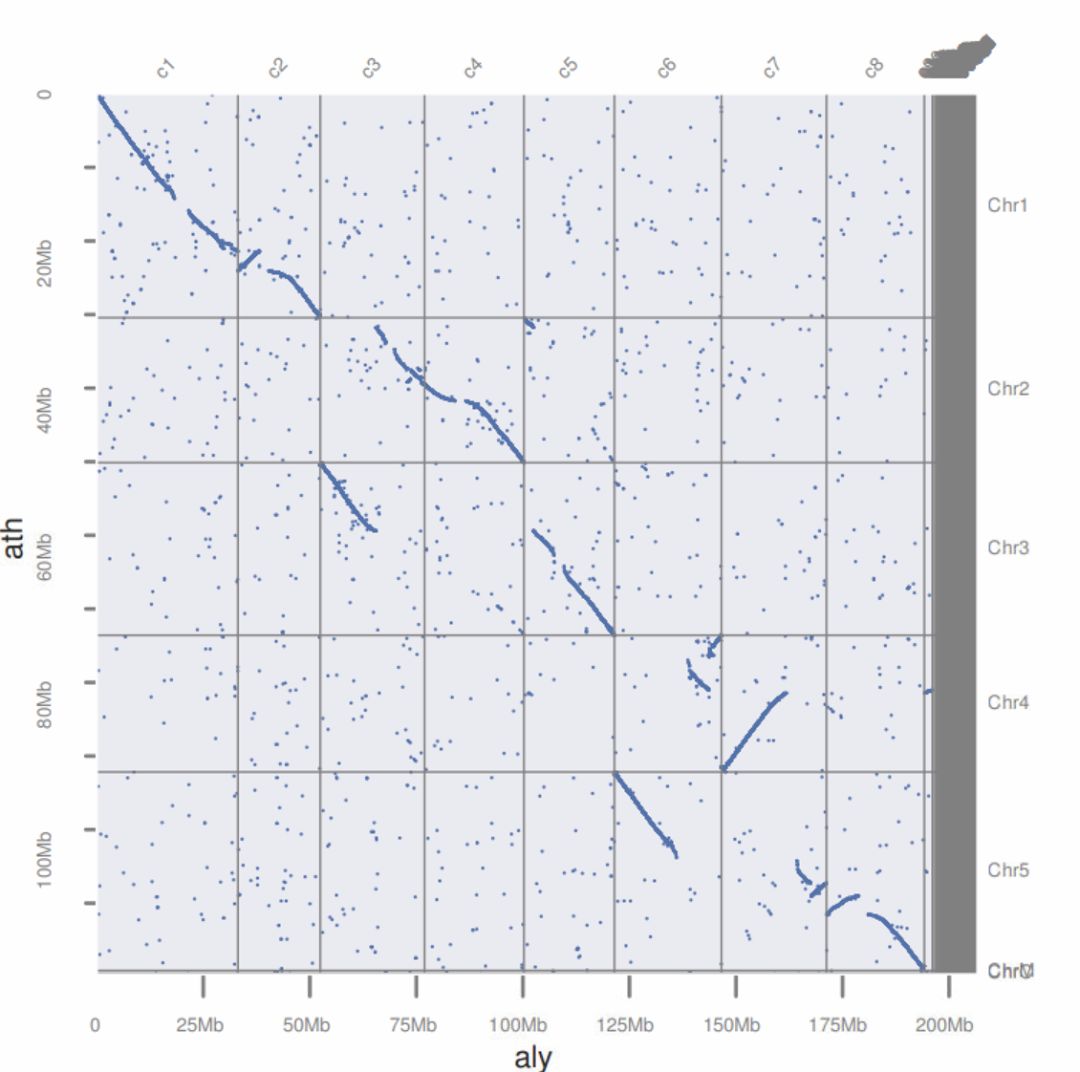
python -m jcvi.graphics.blastplot aly_ath.blast.filtered --sbed ath.bed --qbed aly.bed
最后点图如下