
本文转载自“生命奥秘”。
Aviv Regev是一位生物分析专家。现在,她正致力于绘制人体的每一个细胞。
计算生物学家Aviv Regev喜欢做一些看似不可能完成的任务。2011年,她与分子遗传学家Joshua Levin合作,测试了RNA测序的几种方法。科学家们在测试几种技术的极限,以查看哪种方法表现最佳。他们用降解RNA或极少量的分子来处理样品。最终,Levin指出,一些技术的灵敏度非常高,能检测含量低于单细胞中含有的RNA量的样本。
对于Regev来说,这似乎是个好机会。细胞是生命的基本单位,她长期以来一直在寻找探索复杂的基因网络在单个细胞中的运作机制的方法,并想了解各个细胞中这些网络有何差异,以及最终各种细胞群体如何协同工作。这些问题的答案将从本质上揭示细胞如何构建复杂的生物体,如人类。就职于博德研究所(Broad Institute of MIT and Harvard)的Regev和Levin对18个来自小鼠骨髓的、看似相同的免疫细胞进行了RNA测序,结果发现其中一些细胞与其余细胞的基因表达模式截然不同。这些细胞感觉就像两个不同的细胞亚型。
这使得Regev想进一步开展深入的研究,即使用单细胞测序来了解人体内存在多少种不同的细胞类型、它们在哪个部位,以及它们如何发挥作用。Regev的实验室同时对18个细胞进行检测,一共测定了数十万个RNA的序列,并将单细胞分析与基因组编辑技术结合起来,以了解关键调控基因被抑制时会发生什么情况。
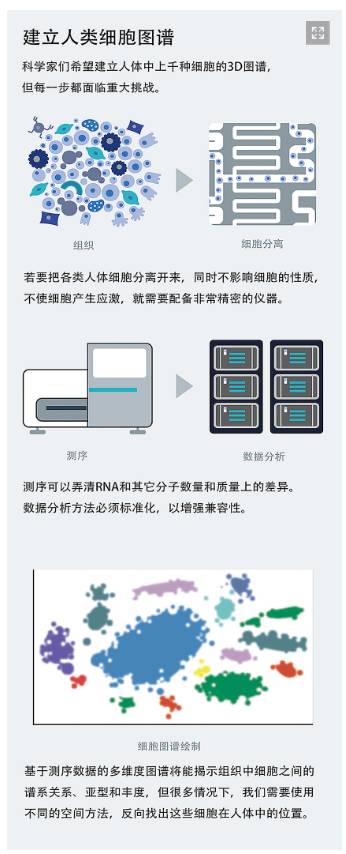
他们的结果发现了一些新的细胞类型——例如,识别两种新型视网膜神经元。Regev还希望找到更多的细胞类型。2016年底,她帮助推出了“国际人体细胞图谱计划(Human Cell Atlas)”。该计划雄心勃勃,准备对人体中所有(估计37万亿个)细胞进行分类和测序(图“建立人类细胞图谱”)。瑞典皇家理工学院(Royal Institute of Technology)的微生物学家Mathias Uhlén指出,现在测绘单个细胞的研究越来越流行了,他认为,人体细胞图谱计划会是历史上最重要的生命科学项目之一,它甚至要比人类基因组计划更重要。
纽约市纪念斯隆凯特琳癌症中心(Memorial Sloan Kettering Cancer Center)的计算生物学家、认识Regev已有18年的Dana Pe'er表示,Regev就喜欢这种大规模的的项目。Regev非常独特的一点是她的视野非常开阔。Pe'er从来没有见过一个科学家,能同时深入而创新地思考这么多事情。
1Regev选择的课程
当Regev还是以色列特拉维夫大学(Tel Aviv University)的本科生时,学生们必须在开始学习之前选择一门课程。但她不想选择。事实上,她选择了一个先进的跨学科项目,让她可以同时学习多个学科,跳过学士学位,直接攻读硕士。
她本科期间的转折点是得到了进化生物学家Eva Jablonka的指导。Jablonka提出了一个备受争议的、关于表观遗传进化的理论。Regev佩服Jablonka面对批评的勇气和坦率。Regev认为,容易走的路总是很多,但选择走困难的路的人更让人印象深刻。
Jablonka的课程涉及Regev喜爱的复杂的遗传学问题。遗传学依赖于抽象推理的方式来达成基本的科学结论,Regev为此深深着迷。她对生物着迷,觉得基因非常有趣,但更有趣的是基因之间的相互协作。而基因彼此协作的第一媒介是细胞。
Regev在以色列魏兹曼科学研究所(Weizmann Institute of Science)的Ehud Shapiro实验室攻读计算生物学博士学位。2003年,她通过特殊的项目(一个允许研究者在没有博后经历的情况下,直接建立个人实验室的项目),搬到了哈佛大学(Harvard University)的剑桥基因组学研究中心(Bauer Center for Genomics Research)。在那里Regev拥有属于自己的独立的小团队,这使她能够决定自己的研究课题。她着重于通过观察细胞中基因产生的RNA分子来分析遗传网络。2004年,她将这种技术应用于肿瘤,由此发现了不同类型癌症共享的基因表达模式,以及一些更具体的基因表达模式,如一组与生长抑制有关的基因在急性淋巴细胞白血病中被抑制了。到了2006年,也就是她35岁之际,她在博德研究所(Broad Institute)成立了自己的实验室。
2明显的相似
在博德研究所,Regev继续致力于研究如何从RNA测序数据中筛选出复杂的信息。2009年,她发表了一篇关于小鼠树突状细胞的文章,揭示了控制这种免疫细胞应对病原体的基因网络。2011年,她开发了一种在不使用参考基因组的情况下,组装出完整的转录组(样本中基因转录得到的所有RNA)的方法,这种技术在生物体的基因组未被深入测序时非常很重要。
就在那时,Levin提出了对单个细胞内RNA进行测序的前景。在此之前,单细胞基因组学几乎是不可能的,因为该技术不够灵敏,无法检测一个细胞内的微量RNA或DNA。但在2011年左右情况开始发生变化。
Regev等人使用18种免疫细胞——也是树突状细胞——来测试她设计的方法。Regev当时的博士后,现在就职于纽约基因组中心(New York Genome Center)的Rahul Satija指出,他当时坚持他们做的实验会证明同样类型的细胞的检测结果是相同的。然而结果并非如此,他发现了两种完全不同的细胞亚型。即使是同一亚型里,个体细胞的调控表达和免疫基因都存在很大的差异。据Regev回忆,那是很小的一个研究,但却她们发现了很多信息。
Satija指出,他觉得Regev恐怕一开始就猜到了这样的结果。当看到那些结果时,她们就知道后面应该做哪些事情。她们计划使用单细胞基因组学揭示细胞的多样性,对生物体内的细胞类型重新做一次划分,并了解这些细胞是如何互动的。
在标准遗传测序中,研究人员会从许多细胞的混合物中提取DNA或RNA,以产生整个细胞群体的平均读数。Regev将这种方法比喻成水果冰沙。颜色和味道都能提示冰沙的成分,但是其中一个甚至十几个蓝莓的味道,很容易就被一堆草莓所覆盖。
Regev指出,相比之下,单细胞数据就像水果沙拉。你可以轻而易举地将蓝莓和黑莓分开。这有助于揭示细胞的多样性。基于此,生物学家可以使用单细胞基因组学来对肿瘤进行序列分析,以确定哪些基因被恶性细胞表达、哪些被非恶性细胞表达,哪些被免疫系统或血管表达——这可能可以推动新型癌症药物的开发工作。
该技术还能帮助开发其它多种疾病的药物。在全面分析哪些细胞高表达致病基因的情况下,了解哪些基因是潜在的药物靶标更具临床意义。
Regev不是唯一一个迷恋大规模单细胞分析的人。至少从2012年起,科学家们就一直有使用这些技术来绘制人类其它细胞类型的想法。加州斯坦福大学(Stanford University)生物工程师、陈-扎克伯格生物科技中心(Chan Zuckerberg Biohub, CZ Biohub)的共同负责人Stephen Quake表示,几乎同时,世界多个地区都各自提出了这种想法。2016年9月以来,CZ生物科技中心一直为各种生物医学研究项目,包括该中心自己的细胞图谱计划提供资金。
3人类细胞图谱
2014年左右,Regev开始举办关于细胞测绘的讲座和研讨会。来自英国维康信托桑格研究所(Wellcome Trust Sanger Institute)的细胞遗传学主管Sarah Teichmann听说了Regev的想法,并于去年联系她,问她是否愿意合作建立一个国际人体细胞图谱项目。该项目不仅需要基因组学研究人员的参与,还需要各种组织和器官系统的生理学专家参与。
Regev抓住了这个机会,她和Teichmann现在是人体细胞图谱计划(Human Cell Atlas)的联合负责人。该项目计划对人体各种细胞的RNA进行测序,然后使用这些基因表达谱将细胞分类,定义新的细胞,并绘制所有细胞及其分子在空间上的组织方式。
该项目还旨在发现和表征人体中所有可能的细胞状态——成熟和不成熟、满负荷和充分工作状态——这需要更多的测序。科学家们认为,人体内大约有300种主要的细胞类型,但是Regev认为人体内的细胞类型和状态远超过这个数字。Regev认为,视网膜似乎含有超过100种神经元亚型。目前,人体细胞图谱计划的研究者们已经齐聚一堂,集中努力研究免疫细胞、肝脏和肿瘤。Teichmann指出,现在项目还处于起步阶段。
Regev在部署人体细胞图谱项目时,建立了包括来自5个大陆的、总计28人的委员会,并协助组织了500多名科学家参与的会议。对此,Jablonka表示,要是他,肯定会不堪重负。但Regev没有。Regev只是简单地觉得,与其他人拥有一个共同的目标是非常有趣的。
目前我们尚不清楚该项目如何拉到充足的资金赞助。但是在6月,加州帕洛阿尔托市的慈善组织陈-扎克伯格倡议(Chan Zuckerberg Initiative,扎克伯格夫妇建立的慈善组织,她资助了前文提到的CZ Biohub)为人类细胞数据平台(将用于存储、分析,并浏览项目数据)提供了一笔资金(具体金额未披露)和软件工程支持。Teichmann认为,数据管理的需求是大项目和小项目的根本差别。计算部分是项目的核心,统一的数据处理和数据浏览等,显然是非常有益的。
4月,陈-扎克伯格倡议也接受了为期一年的试点项目的申请,以测试和开发人体细胞图谱计划的技术和实验程序,并预计在短时间内公布哪些项目会得到资助。其实任何人都可以申请这项资金,并不会不局限于参加该计划的科学家。
4人才流失
一些科学家担心,人体细胞图谱计划将耗尽其它研究项目的资金和努力——这是许多类似大型国际大科学项目都会受到的批评。Regev实验室的博士生Atray Dixit指出,确实有这个压力。我们知道会得到很多重要发现,从学术意义上来讲,这个项目是低风险的。但成本太高了。我们应该思考如何在学术意义和经济成本之间寻找平衡。
英国剑桥大学(University of Cambridge)的发育生物学家Azim Surani不确定该项目是否能够平衡数据量和信息深度。他表示,人体细胞图谱给你的是一幅很大的图,但你并不能深入地了解不同的细胞类型,以及它们之间的关系。因此很难说人体细胞图谱计划的投入产出比有多高。
Surani也怀疑单细胞基因组学是否已经成熟到足以开展一个大项目。他提出,技术已经成熟到你可以充分利用它了吗?例如,细胞提取——在无偏向且不影响RNA品质的情况下,从组织中提取单细胞——仍然是非常困难的。如果很多团体独立摸索这个问题以及其它类似的问题,效果可能会比现在直接开展大规模细胞图谱绘制要好。
很多人还担心这个项目何时才能完成。人类蛋白质图谱计划(Human Protein Atlas,一个自2003年以来一直对正常细胞和癌细胞中的蛋白质进行编目的大型国际项目)的负责人Uhlén指出,细胞类型的定义并不明确。人体中可以表征的细胞类型可能是无限的。人体细胞图谱计划的确是重要且令人兴奋的,但我们需要非常清楚,哪里是终点?
Regev认为完成不是唯一的目标。计划是模块化的,你可以把它分解成很多碎片。即使解决问题的一部分,也具有重要意义。她还表示,即使该项目只是对视网膜中的所有细胞进行编目,也会对药物开发非常有用。时间会证明它的价值。
Regev对人体细胞图谱计划的关注并没有妨碍她对特定细胞类型的研究。去年12月,她的团队和其他两个小组分别发表了研究成果,研究使用精密基因编辑工具CRISPR-Cas9在大批细胞中关闭转录因子和其它调节基因,然后使用单细胞RNA测序观察效果。Regev的实验室将这种技术称为Perturb-seq。
Perturb-seq目的是通过关闭每个细胞中的一个或多个基因,然后测定它们如何影响其它的基因,从而实现大规模、精确地分离遗传途径。以往研究人员只能同时操作少量基因,但是Perturb-seq可以一次处理1000甚至10000个基因。得出的结果将可以揭示基因如何相互调控,以及一次激活或失活多个基因的综合作用——单独操作单个基因是无法揭示这一点的。
该论文的共同第一作者Dixit指出,Regev工作起来没日没夜。提交论文的前几周,她每天6点召开项目会议。Dixit在论文补充方法的末尾写了一句笑话——此句只是为了看看有没有人会读到这里。Regev在凌晨3点发现了这个句子。那是他们论文提交的前一天晚上。也就是说,Regev3点还没睡,6点可是要组织开会的。
Regev的工作强度和高度聚焦源自于她的无限热爱。Regev认为自己是非常幸运的人,做的是她最爱的事情。Regev还热爱细胞。无论怎么看,对她来说,细胞都是神奇而迷人的。
















