
欢迎点击「PaperRss」↑关注我们!
The Journal of Cell Biology
近日以长文形式发表了杨崇林研究组和郭伟翔研究组的最新联合研究论文
(J. Cell Biol. 216(10): 3307-3321)
。该论文揭示了一个新的神经发育的关键蛋白
-WDR91,
并阐明了其作为小
GTP
酶
Rab7
效应因子在溶酶体运输通路中发挥重要作用
(
http://jcb.rupress.org/cgi/content/abstract/jcb.201705151
)
。
内吞体
-
溶酶体运输调控细胞内信号转导、细胞膜修复、细胞迁移和神经轴突生长等过程,对于维持细胞稳态和发育至关重要。其中,早
-
晚期内吞体的转换是内吞体
-
溶酶体运输的关键环节。早
-
晚期内吞体的转换需要将早期内吞体上的特征性小
GTP
酶
Rab5
和磷脂酰肌
-3
磷酸
(PtdIns3P)
转换为晚期内吞体上的特征性小
GTP
酶
Rab7
和磷脂酰肌
-3
,
5
二磷酸
((PtdIns(3,5)P
2
)
。杨崇林课题组的前期研究发现了线虫中的两个蛋白
SORF-1
和
SORF-2
,它们相互作用并与内吞体上磷脂酰肌
-3
磷酸激酶
(
PI3K)
复合体互作
,
从而抑制
PtdIns3P
的合成,促进早
-
晚期内吞体转化。
SORF-1
和
SORF-2
的人类同源蛋白
WDR91
和
WDR81
以同样机制发挥作用
(Liu K et al., 2016, J Cell Biol.212(2):181-198)
。
在本研究中,杨崇林课题组和郭伟翔课题组合作发现
WDR91
通过其
C-
端与活化形式的
小
GTP
酶
Rab7
结合,从而被招募到内吞体上。同时,
WDR91
通过其
N-
端与
PI3K
复合体的
Beclin1
亚基相结合。
WDR91
因而特异地在内吞体上抑制
PI3K
复合物的活性,从而使内吞体转换所需要的
Rab5-Rab7
转换与
PtdIns3P-PtdIns(3,5)P
2
转换同步进行。
Wdr91
敲除
小
鼠在出生后几个小时内发生死亡。而在脑组织中特异性敲除
Wdr91
后,小鼠表现为大脑发育异常,在出生
3
至
4
周后死亡。在缺失
Wdr91
的原代神经元中,有大量异常增大的内吞体存在,
并且神经元树突的长度和复杂度均显著降低。这些内吞体缺陷和神经发育缺陷可被野生型
WDR91
蛋白恢复,但却不能被与
Rab7
结合的有缺陷的
WDR91
突变蛋白恢复。该研究表明
WDR91
是
Rab7
的一个新的效应因子,在对神经元的发育中发挥不可或缺的作用。
同期
J. Cell Biol.
以
Spotlight: A new Rab7 effector controls phosphoinositide
conversion in endosome maturation (
Casanova J. and Winckler B. 2017. J. Cell Biol. 216(10): 2995-2997)
为题,对该研究作了亮点评述。
杨崇林研究员和郭伟翔研究员为该论文的共同通讯作者。
杨崇林研究组已毕业博士生刘锴、郭伟翔研究组的博士生邢如晓、杨崇林研究组的蹇友理副研究员和高之扬副研究员为该论文的共同第一作者。该研究受到国家重点基础研究发展计划、国家自然科学基金委、中科院跨学科创新团队、中科院前沿科学研究重点项目资助。
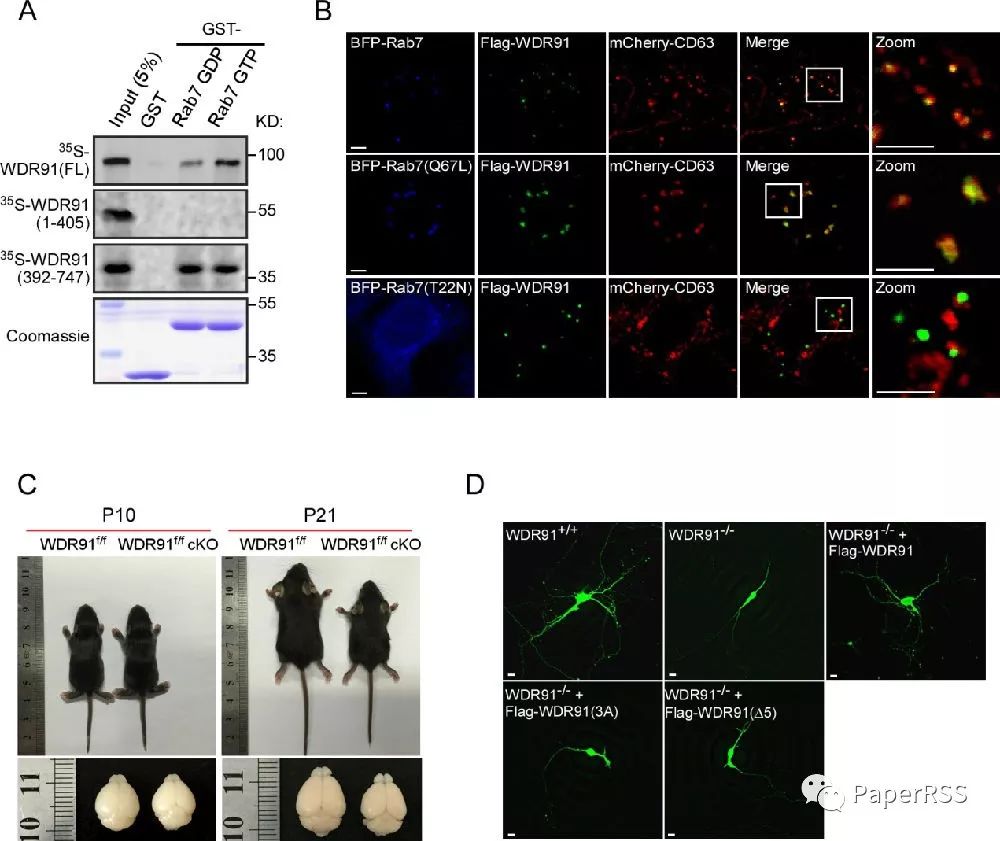
A.WDR91
与活性形式
GTP-rab7
的相互作用。
B.WDR91
被野生型
Rab7
或持续活化的
GTP-Rab7(Q67L)
招募到内吞体上。
C.
脑组织特异性敲除
Wdr91
小鼠的大脑发育异常。
D.
野生型
WDR91
而非
Rab7
结合缺陷性的
WDR91
突变体使
缺失
Wdr91
的异常原代神经元恢复为正常。


如果您觉得这篇文章不错,请转发到您的朋友圈吧!
( 免责声明: 本文中的部分信息援引自网络。本公众号发布的图文一切仅为分享交流,并不代表本公众号的观点。所有援引自网络的部分,其版权归原作者、原公号或原网站所有,如有涉及版权敬请及时告诉我们,定将及时删除或妥善处理。)

长按下面二维码,关注我们!
觉得不错点个赞吧!




