
本文原载于《
中华眼科杂志》2017年第9期
近年来,角膜内皮移植术(endothelial keratoplasty,EK)在全球发展迅速,成为治疗角膜内皮功能失代偿的主要手术方法。美国角膜移植手术的年手术量约为45万,2005年至2014年,穿透性角膜移植术(penetrating keratoplasty,PKP)的比例从94.9%降至41.5%,而EK的比例从3.2%增加到55.9%
[1]
。EK可保留正常的角膜上皮和基质,仅去除病变的内皮层,保证了角膜前表面结构和功能的完整性,并且手术无需缝线,减少了发生散光的可能,术后视力恢复快
[2,3]
,可显著提高患者术后的视觉相关生活质量
[4]
。随着EK技术的发展,手术适应证也发生了变化。在美国,因Fuchs角膜内皮营养不良(Fuchs endothelial dystrophy,FCED)行PKP者2005年占PKP总量的13.6%,2014年占3.1%;因大疱性角膜病变者2005年占19.8%,2014年占8.7%。而角膜内皮病变行EK的比例升高,2014年因FCED和大疱性角膜病变行EK者分别占患病总人数的90%和60%
[1,5]
。
EK主要包括以下几种术式:(1)剥离后弹力层EK(descemet stripping endothelial keratoplasty,DSEK)和剥离后弹力层自动EK(descemet stripping automatic endothelial keratoplasty,DSAEK);(2)后弹力层EK(descemet membrane endothelial keratoplasty,DMEK);(3)超薄植片-自动角膜刀剥离型后弹力层EK(UT-descemet stripping automatic endothelial keratoplasty,UT-DSAEK)。目前EK手术疗效尚未达到临床医师的预期效果,存在术后视力改善不理想、并发症多等问题。
一、手术适应证
在西方国家,FCED是主要的致盲性角膜病。在年龄为40岁以上的人群中,FCED的发病率为4%
[6]
。FCED是美国角膜移植手术的主要适应证,约占全部角膜移植手术的22%
[1]
。而我国FCED的发病率较低,在50岁以上的老年性白内障患者中,发病率仅为0.8%
[7]
。在美国,因角膜内皮功能失代偿行角膜移植手术的手术指征为角膜内皮细胞功能障碍、角膜水肿及上皮下大泡、视力低于0.4或患者对视力有更高诉求
[8]
。而我国角膜内皮功能失代偿患者行角膜移植手术的指征更为严格。
DSEK、DSAEK及UT-DSAEK在眼前房具有足够手术空间的前提下,适用于所有角膜内皮功能失代偿患者,包括眼部存在合并症,如青光眼分流装置、虹膜周边前粘连、虹膜异常(先天性无虹膜、虹膜萎缩或虹膜部分缺失)、无晶状体和(或)前房IOL等。DMEK不适用于以下情况:(1)植片较薄,易卷曲,易脱位进入后房;(2)较薄植片在展开过程中容易被青光眼分流装置的分流管划伤,甚至脱入管腔中;(3)眼压不易控制,术中植片在前房中不宜展开,术后植片脱位风险高(表1)
[9]
。
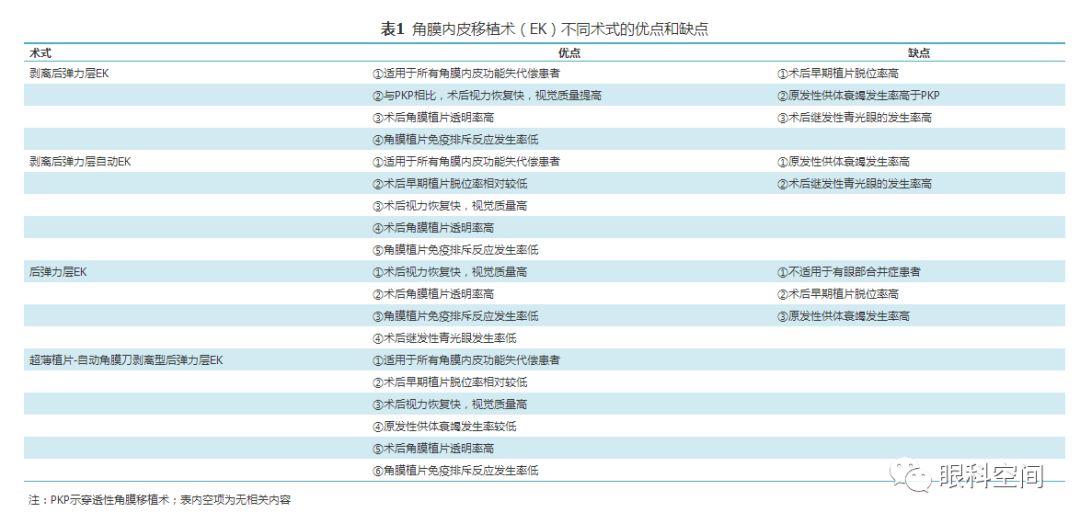
二、术后视觉效果
EK符合角膜的解剖形态,无缝线引起的术后角膜散光,视力恢复快,视觉效果较PKP明显提高
[10]
。欧美国家患者EK术前平均视力为20/100~20/50(视力范围为眼前手动至20/25),不同术式患者术前视力无明显差异
[11,12,13,14]
;我国患者EK术前平均视力均低于20/125
[15]
。而DSEK术后38%~100%的患者视力达到20/40,且术后视力逐年提高
[5]
。术后1年,约26%患者达到20/25;术后5年,约56%患者可达到20/25,提示术后发生角膜重塑
[12]
。DSAEK使用微型角膜刀制作供体植片,植片厚度更精确一致,基质界面更光滑,术后视觉效果更好,并且可预先制作供体植片,降低了手术难度。Li等
[16]
的研究结果表明,DSAEK术后6个月,36%患者最佳矫正视力达到20/25;术后3年,70%患者达到20/25。DMEK仅移植后弹力层和内皮层,更符合角膜的解剖结构,术后视力恢复更快,视觉效果更好。术后1个月平均视力即可达到20/30;术后6个月,30%~47%患者达到20/20
[17,18]
;术后1年,41%患者达到20/20,80%患者达到20/25
[13]
,且术后视力长期稳定
[19]
,视觉效果明显优于DSEK和DSAEK(表1)
[14,20]
。UT-DSAEK和DSAEK相比,植片厚度更薄,术后视觉恢复效果更好,术后1年患者视力可达到DMEK的水平(表1)
[21]
。Busin等
[22]
的研究结果表明,UT-DSAEK术后6个月,26%患者视力达到20/20;术后1年,40%患者达到20/20;术后2年,50%患者达到20/20。
EK术后影响视觉恢复的主要因素为眼底病变和眼部严重合并症
[23]
。角膜后基质层剥离不规则或基质皱褶可影响术后视力,光学区的皱褶与植床贴附后,视力可逐渐改善
[24]
。术后植片厚度DSEK约为155 μm,DSAEK约为209 μm(147~289 μm),UT-DSAEK约为101 μm(50~145 μm)
[12,25]
,排除基质混浊等因素,术后植片越薄视力越好
[26]
。Meta分析结果表明,EK术后视力与供体植片厚度无密切相关性
[27]
。术后植片厚度在100~200 μm之间,术后视力较好;植片厚度小于131 μm,术后视力达到20/20的比例明显增高。植片过薄或过厚均可影响视觉效果
[28]
。
三、屈光状态
EK术后球镜屈光度数和柱镜屈光度数均较PKP术后明显降低。更薄的角膜植片更易贴附角膜,植片与植床的平行度增加,可优化角膜内皮面的补偿。不同术式EK术后远视偏移度数无明显差异,为+0.70~+1.50 D,主要与术前屈光状态相关
[22,29,30]
。对于联合白内障摘除手术的患者,IOL度数的计算需考虑术后远视偏移度数。高阶相差和光散射是影响术后早期视力的主要原因。植片厚度与高阶相差呈正相关
[31]
,角膜植片越薄,术后早期视觉效果越好,经过角膜重塑,术后2年可恢复至术前水平
[32,33]
。EK术后植床上皮下混浊可使患者产生眩光症状,影响视力。随着术后时间延长,症状逐渐改善,尤其年轻人症状改善明显
[34]
。
四、角膜内皮细胞丢失率
EK术后角膜内皮细胞丢失可影响植片的存活时间。Price等
[35]
回顾性研究DSEK术后1 009只眼,术后半年角膜内皮细胞丢失率为32%,每年平均丢失率为3.6%,术后10年丢失率为71%,与术后半年丢失率呈正相关,与PKP术后10年丢失率相当。Wacker等
[12]
和Price等
[36,37]
等报道角膜内皮细胞丢失率DSEK术后5年为55%,PKP术后5年为70%。DSAEK和UT-DSAEK术中使用微型角膜刀制作植片或超薄植片,对术后角膜内皮细胞密度和细胞丢失率无明显影响。Terry等
[38]
前瞻性研究DSEK和DSAEK术后角膜内皮细胞丢失率,结果显示无明显差异,术后半年均为34%,术后1年分别为39%和34%。Busin等
[22]
和Dickman等
[25]
对UT-DSAEK术后285只眼随访2年,角膜内皮细胞在6、12、24个月的丢失率分别为33%、36%、37%。DMEK手术难度大、手术时间长,但术后角膜内皮细胞丢失率与其他术式比较无明显差异
[13,36]
。
供体角膜内皮细胞密度与供体死亡-保存时间和死亡-使用时间无直接相关性
[39]
。国际运输,有利于供体角膜的全球分配和利用,对角膜内皮细胞损失的影响为2.3%,可忽略不计
[40]
。小切口EK需卷曲角膜内皮植片,且手术难度大,可造成内皮细胞损伤。Price等
[41]
对DSAEK术后患者随访3年,角膜内皮细胞丢失率手术切口直径为5 mm的患者为33%,而直径为3.2 mm的患者为60%。EK术后角膜内皮细胞密度逐渐降低,术后免疫排斥反应可增加角膜内皮细胞的丢失率
[42]
。
五、角膜植片透明率
随着EK术式的不断改进和围手术期治疗经验的增多,术后植片透明率不断提高。术后5年植片透明率DSEK为76%~95%
[36]
,DSAEK为79.4%~93%
[43]
。Busin等
[22]
对285例UT-DSAEK术后患者随访2年,植片透明率为96.2%。Hos等
[44]
对1 000例DMEK术后患者随访18个月,植片透明率接近100%。Ham等
[19]
报道,DMEK术后7年植片透明率为85%(表1)。EK术后影响植片透明率的主要危险因素包括术后植片免疫排斥反应、青光眼滤过手术史、PKP植片免疫排斥反应发作史、二次或多次PKP手术史等
[45]
。EK术后免疫排斥反应是影响植片透明的主要危险因素,发生免疫排斥反应的患者术后1年植片透明率为70%
[45]
。具有青光眼滤过手术和PKP手术史的患者,EK术后5年植片的透明率分别为22%~40%和47%
[22,36]
。
六、术后并发症
(一)术后早期植片脱位
EK手术界面光滑,术后植片脱位是早期最常见的并发症,通常为周边部脱位或部分脱位,全脱位的发生率较低。植片脱位后前房再次注入气泡,通常可使植片复位。随着手术经验的积累,植片脱位的发生率逐渐下降。开展DSEK早期,术后植片脱位的概率为0~82%
[5]
,DSAEK术后植片的脱位率为0~35%
[5,46]
。UT-DSAEK和DSAEK术后植片的脱位率无明显差异
[25]
。DMEK植片薄且界面光滑,植片脱位的概率高达62%~92%(表1)
[13,14,47]
。植片脱位的危险因素包括抗青光眼手术史(装有青光眼分流装置的患者植片脱位率增加3倍
[48]
)、后弹力层剥离不彻底、有PKP手术史等
[49,50,51]
。术中使用20%SF6气体形成前房,可减少术后植片脱位
[52]
。Terry等
[53]
认为减少术后植片脱位的关键在于手术技术,避免术后切口渗漏,实现空气密闭,清除层间积液以及适当去除受体周边角膜后基质层,均有助于供体植片贴附。DMEK手术规范化和标准化,可降低术后植片脱位的发生率和二次手术的概率,提高植片的存活率
[54]
。
(二)原发性供体衰竭
原发性供体衰竭是由于植片自身内皮细胞功能损伤而导致移植失败。PKP术后原发性供体衰竭比较罕见,发生率为1%~3%
[55]
。DSEK术后原发性供体衰竭的概率为0~29%
[5]
,提示手术操作对内皮细胞的损伤可能是造成原发性供体衰竭的主要原因。DSAEK和DMEK术后原发性供体衰竭的发生概率均约为8%
[13,14,47]
。UT-DSAEK术后原发性供体衰竭的发生概率较低,约为1.4%(表1)
[22]
。原发性供体衰竭的发生概率随着EK手术技术的进步而逐渐降低。原发性供体衰竭后需行二次手术,选择相同或不同的手术方式
[54,56,57]
,术后效果与首次手术无差异
[58]
。有青光眼手术史患者原发性供体衰竭的发生概率明显增高,约为16%
[59]
。
(三)角膜植片免疫排斥反应
EK不触及角膜缘血管且角膜前表面形态完整,术后可长期使用糖皮质激素药物,术后免疫排斥反应的发生率明显低于PKP。角膜植片免疫排斥反应可降低内皮细胞密度,从而影响植片的长期存活率
[60]
。EK术后2年为免疫排斥反应的高发期。Li等
[16]
对615只EK术眼进行分析,术后12~18个月间免疫排斥反应发生率最高。DSEK术后3个月至2年植片发生免疫排斥反应的概率为0~45%
[61]
。在有关598例行DSEK患者的大样本研究中,术后1年和2年的免疫排斥反应发生率分别为7.6%和12.0%
[61]
。DSAEK的免疫排斥反应发生率术后1年为6%~8%,2年为7%~12%,3年为9%
[41]
。UT-DSAEK患者术后1年和2年的免疫排斥反应发生率分别为2.4%和3.3%
[22]
。Anshu等
[47]
的研究结果显示,DMEK术后内皮植片的免疫排斥反应发生率是DSEK的1/15,PKP的1/20(表1)
[47]
。Hos等
[44]
回顾性总结1 000例行DMEK患者的免疫排斥反应发生率,术后1年为0.9%,2年为2.3%年,4年为2.3%,其中75%患者是由于自行停用糖皮质激素药物。EK术后发生免疫排斥反应的主要危险因素包括青光眼手术史、PKP免疫排斥反应病史、不规范使用糖皮质激素药物等。经规范药物治疗后,免疫排斥反应后的角膜植片厚度和视力无明显变化,植片可恢复透明,但内皮细胞数量下降。















