石药集团最近在国内的药品注册真得是挺抢眼的,比如:
①
石药、恒瑞出奇兵,留给“二甲双胍”们的时间可能不多了
,
②
石药「孟鲁司特钠咀嚼片」获FDA批准,又将“扰乱”一致性评价?
没过多久,石药再一次给大家送惊喜了。
根据CDE网站5月5日的信息,石药集团欧意药业达沙替尼片的生产申请正式获得CDE承办受理,受理号为CHYS1790027/8/9。一般而言,受理号中7位数字的前2位代表受理年份,后面5位代表受理流水号。但如果受理号流水号是以9开头,则代表是企业完成生物等效性后直接寄资料到国家局药审中心申请生产。
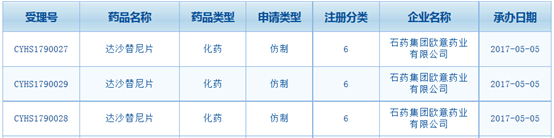
达沙替尼是BMS开发的治疗慢性髓性白血病(CML)的重磅药物,2016年全球销售额18.24亿美元,目前在国内仅有BMS原研和正大天晴的首仿上市,在研企业高达17家。石药目前是这17家企业中最快申报生产的,有望成为达沙替尼片的“二仿”企业。
说到这里,就不得不提一下双鹭药业。
正大天晴和双鹭是国内最早申报达沙替尼的两个厂家,分别于2010年6月和20
10年8月按3.1类新药申请临床。双鹭药业虽然晚了2个月,但也有自己的优势,就是对外宣称的打破了原研晶型专利,不构成上市障碍。但是在之后的临床试验推进过程中,双鹭药业逐渐被正大天晴甩在了身后。正大天晴的达沙替尼片在
2012-09-24申报生产,2013-09-17获批上市,而双鹭的生产申请(
2014-04-01
)直到正大天晴的
产品
上市后才珊珊来迟。
“拖延症”的后果就是,双鹭药业的达沙替尼赶上了2015年7月22日的临床数据自查。。。就这样,双鹭与天晴从最初的2个月之差,变成最后一个以首仿身份上市,风光无限,一个以铩羽而归,悲壮撤回。
再到如今石药集团的达沙替尼片(6类)也申请上市,更是让双鹭药业的达沙替尼片(3.1类)平添了几分悲情色彩。





