内容来源:
氢电邦
“
3060
”
粉丝
7.3
万+,
承
接
各种
商业广告
,价格从优
感谢您的认可和支持
!
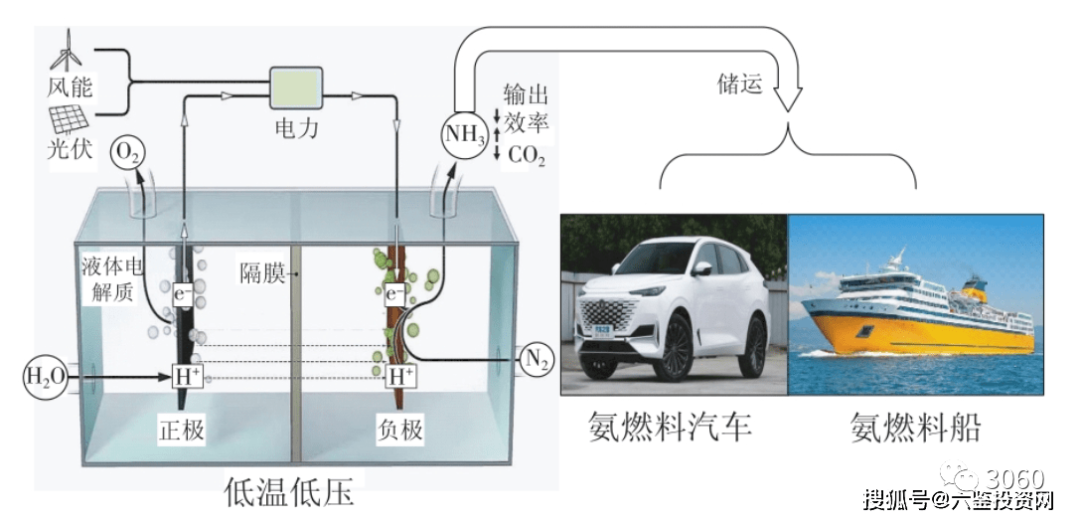
介绍了当前氨在储氢、直接燃烧与燃料电池等领域的应用,详细总结了氨裂解制氢催化剂的研发、相关反应器设计、氨
-
氢
/
甲烷共混燃烧技术以及几种重要的燃料电池等方面的研究进展,并分析了其在经济、环境、技术等方面的先进性,
指出了氨能在未来新能源领域的挑战和机遇。
01
由于化石燃料的大量使用,能源枯竭和气候恶化已成为
21
世纪人类面临的两大难题。为了应对这些威胁,各国陆续制定了新能源发展战略和减碳目标。根据国家统计局的数据
[1]
,
2021
年我国能源消费总量为
52.4
亿
t
标准煤(
SCE
),其中,作为碳排放大户的煤炭占能源消费总量的
56.0%
,而清洁能源(如天然气、核能、水电等)仅占比
25.5%
,这离实现
“
双碳
”
目标还有一定距离。
由于氢气的燃烧热值高,约为天然气的
3
倍,且燃烧后不产生碳排放,因此氢气被认为是一种极具潜力的新型绿色能源。在过去数十年的发展历程中,已开发出了多种类型的储氢材料,但市场上大部分氢气产能仍严重依赖甲烷重整、烷烃脱氢等化石燃料制氢工艺,使得制氢环节不可避免地产生碳排放,造成氢能
“
越发展,越污染
”
的窘境。另外,电解水作为最理想的制氢方式之一,该过程的产物中只含有氢气与氧气,但电解成本始终居高不下,难以得到大规模普及
[2]
。
氨作为一种工艺成熟、成本低廉的非碳基储氢材料,在
-33℃/0.1 MPa
的条件下就能以液态形式进行储存与运输,可以有效突破氢能的发展瓶颈,具有极大的研究价值。另外,目前在合成氨领域的研究已开始由传统的
haber-bosch
工艺逐步转向光
/
电催化固氮,在降低生产成本的同时,还可避免使用工业副产氢作为原料,实现真正意义上的零碳制氢。除了用作氢载体,氨还可以直接以燃料的形式进行利用,在这方面的研究也越来越多,并且在工业上已经取得了一定的突破。本文中从氨裂解制氢、直接燃烧、燃料电池等
方面对氨能展开了系统的综述。
1904
年,
Perman
等
[3]
发表了第一篇关于氨热裂解反应的报道,他们发现在
1 100℃
以上的高温环境中
氨近乎完全裂解为氢气和氮气。早期对氨裂解反应的研究主要是为了促进合成氨工业的发展,但随着人们
对储氢材料的开发,氨裂解反应逐渐成为研究热点。氨裂解反应方程式如(
1
)所示。
2NH3⇌ N2 + 3H2,∆H= + 92.4 kJ/mol (1)
1.1
氨裂解催化剂
氨裂解与合成氨为互逆反应,合成氨催化剂在理论上也适用于氨裂解过程,且这一推论已得到广泛证实。
Ganley
等
[4]
对单金属催化剂进行了系统研究,发现在氨裂解反应中不同金属催化剂的活性排序为
Ru
>
Ni
>
Rh
>
Co
>
Ir
>
Fe
>
Pt
>
Cr
>
Pd
>
Cu
>>
Te
、
Se
、
Pb
,但即使是活性最高的
Ru
基催化剂,在低温下仍远未达到反应的热力学平衡。除了传统的单金属
/
合金类催化剂,近几年氮
/
碳化物、金属酰胺及酰亚胺等材料也展现出优异的氨裂解催化性能
[5]
。
Huo
等
[6]
利用
SBA-15
的空间限域效应,将
Mo2N
负载到
SBA-15/rGO
复合载体上,得到高度分散的催化剂,氨裂解速率达到
30.58 mmol/(g·min)
,性能可与
Ru
基催化剂相媲美。中科院大连化物所陈萍团队研究了
BaNH
、
CaNH
和
Mg3N2
在氨裂解反应中与
Co
的协同作用,发现在金属
Co
和
BaNH
相的界面处形成了
[Co-N-Ba]
中间物质,从而促进了氨气的裂解
[7]
。各类氨裂解催化剂的制氢性能如图
1[8]
所示。

1.2
氨裂解反应器
氨裂解反应是一个结构敏感的体积增大过程。因此,设计一个合适的反应器可以有效提高低温下氨的裂解效率,同时将产生的氢气转移,促进氨裂解反应正向移动。
Badescu
等
[9]
采用一维模型,研究了填充床反应器的最优化设计方案,发现通过改变反应器的形状或沿轴向控制催化剂颗粒的大小可以提高氨裂解催化性能。
Itoh
等
[10]
开发了一种高效管壁催化膜反应器,该反应器主要由管壁催化剂和钯膜管组成,氨在催化剂表面裂解后,产生的氢气经过钯膜分离提纯,在
375℃
下实现了近
100%
的氨转化率。
Badakhsh
等
[11]
首次提出了通过焦耳加热机制分解氨的紧凑型催化泡沫反应器,该反应器具有体积小、效率高和功率密度大等优点,与外部加热相比,使用焦耳加热机制后反应器的比活性提高了
10
倍。
1.3
待突破的关键技术
尽管利用氨作为储氢载体可以解决氢气储运难度大、成本高等行业痛点问题,但目前该方式也存在许
多不容忽视的制约因素:①氨裂解反应所需温度较高,远未达到低温下的热力学平衡,能量损耗大且不利于分布式应用;②催化剂的研发很难脱离合成氨催化剂范畴,所使用的非贵金属普遍存在活性不足等问题,而贵金属催化剂成本高,高温下易汽化,造成活性组分损失;③高温裂解过程中产生的
H2
会使高分散的活性中心发生迁移团聚,催化活性迅速降低。因此,开发温和条件下的高效氨裂解催化剂引起了学者们的
广泛兴趣。
氨的储能特性与甲烷类似:甲烷通过
4
个
C-H
键的断裂重组来释放能量,氨拥有
3
个键能相近的
N-H
键。如方程式(
2
)、(
3
)所示,二者的关键区别在于甲烷燃烧会产生碳排放,而氨燃烧后的理想产物为对
环境无害的氮气,且氮气可回收作为合成氨的原料,形成一个氮循环过程。因此,氨可能会成为未来化石燃料的替代能源之一。
CH4 + 2O2⟶CO2 + 2H2O,∆H= -889.6 kJ/mol (
2
)
4NH3 + 3O2
⟶
2N2 + 6H2O
,
∆
H
= -1268 kJ/mol
(
3
)
2.1
氨
-
氢混燃
1965
年,
Samuelsen
等
[12]
研究了火花式发动机中氨
-
空气火焰的火焰传播速率,发现氨的火焰传播速率要慢于异辛烷,维持稳定燃烧状态较为困难,这可能是氨的燃点较高导致的。
Han
等
[13]
测量了氨
-
氢
-
空气火焰的层流燃烧速度,发现在
0.7~1.6
的宽当量比范围内氢气对氨火焰均具有增强作用。此外,
He
等
[14]
在同一个发动机系统中对不同燃料的燃烧情况进行分析,其中,氨
-
氢燃烧的大部分特性与碳氢燃料相似,只是热值相对较低。
Comotii
等
[15]
基于氨的储氢特性,将装有钌基催化剂的氨裂解反应器与发动机耦合,通过裂解产生的氢进行助燃,成功实现了氨的稳定燃烧,且热效率与汽油发动机相当。尽管氢的添加可以显著提升氨燃料的燃烧效率,但也存在着一些现实问题,如氮氧化物排放等。例如,
Khateeb
等
[16]
在涡流燃烧器中证实了掺氢量与火焰稳定性正相关,但当氢的体积分数增加到
20%
时,尾气中
NO
x
的体积分数达
750×10-6
。因此,当选用氢
/
氨比较高的混合气体作为燃料时,可能需要在尾气处理部分安装烟气脱硝(
SCR
)装置,以利用燃烧残余氨除去
NO
x
。
2.2
氨
-
甲烷混燃
天然气在三大化石能源中相对最为清洁环保,目前国外针对甲烷掺氨混燃做了大量的研究工作,以进一步降低天然气燃烧的碳排放。
2016
年,
Valera-Medina
等
[17]
在旋流喷射装置中进行了氨
-
甲烷混合物燃烧试验,发现
2
种气体分子的混合燃烧过程非常复杂,火焰的稳定性与尾气中
CO
浓度直接关联,且富燃条件下的试验结果更好。
Ji
等
[18]
在钝体旋流燃烧器上进行了
3
种甲烷组分
[
x
(CH4)=0
,
0.5
,
1]
的无侧限贫燃预混氨
-
甲烷
-
空气火焰研究,当进气流速大于
5 m/s
时,氨
-
空气混合气无法被点燃,而添加
50%
甲烷后,层流火焰速度较当量比
φ
=0.8
的氨
-
空气火焰提高了
2
倍,且火焰更加稳定。
Ariemma
等
[19]
考察了不同氨
/
甲烷比下燃料气的燃烧特性,发现相比纯氨,混合燃气在工作温度与等效比方面具有更高的稳定运行范围,但
NO
x
排放量也相应增加,并强烈依赖于
φ
值。如图
2
所示,
Filipe
等
[20]
利用现有的燃气轮机对氨
-
甲烷混合气燃烧产物进行了分析,发现在相同条件下,只使用氨时产生的
NO
x
最少,但残余氨体积分数超过
1500×10-6
,当适当掺入甲烷后,尽管会使尾气中
NO
x
排放量有所增加,但残余氨的体积分数可大幅降低到
30×10-6
以下。

2.3
工业氨燃烧技术
自从氢能的工业化发展到达瓶颈以来,世界各国开始对氨燃料的规模应用进行开发。日本
AIST
公司与东北大学正进行
50 kW
级微型燃气轮机的氨直燃试验,目前已实现了氨的完全转化以及尾气中
NO
x
的抑制。丰田等公司利用
300 kW
级小型燃气轮机成功完成了
100%
氨稳定燃烧试验
[21]
。
IHI
与东北大学等机构在
2 000 kW
级燃气轮机中完成了氨
/
甲烷混燃比例从
20%
到
70%
的过渡试验,并计划下一步开发
100%
氨专烧技术
[22]
。近期,国家能源集团在氨掺煤领域开展了
40 MW
级燃煤锅炉掺氨
35%
的中试,氨燃尽率达
99.99%
,实现了煤电行业的技术突破,也证明氨具有替代煤粉燃烧发电的潜力
[23]
。
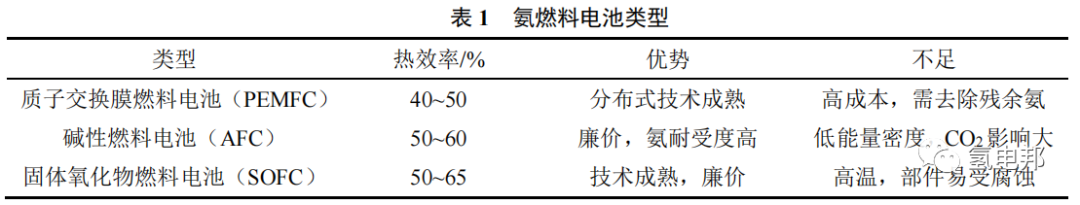
相较于裂解制氢与直接燃烧,燃料电池的优势是可以更大限度地利用氨分子中的化学能,整体效率较高。氨燃料电池可以根据不同的类型进行分类,如表
1
所示。
3.1
质子交换膜燃料电池
(
PEMFC
)
PEMFC
是一种通过氧化还原反应将化学能转化为电能的装置,具有高效率、高功率密度和环保等多项优点,并在过去
20
多年里取得了长足进步。目前对
PEMFC
的研究大多集中在氢能领域,但其对氢气的纯度有严格的要求。研究表明,
PEMFC
阳极进料中的痕量
NH3
会导致相当大的性能损失,主要原因是
NH4 +
离子置换
H+
导致
Nafion®
膜电导率降低,且
NH3
的存在会使得膜发生不可逆的降解
[24]
。
2019
年,国际标准化组织针对
PEMFC
提出了低至
0.1×10-6
的
NH3
体积分数阀值,因此,当氨被用作
PEMFC
的燃料源时,通常需要先分解,然后进行分离和纯化,以除去未转化的氨和氮,未转化的氨可以被酸性沸石和树脂有效吸收,而氮气与氢气的分离膜则采用膜分离技术
[25]
。
Cha
等
[26]
制造了由氨裂解器、吸附塔和聚合物电解质膜燃料电池组成的千瓦级发电系统,该发电系统可成功使无人机飞行
2 h
。尽管分离和纯化过程不可避免地会产生大量成本,但氨燃料
PEMFC
仍具有吸引力。
3.2
碱性燃料电池
(
AFC
)
AFC
是第一种投入实际应用且能够提供强大动力的燃料电池,具有非常高的电气效率,可以内置到分布式发电厂中,这些优势使得
AFC
系统的开发逐渐成为热点话题。
2008
年,
Ganley[27]
以
KOH-NaOH
低共熔混合物作为电解质,在
200~450℃
工作温度下进行了氨燃料电池的性能测试,
450℃
时能产生大约
40mW/cm2
的功率。不同工作温度下的极化特性表明,该燃料电池性能受到欧姆电势损失的影响。为了解决电池的耐久性问题,
Lan
等
[28]
对
AFC
损耗机理进行了深入研究,发现空气中的
CO2
与氢氧化物电解质反应后会形成碳酸盐沉淀,造成电池中毒,而在新的碱性膜燃料电池(
AMFCs
)系统中,虽然碱性膜仍能与
CO2
反应生成
CO3 2-
,导致
OH-
的电导率降低,但不会形成沉淀,避免了传统
AFC
易中毒
的问题。
3.3
固体氧化物燃料电池
(
SOFC
)

SOFC
因燃料灵活性和高效率而成为燃料发电的理想选择之一。单独应用
SOFC
时热效率最大在
50%
左右,目前大多技术都是将
SOFC
与底部热循环相结合(如图























