素有“红颜杀手”之称的乳腺癌,确实时刻威胁着女性健康。而乳腺癌久攻不下的现状也成为众科研者心中驱之不散的阴霾,但庆幸的是,在科研者孜孜不断的努力下,乳腺癌似乎初露败绩,其相关研究也进入了一个崭新的阶段。本文则盘点了近期乳腺癌领域中的亮点研究,让大家一睹为快!
1. Nat Com:脂肪细胞助纣为虐,促进乳腺癌生长
目前已有研究证实,脂肪细胞与乳腺内部癌细胞确实存在着千丝万缕的关系。为了研究乳腺癌细胞与脂肪细胞的相互作用机制,台湾研究者提出脂肪细胞分泌的β-羟基丁酸对乳腺癌细胞的生长具有促进作用。
他们在将乳腺癌细胞与经过手术切除离体的脂肪细胞共培养后发现,脂肪细胞通过生成蛋白质MCT2将分泌的β-羟基丁酸转运至肿瘤细胞内,而后上调数个癌基因的表达,促进了人乳腺癌细胞的生长。
参考文献:Adipocytes promote malignant growth of breast tumours with monocarboxylate transporter 2 expression via β-hydroxybutyrate
2. Nature:乳腺细胞命运与雌激素信号息息相关
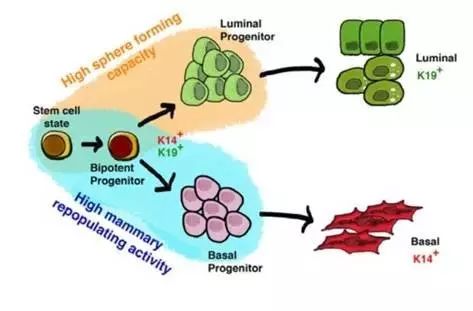
正常细胞命运的干扰是许多人类疾病产生的重要原因,其中也包括乳腺癌。乳腺上皮由分化的luminal上皮和基底肌上皮组成,同时也包括未分化的干细胞以及更加原始的细胞。
乳腺癌细胞起源于上皮细胞,但是其分化变异的过程仍未能得到明确的揭示。瑞典Friedrich Miescher研究所的研究者通过基于共聚焦影像的高含量短发夹RNA扫描发现,Hippo通路的组成部分——肿瘤抑制激酶LATS1和LATS2的缺失可推动了乳腺细胞luminal表现型的产生,进而增加了大部分乳腺癌起源细胞的数量。
而这正是由于Hippo通路和雌激素受体 (ER-α) 信号相互影响所致。雌激素信号在绝大部分人类组织中具有重要作用,因此该研究除了揭示乳腺细胞的生长分化过程,也提示了通过对Hippo通路的组织特异性缺失效应的检测,可揭示出更多组织中细胞分化与命运的变化机制。
参考文献:The Hippo kinases LATS1 and 2 control human breast cell fate via crosstalk with ERα
3. Nature:TMP195激发巨噬细胞的抗癌潜能
TMP195是一种重要的选择性脱乙酰化酶抑制剂,体外实验证实了其可以影响人类单核细胞对集落刺激因子CSF-1和CSF-2的反应性。
本文研究通过建立巨噬细胞依赖性的原位小鼠乳腺癌模型,验证了TMP195可改变肿瘤内环境,并调控巨噬细胞表型,减少了肿瘤体积和肺转移的几率。
TMP195可诱导具有高度噬菌作用和刺激作用的巨噬细胞分化和聚集,并能够与化疗或T细胞检查点阻断疗法相联合,产生更加持久的肿瘤抑制作用。这些都提示了巨噬细胞的抗肿瘤潜能,在增加抗癌疗效中可能起到重要的作用。
参考文献:Class IIa HDAC inhibition reduces breast tumours and metastases through anti-tumour macrophages
4. Science:乳腺癌中异常表达LncRNA的综合筛查
比利时癌症胚胎学实验室的研究者,对乳腺癌中的lncRNA生物学功能进行了大范围、综合性的筛选和分析后发现了210余种异常表达的且与临床预后相关的LncRNA。
同时,他们在对乳腺癌的亚型上进行相关分析后发现,luminal A亚型的乳腺癌特异性LncRNA与磷脂酰肌醇3-激酶、纤维母细胞生长因子(FGF)和转化生长因子β(TGF-β)三种通路的激活有关,而基底样亚型的乳腺癌特异性LncRNA,与表皮生长因子受体(EGFR)依赖性通路和上皮-间叶转化(EMT)的激活有关。
最后他们确定了一种与乳腺癌肿瘤细胞增殖、转移和细胞骨架相关的新型lncRNA-CYTOR,这为未来的lncRNA作为诊断及治疗标志物的应用打下了坚实的研究基础,并推动了乳腺癌中LncRNA相关作用机制的研究。
参考文献:Portraying breast cancers with long noncoding RNAs
5. Sci Trans Med:抑制mTOR/4E-BP通路可靶向治疗PIK3CA沉默态乳腺癌
在乳腺癌的治疗选择上,有效诱导肿瘤细胞的凋亡,往往能够在实体瘤患者中产生稳定持久的临床疗效。
美国杜克大学的研究者通过药理学筛查以及运用细胞学和动物模型的研究方法,证实了对BCL-XL和mTOR/4E-BP轴进行联合抑制,可在PIK3CA沉默的乳腺癌中诱导产生具有选择性和协同性的肿瘤细胞凋亡。这提示了具有PIK3CA沉默状态的乳腺癌,可从BCL-XL和mTOR/4E-BP(介导MCL-1转录)轴的抑制治疗中而获益。
此外,这项研究对于三阴性乳腺癌(TNBC)的治疗方面意义重大。TNBC做为一类PIK3CA沉默状态的乳腺癌,一直缺乏有效的治疗手段。而通过对BCL-XL和mTOR/4E-BP轴的抑制,不仅能抑制肿瘤的生长,还能增强TNBC对标准化学治疗的敏感性。
近来有研究证实了乳腺癌中一线治疗(包括内分泌治疗)耐药的乳腺癌通常伴有PIK3CA的沉默,提示了BCL-XL和mTOR/4E-BP轴的抑制将对于TNBC耐药治疗具有重要的作用。
参考文献:PIK3CA mutations enable targeting of a breast tumor dependency through mTOR-mediated MCL-1 translation
6. Cell:三阴性乳腺癌的CDK7依赖性转录成瘾性
三阴性乳腺癌(TNBC)具有高度侵袭性以及极其复杂的基因特性和转录机制。Yubao Wang等研究者发现TNBC对一系列连续性关键基因具有依赖性,随后也证实了TNBC对细胞周期蛋白依赖性激酶——CDK7也具有特异性依赖作用。
研究者在对CDK7进行抑制后,发现那些可被称之为“阿喀琉斯之踵”的关键基因对于CDK7的抑制十分敏感,被“直中要害”的TNBC细胞随即发生了凋亡性细胞死亡。
因此,基于CDK7可影响TNBC对一系列关键基因的转录成瘾,则抑制CDK7可成为TNBC的有效治疗手段之一。
参考文献:CDK7-Dependent Transcriptional Addiction in Triple-Negative Breast Cancer
7. Oncogene:“饥饿”疗法有望治愈难治性乳腺癌
肿瘤细胞的生长代谢需要特殊的环境因素支持,而不同类型的肿瘤,其“偏好”的营养成分也不尽相同。
一直以来,科学家们尝试通过研究肿瘤细胞的营养需求来开拓肿瘤治疗的新途径。去年11月,杜克大学研究者在对三阴性乳腺癌(TNBC)进行的营养剥夺试验中,发现TNBC对胱氨酸具有强烈依赖性,确立了胱氨酸作为TNBC肿瘤细胞生长的能量供给者的身份。
在对细胞进行基因分析后,发现这种依赖性的产生,可能是由上皮-间质转化过程(EMT)而触发,这也强调了EMT作为癌症进展过程中转折点的重要作用。那么通过寻找能够阻断胱氨酸的途径,有望大大增强该难治性乳腺癌治疗的有效性。
参考文献:Cystine addiction of triple-negative breast cancer associated with EMT augmented death signaling
8. Science Signal:新靶点让失控的乳腺癌转移“刹闸”
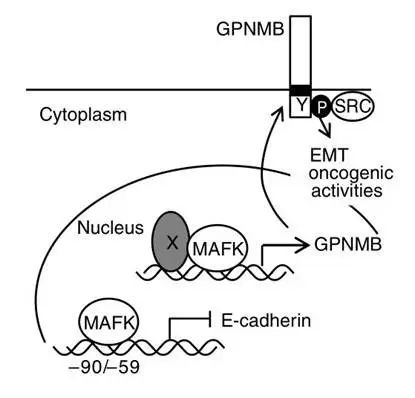
为了延缓三阴性乳腺癌的进展,控制癌症转移过程,日本筑波市大学的研究者分析了三阴性乳腺癌患者的肿瘤组织,发现较低的预后与编码转录因子MAFK的基因过表达有关,且在抑制MAFK-GPNMB通路后有效减低肿瘤的迁移和肺转移的发生率。
现已知MAFK-GPNMB通路与TGF-β通路和激酶SRC相关通路关。但相较于前者,后两种通路较难有效并安全地通过靶向作用抑制,该研究提示了可通过抑制MAFK-GPNMB通路来延缓TNBC肿瘤进展。
参考文献:The transcription factor MAFK induces EMT and malignant progression of triple-negative breast cancer cells through its target GPNMB













