正文
2025年3月2日上午,
天辰生物
LP-003的CSU慢性荨麻疹II期临床期中分析数据在美国过敏、哮喘和自免学会(AAAAI)年会上首次公开。该二期临床试验设计方案如下。

LP-003荨麻疹II 期(NCT:06228560/CTR20233300)的临床设计为
与奥马珠头对头的随机双盲试验。
期中分析结果显示(n=151例):
LP-003组的UAS7从基线到第12周的变化显著优于奥马珠组和安慰剂组,且呈剂量依赖效应。其高剂量组(200mgQ4W组)与奥马珠组相比,P=0.0501 (在每组统计例数n≈30的情况下)。

在第二个主要疗效指标中:在第12周,奥马珠组有约40%的受试者的荨麻疹症状完全缓解(即UAS7=0),这一数据与奥马珠的历史数据匹配,
同时LP-003治疗组受试者的荨麻疹症状完全缓解的比例(即% of patient with UAS7=0)显著高于奥马珠组和安慰剂组,且呈剂量效应。

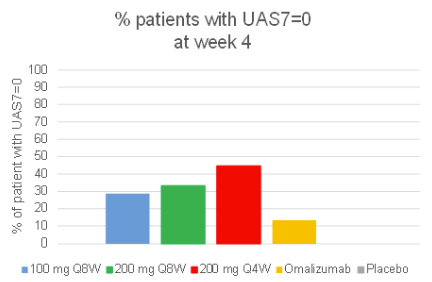
LP-003还展现了快速起效的作用
在给药4周后,LP-003治疗组受试者的荨麻疹症状完全缓解的比例(即%of patient with UAS7=0)显著高于奥马珠组(30%~40% vs
~
10%),且呈剂量效应。
LP-003也表现出了良好的安全性,在不良事件发生率方面,LP-003组与安慰剂组相似。
LP-003 展示出比竞品更好的临床结果
LP-003和Ligelizumab (诺华) 与anti-C-Kit Ab (Celldex的Barzolvolimab)的临床结果相比:
-
Ligelizumab(诺华)的II 期临床试验结果中,其主要临床终点为受试者的荨麻疹症状完全缓解的比例(即% of patient with UAS7=0),在第12周,Ligelizumab 组与奥马珠组的受试者的荨麻疹症状完全缓解的比例分别为~40% vs~26%(即Ligelizumab 优于奥马珠组约~14%);
-
在LP-003的II 期临床试验中,200 mg Q4W组和奥马珠组的受试者的荨麻疹症状完全缓解的比例分别为~60% vs~40%(即优于奥马珠组约~20%),且奥马珠组在第12周的% of UAS7=0为~40%与历史数据较为接近(包括Ligelizumab的III 期注册临床研究)
-
Celldex 的anti-C-Kit Ab (Barzolvolimab)的II期临床结果显示,其UAS7从基线到第12周的变化为~-23.84,由于其未设立奥马珠的阳性对照组,因此仅与LP-003的II期临床的UAS7从基线到第12周的变化的绝对值(200mgQ4W组~-25)进行比较。考虑到anti-C-Kit 抗体的不良反应以及发生率(头发颜色变化,以及皮肤颜色变化,且均>10%),
LP-003在药效和不良反应均优于Barzolvolimab
(anti-C-Kit Ab),且为目前荨麻疹临床阶段的best-in-class的候选分子。
同时作者也注意到天辰生物在LP-003的半衰期可达45-76天,而奥马珠单抗约24-26天。
天辰生物正在国内开展LP-003每3个月给药一次(Q12W)用于哮喘的II期临床试验(CTR20243191)。

慢性荨麻疹虽然不致命,但对于生活质量影响巨大,约有五分之一的患者因为这种疾病不得不一度停止工作,同时60%的患者会经历抑郁、焦虑等精神健康的困扰。

中国慢性荨麻疹患者的数量远超美国、欧洲,据估计目前有510万患者正在接受治疗,其中10万患者接受生物制剂的治疗,同时还有200万患者病情没有得到控制,存在巨大的未满足临床需求。
慢性荨麻疹不但最大的患者人群在中国,接受生物制剂治疗人数最多的国家仍然是中国!

食物过敏在美国有着巨大的市场潜力(>$100亿美金),根据罗氏的数据:美国共有约~1700万食物过敏的患者 (Diagnosed prevalence):其中约~350万为儿童和青少年(1-17岁),约~1350万为成人(18+岁) ,奥马珠单抗为FDA首个且唯一批准的治疗食物过敏的药物,根据Roche季报数据,
奥马珠单抗在食物过敏中的临床应用呈现迅速增长,显示出巨大的市场潜力。

总结
众所周知,孙乃超博士既是天辰生物的联合创始人,同时也是奥马珠单抗的主要发明人和Tanox公司的联合创始人。Tanox是华人生物制药领域的先行者和开拓者,创造过多个第一和唯一:成功开发了第一也是唯一上市的抗IgE抗体奥马珠单抗,华人开发的第一个年销售金额超过30亿美元的抗体药,第一也是唯一被Genentech公司收购的企业。
期待孙乃超博士和天辰生物继续在华人生物领域创造更多的佳绩,引领后人们乘风破浪,披荆斩棘。




