由于高血糖环境,糖尿病伤口常处于长期炎症状态,导致免疫反应减弱、血管生成受阻、氧化应激增加,从而显著干扰正常愈合过程。传统治疗方法(如组织清创、常规敷料和控制感染)虽然在一定程度上有效,但存在愈合速度慢、感染风险高和伤口复发率高等局限性。
因此,开发一种能够整合多种治疗功能、协同促进伤口愈合的创新策略成为迫切需求。

鉴于此,
西安交通大学孙祺团队
设计了一种具有协同光热疗法、电刺激和抗菌作用的自供电酪蛋白水凝胶电子敷料(
SM@PP/ZIF-8
),用于慢性伤口管理(图1)。
相关研究成果以
“A Self-Powered Casein Hydrogel E-Dressing with Synergistic Photothermal Therapy, Electrical Stimulation, and Antibacterial Effects for Chronic Wound Management”
为题发表在
《Acta Biomaterialia》上。
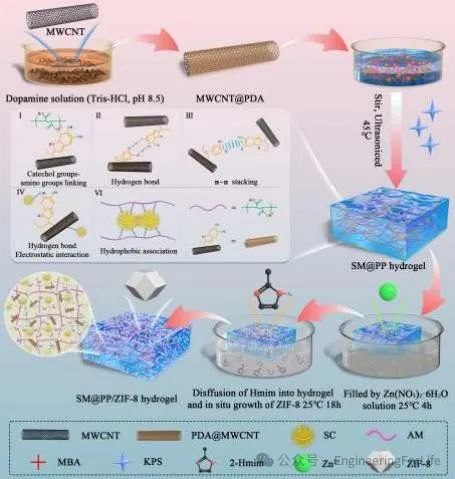
图1 SM@PP/ZIF-8水凝胶的制备工艺及形成机理
1.
SM@PP/ZIF-8水凝胶的合成与表征
通过自由基聚合反应将酪蛋白酸钠(SC)、多壁碳纳米管-聚多巴胺(MWCNT@PDA)和聚丙烯酰胺(PAM)形成双网络结构的SM@PP水凝胶,并通过原位生长的方式引入金属-有机框架ZIF-8。该水凝胶整合了光热、光动力抗菌和电刺激功能,其中MWCNT@PDA提供高效的光热转换能力,ZIF-8实现抗菌剂Zn
2+
的光热调控释放,同时水凝胶作为摩擦电纳米发电机(TENG)的电极材料,提供非接触式电刺激。通过多种测试验证了ZIF-8在水凝胶中的成功合成和化学组成。扫描电镜(SEM)和能量色散X射线光谱(EDS)展示了水凝胶的多孔结构和ZIF-8的均匀分布。此外,实验表明该水凝胶具有高效的光热转换能力(效率达52.19%)、良好的柔韧性和延展性以及对多种基底具有优异的粘附力。
这些表征结果共同证明了SM@PP/ZIF-8水凝胶的多功能特性,为其在伤口愈合中的应用提供了结构和性能基础。
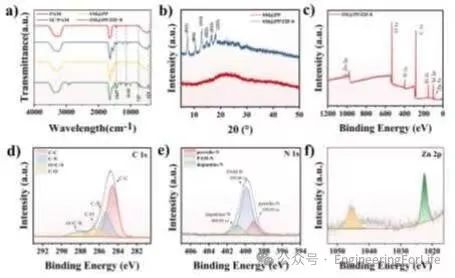
图2 SM@PP/ZIF-8水凝胶的表征
2.
SM@PP/ZIF-8水凝胶的形态
进一步通过SEM和EDS分析了SM@PP/ZIF-8水凝胶的表面和内部形貌。结果显示,ZIF-8成功在水凝胶表面生长,呈现出菱形十二面体结构,并且在水凝胶中均匀分布。此外,水凝胶内部具有相互连通的三维多孔结构,孔径较大且孔壁较薄,这可能是由于ZIF-8的引入和溶胀效应导致的。
这种多孔结构不仅提高了水凝胶的比表面积,还增强了其吸水性和机械性能,为伤口愈合提供了良好的物理基础。

图3 不同体系水凝胶表面的扫描电镜图像
3.
溶解度,机械和粘附性能
作者接下来评估了SM@PP/ZIF-8水凝胶的溶胀性能、机械性能和粘附性能。溶胀性能测试表明,该水凝胶具有较高的吸水能力,尤其是ZIF-8的加入进一步增强了其吸水性和多孔结构。机械性能测试显示,水凝胶具有良好的柔韧性和延展性,尽管加入ZIF-8后机械强度略有下降,但仍能满足伤口敷料的需求。粘附性能测试表明,水凝胶对多种基底(如皮肤、金属和塑料)具有优异的粘附力,这归因于PDA和酪蛋白中的功能基团与基底的多重相互作用。
这些特性共同表明SM@PP/ZIF-8水凝胶在伤口愈合中具有良好的适应性和保护性。
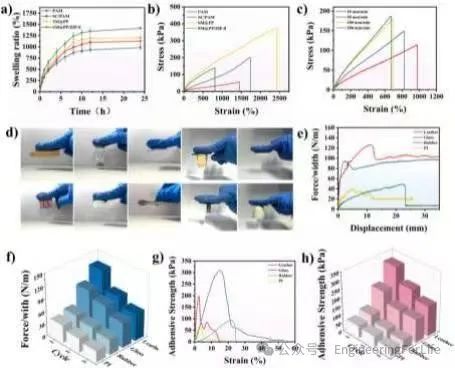
图
4 SM@PP/ZIF-8水凝胶的溶解度,机械和粘附性能
4.
协同光热/化学抗菌活性
作者同时探讨了SM@PP/ZIF-8水凝胶的光热性能和抗菌性能。水凝胶在808 nm近红外激光照射下表现出快速的光热升温能力,效率达52.19%,且具有良好的热稳定性。ZIF-8的加入实现了Zn
2+
的光热调控释放,避免了抗菌剂的过量释放,维持稳定的抗菌环境。抗菌测试表明,水凝胶对大肠杆菌和金黄色葡萄球菌的抗菌效率超过99%,尤其是结合光热和光动力离子释放的协同作用,显著增强了抗菌效果。
这些特性表明SM@PP/ZIF-8水凝胶在伤口抗菌治疗中具有显著优势。
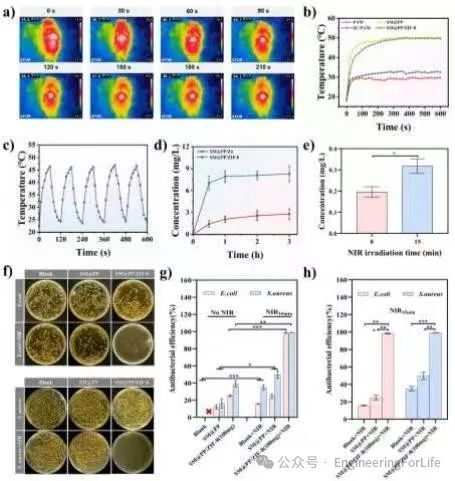
图
5
SM@PP/ZIF-8水凝胶的
协同光热和化学抗菌活性
5.
传感性能和人体运动监测
此外,作者探讨了SM@PP/ZIF-8水凝胶作为应变传感器的应用潜力。水凝胶传感器对1%到800%的应变范围均有响应,灵敏度因子达1.02,响应时间为397ms,展现出快速响应和高灵敏度。
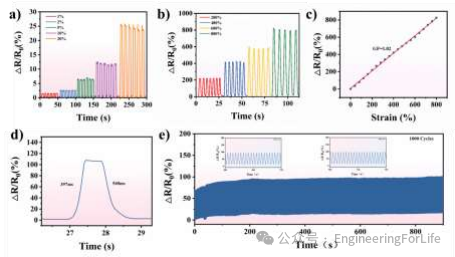
图
6
SM@PP/ZIF-8水凝胶应变传感器
的
传感性能测试
此外,水凝胶在1000次手指弯曲循环测试中表现出良好的耐久性。该传感器能够实时监测人体多种运动(如开口、手指轻敲、弯曲等),显示出高重复性和一致性,
表明其在医疗领域评估运动对伤口愈合影响方面的潜在应用价值。
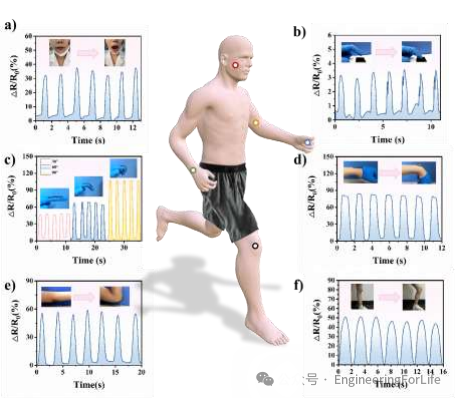
图7
使用SM@PP/ZIF-8作为表皮传感器附着在人体模型中来监测全身信号
6.
基于SM@PP/ZIF-8水凝胶的S-TENG工作原理及性能
电刺激疗法是一种成功的伤口愈合策略,它能够促进成纤维细胞、上皮细胞和其他细胞类型的迁移和增殖,还会改变生长因子的分泌,影响酶的活性。图7展示了SM@PP/ZIF-8水凝胶在单电极模式下产生电能的具体工作机理。
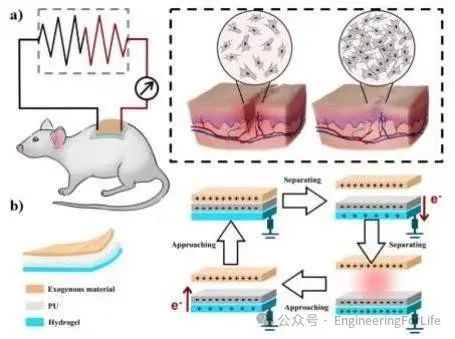
图
8
S-TENG结构及工作原理示意图
作者探讨了基于SM@PP/ZIF-8水凝胶的S-TENG的工作原理和性能。S-TENG通过接触起电和静电感应产生电能,具有单电极模式下的高效电输出能力。实验表明,SM@PP/ZIF-8-TENG的输出电压和电流优于SM@PP-TENG,尤其是与聚酰亚胺接触时,输出电压可达131 V,电流达100 nA。此外,S-TENG在不同压力、频率和距离下均能稳定输出电能,并在非接触模式下表现出良好的电输出能力,适用于复杂的伤口治疗场景。设备在1500次接触循环后仍保持稳定,证明了其机械和电学稳定性。这种自供能电刺激为慢性伤口愈合提供了新的治疗手段。
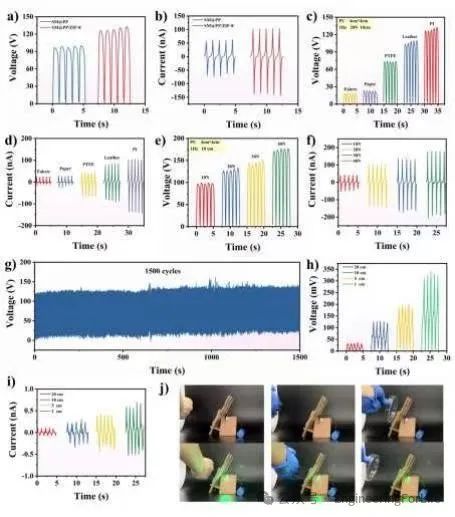
图
9
S-TE
NG的电输出性能测试
7.
体外生物相容性及促迁移效应
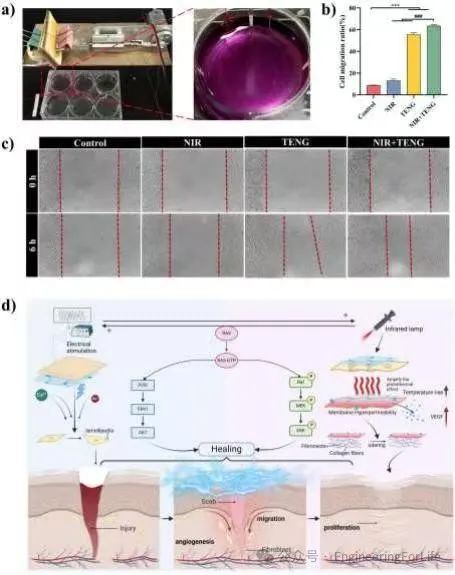
作者评估了SM@PP/ZIF-8水凝胶的生物相容性和对细胞迁移的促进作用。细胞毒性测试表明水凝胶提取物对小鼠成纤维细胞具有良好的生物相容性,细胞存活率超过90%。细胞划痕实验显示近红外光热治疗(NIR)和TENG电刺激均能显著提高细胞迁移率,其中NIR+TENG组合治疗效果最佳,6小时后迁移率达到63.3%。
这种协同效应归因于光热诱导的膜通透性增强和电刺激驱动的细胞骨架重组,表明SM@PP/ZIF-8水凝胶在促进伤口愈合方面具有显著优势。
图
10 SM@PP/ZIF-8水凝胶的体外生物相容性及促迁移功能
8.
慢性糖尿病伤口愈合可视化监测
皮肤是抵御外界刺激和有害物质的主要屏障。创伤后的再生和修复是一个复杂的现象,涉及多个因素的多因素相互作用。因此,作者通过链脲佐菌素(STZ)诱导的糖尿病大鼠模型评估了光热和电刺激疗法对慢性糖尿病伤口愈合的影响。实验分为四组:对照组、NIR组、TENG组和NIR+TENG组。结果显示,NIR+TENG组的治疗效果最佳,10天后残余伤口面积最小(约4.90%),
表明光热和电刺激的协同作用能显著加速伤口愈合。此外,治疗期间各组大鼠体重无显著变化,表明治疗的安全性和耐受性良好。
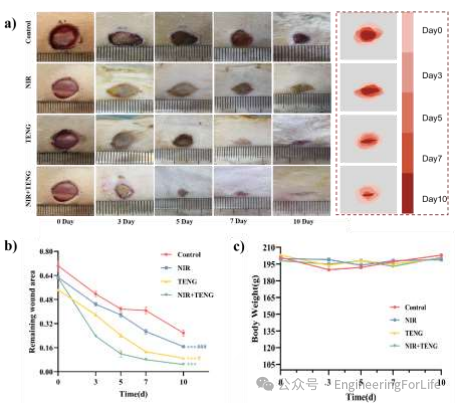
图11 光热治疗和电刺激对创面模型的影响
9.
TENG/NIR治疗伤口愈合的机制和生物标志物
光热疗法和电刺激疗法通过多种机制协同促进伤口愈合。光热疗法通过局部升温促进内皮细胞增殖和迁移,上调CD31表达,增强血管生成;电刺激通过激活PI3K/Akt和MAPK信号通路,促进内皮细胞活动并上调VEGF表达,进一步加速血管生成。同时,光热和电刺激协同作用有效抑制促炎因子IL-6和TNF-α的释放,减轻炎症反应,促进伤口从炎症阶段向增殖阶段转变。
这种协同机制显著提高了伤口部位的血液供应和营养输送,加速了整体修复过程,为慢性伤口愈合提供了高效的治疗手段。
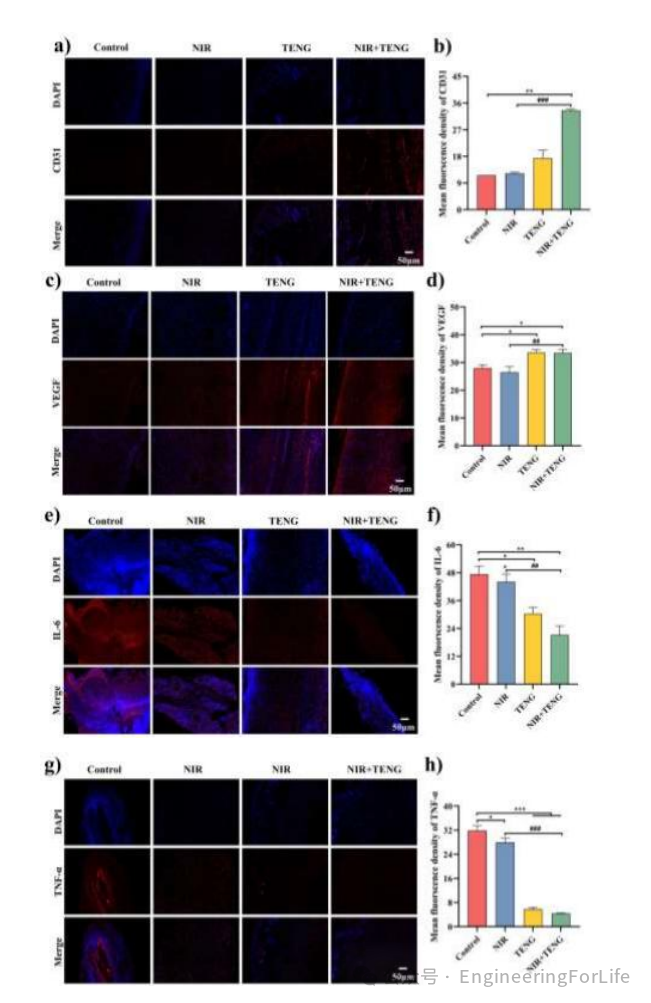
图12免疫荧光染色分析
10.
创面组织学分析
通过H&E染色和Masson染色对创面组织进行了组织学染色分析。结果显示,NIR+TENG组的胶原蛋白沉积量显著高于其他组,表明光热和电刺激的协同作用显著促进了组织修复和再生。H&E染色显示该组的毛囊和腺体再生更为显著,表明光热和电刺激通过促进细胞增殖、分化和生长因子分泌,加速了伤口愈合过程。
这些结果进一步证实了光热和电刺激疗法在慢性伤口治疗中的有效性和潜力。
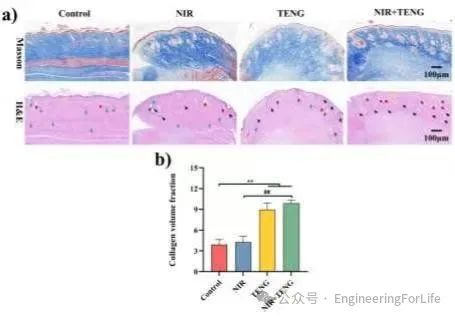
图13 创面的组织学染色
11.
全文小结
综上所述,本研究通过设计一种基于酪蛋白水凝胶的自供能电子敷料,结合光热疗法、光动力抗菌和电刺激功能,为慢性伤口管理提供一种高效、智能的解决方案,有助于推动伤口治疗领域的精准化和高效化发展。
参考资料:
https://doi.org/10.1016/j.actbio.2025.03.047
来源:
EngineeringForLife
声明:仅代表作者个人观点,用于研究用途,作者水平有限,如有不科学之处,请在下方留言指正!






