在医药领域,制药企业依靠药品的专利保护的排他权获得垄断市场。随着专利期限届满,仿制药进入市场,原研药厂依靠垄断的销售收入和利润出现显著的大幅下降。业内将这种现象其形象的比喻为“专利悬崖(Patent cliff )”。原研制药企业当然不会坐以待毙,面对“专利悬崖”,其通过构建“基础专利+次级专利”组合的方式,沿技术分支和产品开发时序进行布局,以累叠专利有效期,延长产品保护,拖延竞争对手的进入,维护垄断利润。我国制药产业创新驱动不足,企业大多以仿制药为主,对于国外制药巨头的布局策略,政府、企业都需要给予足够的重视。
「引言」
制药行业的研发具有投资大、风险高、周期长等特点,需要投入大量的金钱以及科研精力。如果没有专利制度的保护,发明人将无法收回高昂的成本,从而丧失研发的动力。对于制药行业中的企业来说,推出的新药能否确保长期盈利和收入成为关切。在许多行业,一旦产品失去专利的排他权保护,企业一般都会面临销售额的大幅下降和利润损失。在这一点,制药行业表现的有为明显,当专利权到期,随着仿制药厂商的进入,产品以较低的价格销售,原研企业产品的原有的定价难以为继。
业内将年销售额大于10亿美元的药物称为“重磅炸弹”(blockbuster),这些药物一般占据公司收入的一大部分。欧盟的一项调查表明,仿制药企业进入2年后,其报价仅为原研企业的40%。
「“专利悬崖”冲击显著且不可避免」
虽然专利药到期后,有益于降低公众的健康支出,提高社会福利,但是对于原研企业来说其不得不面对收入大幅下降的挑战。失去排他限制后,这些产品将对公司的业绩造成显著的负面影响,还将迫使原研药厂去寻找新的目标。医药企业价值链由研发驱动,对专利保护资产的依赖意味着制药企业必须能够不断重复研发的成功。
这种高度依赖研发投入的商业模式,风险无处不在。制药行业相较于其他行业具有独特的研发特征,其属于强研发驱动,高政策规则,产品复杂程度和质量要求越来越高。将一个“重磅炸弹”推出并得到市场的认可,一般花费超过10年时间,而专利的保护期限为20年。这种商业模式下,拥有“重磅炸弹”的制药企业每经过10-12年左右的时间,就会面临一次核心业务的调整。
即将到来的“专利悬崖”对公司收入带来巨大冲击,导致公司财务上的巨大缺口。近年来,一些“重磅炸弹”药物相继失去专利保护。辉瑞公司的立普妥曾是非常畅销的处方药,随着专利权2012年到期,其销售情况随之出现了大幅下降。
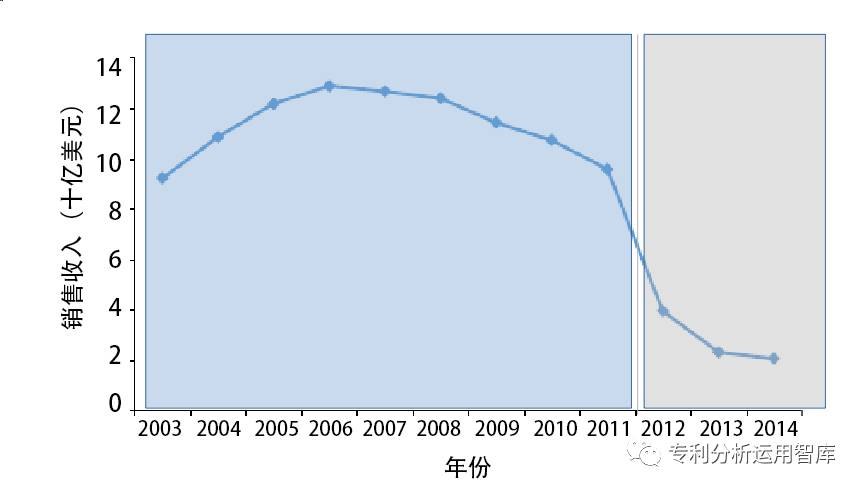
图1.辉瑞公司产品立普妥lipitor®2003-2014年销售收入(数据来源公司年报)
一般认为由专利保护到期给企业销售收入下降不可避免,只能通过一些预防手段进行延缓。例如美国国会在Hatch-Waxman法案中规定了药品专利期延长的制度。法案涉及美国新药审批程序中的专利链接制度规定了适当延长药品专利期限以弥补药品因注册审批期间而受到的经济损失。
美国对药品专利的延长可以有以下两种途径:一种是由美国专利商标局对于因专利审查延误的专利给予保护时间的补偿;另一种是针对因药品行政许可审批程序而耽搁时间的,由美国专利商标局审核确认后给予补偿,这种情况的补偿期一般为5年,最多不超过14年,专利保护补偿期从上市之日起计。
「造成“专利悬崖”的因素」
首先,原研制药企业的“专利悬崖”现象主要由仿制药企业的进入引起。仿制药厂的进入给药价带来实质的影响,使得市场从垄断转向基于价格的竞争。仿制药厂在研发上的投资远远低于原研药厂,使其能够将药价定到一个较低的水平。竞争的引入打破了产品和价格的垄断,造成原研企业销量和售价的双线调整,最终反应在销售业绩的快速下滑。
其次,近年来,原研企业研发产出持续下降。这一方面由于研发成本的增加,另一方面得归因于政府对于药品审批过程的延长,因此造成依赖研发驱动的制药企业产品线的萎缩。
第三,仿制药企业通过营销手段影响医务人员处方,来增加其市场占有率的行动更加积极,抢占了原研药厂的市场份额。
第四,公共政策制定者为了控制成本维系公共健康体系稳定、可持续,往往倾向于处方相对便宜的仿制药。
此外,随着对于人类疾病分子水平的认知和药物基因组学的研究导致个体化治疗的出现。个体化的治疗方案能够提高临床效果、增加病人的安全性,这些都是以往的“重磅炸弹”难以实现的。这种转变也许将彻底重构药物研发的结构和路径。
表1:2016年到期的重磅销售药物「数据来源于IMS
(2012)」
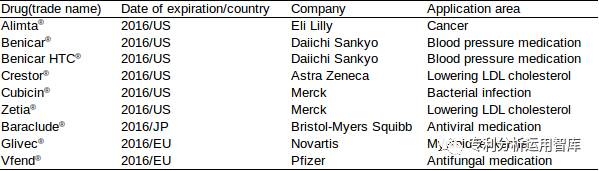
对于研发驱动的制药企业来说,如何确保现有产品线的收入,减缓仿制药企业进入市场的冲击变得日益重要,需要理性辩证的看待应对的策略。
「“专利悬崖”该如何应对」
总的来说,对于制药企业而言其面对“专利悬崖”可选择的策略大致可以分为四类:延长保护期进行防御、价格战差异化竞争、妥协共享市场和创新开拓新产品线。该如何进行策略选择,制药厂商需要根据目前的能力、机会和优先考虑的选项等因素相机抉择。
从四种策略的演进顺序来讲,首先应考虑如何延长专利的保护期,推迟“专利悬崖”的到来。本文将重点讨论如何基于专利布局来进行策略性防御。
防御策略的一个基本原则是寻求延长市场排他权的可能性。策略导向是延长专利保护,取得暂时的保护或者干预竞争者的产品周期。主要手段是构建专利簇或专利组合,以基础专利加次级专利的方式布局。基础专利保护药物活性组分及其制备,次级专利保护原始活性化合物的晶型、制剂、用途等,通过构建牢固的专利组合,以覆盖药物的各个方面。假设仿制药厂挑战基础专利的有效性,次级专利的保护也将有助原研厂维持其市场份额。
对于基础专利,化合物本身的保护也可考虑拆分成多个申请文件进行保护。例如,在一份申请中涵盖多种化合物,同时在另一份申请中只包含特定的一个化合物。如果发现异构体取得了预料不到的技术效果,尽量考虑通过单独的申请进行保护。药物合成方法的改进的技术方案可以在后续的申请文件中予以保护,不必一开始就在化合物的申请文件中公开,可以选择在产品周期的后续阶段进行布局。对于次级专利,可以针对基础专利技术方案的各种改进进行布局。
据统计,制药企业在基础专利到期日之前申请的次级专利与基础专利的比例大概为7:1。这种申请显然不是为了技术创新,而是为了将竞争对手排除在市场之外。因为对于仿制药厂商来说,次级专利增加了判断相关专利到期的难度,在进入相关市场时对于潜在的侵权行为有所顾忌。比如,仿制药厂很可能会发现在已经明确化合物专利已经过期后,想要以一种更为经济的方法生产该化合物或者使用其更为稳定的晶型时,又落入原研制药企业次级专利的保护范围内。
「举个栗子-雅培HIV治疗药物的专利布局策略」
由雅培(abbvie)原研推上市场的治疗HIV的药物ritonavir通过外围次级专利构建庞大的专利组合,在基础专利到期后成功拖延了竞争对手的进入。雅培共围绕lopinavir/ritonavir申请210件专利,将专利保护期至2028年,距基础专利到期之日后12年之久。
技术分布方面:
在210件专利或申请中,涉及活性组分的化合物专利有2件,分别为US5,541,206涉及ritonavir,该专利申请于1995年,于2015年到期;及涉及lopinavir活性组分基础专利US5,914,332于1996年申请,于2016年到期。
有81件(39%)相关专利涉及活性成分的组合物或制剂,活性组分的中间体,多晶型以及前药。其中60%涉及组合物和制剂,27%覆盖中间体,5%关于多晶型和无定型固体,另外有6件专利涉及前药。多晶型对药物的物理和药代动力学特征有影响,例如,药物的稳定性、溶解度、溶解速率、吸收和生物利用度等。
有68件(32%)相关专利涉及制备步骤和方法,包括制备与ritonavir、lopinavir类似结构的化合物、中间体以及制剂、组合物、多晶型的制备方法。
有31件(15%)相关专利针对HIV的制药用途。专利涉及ritonavir、lopinavir在治疗HIV感染或其他疾病的用途。其中US6,037,157(2016年到期)涉及改善ritonavir药物被CYP3A4系统代谢的方法。
有28件(13%)属于一般申请,这些专利申请涉及药物组合物、制剂以及固体口服制剂的一般制备方法。这些申请虽未明确提及ritonavir、lopinavir但对与仿制药厂来说仍是绊脚石。
专利时序方面:
雅培选择的后续专利申请多聚焦在多晶型、药物用途和制剂,特别是热稳定片剂。最终,在基础化合物专利到期后,雅培覆盖lopinavir、ritonavir的次级专利的保护期重叠至2028年,比基础专利到期时限晚12年(参见图2)。
其中,多晶型专利将ritonavir保护期延伸至2019年,将lopinavir保护期延伸至2021年。制剂相关申请涉及ritonavir、lopinavir/ritonavir的软胶囊,其在时间上有重叠,这些专利最迟于2020年到期。
US7,346,752和US8,025,899专利均涉及lopinavir/ritonavir热稳定片剂。这些专利涉及聚乙二醇及聚乙烯吡咯烷酮等水溶性聚合物辅料。类似的,专利申请US2007/0249692权利要求覆盖了以上两种聚合物辅料的组合。这些专利将在2025-2028年逐步到期。
而且这些专利组合保护范围还涵盖了对当前剂型的改进,雅培在保护新版的lopinavir、ritonavir药物的同时,也丰富了产品线。如果上述专利被写入橙皮书,这些不同的申请将能够延迟仿制药厂商的进入,从而延展当前市售制剂的专利保护期。
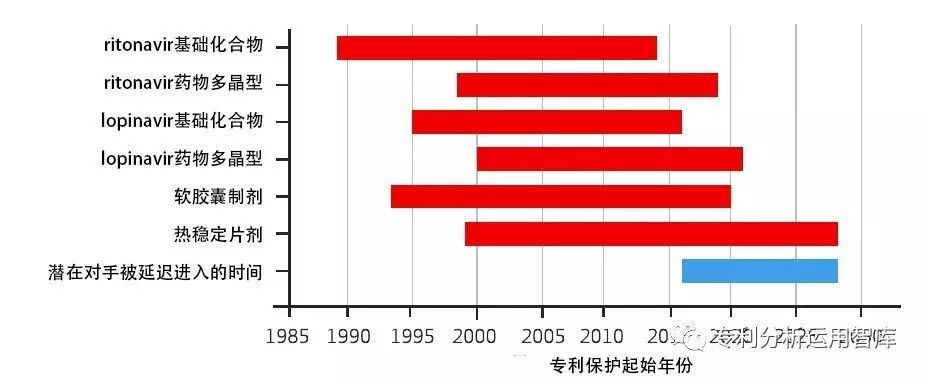
图2.雅培lopinavir/ritonavir产品专利生命周期管理
(数据来自Health Affairs 31, no.10 :2286-2294)
「我国制行业相关政策的思考」
专利制度在赋予专利权人垄断权的同时,也造成专利药品高昂的价格。原研药厂产品的保护的延长无疑会给依赖药品的消费者带来利益损害。这也体现了专利制度与公共健康权之间的矛盾。我国制药企业以仿制药厂商为主,国内企业与原研药厂的竞争往往处于劣势,在专利药品领域远低于全球平均水平。国内消费者面对高医疗费用的状况短期内还难以缓解。
如何应对?
短期来说,发展中国家应对药物多晶型及剂型改进的专利申请的创造性进行严格审查,对于显而易见性的判断标准应严格把握。在印度,如果请求保护对已知化合物的改进,则要求提供临床效果作为技术方案具备创造性的依据。
同时还应对专利有效性进行积极挑战,特别对于原研药厂的次级专利。从雅培的策略可以看出,很多专利申请仅仅是对原始技术方案的微小改进,比如辅料的组合或选择,国内制药企业应积极对专利有效性进行挑战或提交公众意见。
长期而言,加快建立我国的橙皮书制度,增加原研药厂专利透明度。而且不仅要列出直接相关授权专利,列出专利申请也十分必要。这对于亟待进入的仿制药企业来说就能清楚的知道潜在的障碍。
此外,应建立对列入橙皮书专利的有效性进行审核。比如加拿大卫生部专利药品和联络办公室从第三方收集上市药品的专利信息,其中包括对专利有效性等资质的核实,如果经办公室审查发现该专利不应被列入,则会将该专利从列表中删除。
「展望」
我国已是世界第一大原料药生产和出口国、第二大OTC药物市场、第三大医药市场,国内日益旺盛的需求完全可以成为国内医药行业发展的动力源泉。但从药品销售排名前列的品种看,国外一般都是专利药,而国内基本是中药注射剂以及专利过期的仿制药。
国内制药企业一方面需要持续进行技术改进,降低成本;另一方面则要加大投入开发高附加值的新产品。唯有依赖自主创新才能从根本上解决国内药价贵,企业利润低的悖论。
作者/单位:李瑞丰/国家知识产权局知识产权发展研究中心
注:本文节选自2017年第6期《电子知识产权》,作者李瑞丰、陈燕。(专利布局视角下药企应对“专利悬崖”策略研究及思考[J]. 电子知识产权,2017,(06):64-72. )
参考资料:
1.Tahir
Amin and Aaron S. Kesselheim, Secondary Patenting Of Branded
Pharmaceuticals: A Case Study Of How Patents On Two HIV Drugs Could
Be Extended For Decades,Health Affairs 31, no.10 :2286-2294
2.IMS (2012) The global use of medicines: outlook through 2016. https://www.imshealth.com/files/web/IMSH%20Institute/Reports/The%20Global%20Use%20of%20Medicines%20Outlook%20Through%202016/Medicines_Outlook_Through_2016_Report.pdf
图片:来自网络
编辑:李瑞丰
【往期精编】
-专利布局速递-

- 关于我们 -
专利分析和预警的领路人
专利导航理论和实务的开拓者
专注 | 专家 | 专栏
- 关注我们 -
订阅号:专利分析运用智库
微信号:patent-analysis
项目合作 | 专业咨询 | 成果发布 | 培训服务
联系方式:[email protected]







