依据体外诊断试剂注册管理办法(国家食品药品监督管理总局令第 5 号)“”第十二条 体外诊断试剂产品研制包括:主要原材料的选择、制备,产品生产工艺的确定,产品技术要求的拟订,产品稳定性研究,阳性判断值或者参考区间确定,产品分析性能评估,临床评价等相关工作。申请人或者备案人可以参考相关技术指导原则进行产品研制,也可以采用不同的实验方法或者技术手段,但应当说明其合理性”。
研究主要生产工艺之前,首先要先弄清楚试剂盒所采用的方法学原理。主要生产工艺研究内容要依据试剂所采用方法学而定。以酶联免疫法检测试剂为例,ELISA试剂主要组分的生产包括:酶标记物的制备及滴配过程(酶工作液浓度确定)、各种工作溶液的配制、包被酶标反应板、分装及包装等步骤;并通过产品的半成品检验和成品检验两个质控过程来保证其质量符合规定。
市场上流通的免疫学检测试剂盒(包括有抗原抗体反应的生化试剂)所采用的方法原理,可根据是否应用标记技术大体上分为凝集反应和免疫标记反应。(小编的研究主要集中在免疫检测方面,对分子和生化知之甚少,所以暂且只能以免疫学检测试剂举例;不过,个人认为大致的思路应该是相通的。)
凝集反应是指在一定浓度的电解质环境下,颗粒性抗原/抗体(如红细胞、细菌、包被的乳胶微粒等)和相应的抗体/抗原反应能够产生肉眼可见的凝集块。凝集反应根还可分为直接凝集、间接凝集和间接凝集抑制试验。此类反应的试剂盒主要有ABO血型试剂、菌凝试剂、血球试剂以及生化乳胶试剂。除了生化乳胶试剂外,其它试剂在市场上并不多见,多数已经逐渐被相应的免疫标记所替代。但是,传统而又经典的凝集反应试剂在一些特殊领域的应用,仍然发挥着不可替代的作用。小编在毕业之后从事体外诊断试剂行业,最早接触就是这一类方法学试剂(菌凝试剂、血球试剂(直接凝集、间接凝集、间接凝集抑制试验)、血型试剂如ABO等)。在2013版的6840 - 体外诊断试剂分类子目录的前几十项基本都是此类试剂。
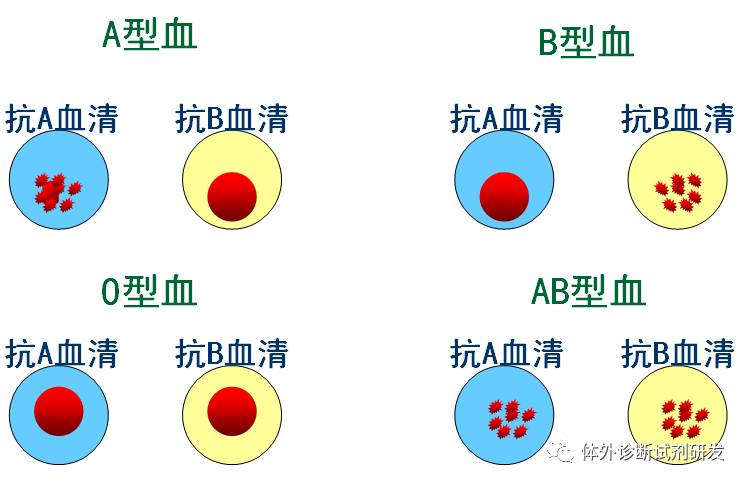
免疫标记技术是在已知抗体或抗原标记上易显示的物质,通过检测标记物来反映抗原抗体反应的情况,从而间接地测出被检抗原或抗体的存在与否或量的多少的一种生物技术。常用的标记物有荧光素、酶、放射性核素及胶体金等。免疫标记技术具有快速、定性或定量甚至定位的特点,是目前应用最广泛的免疫学检测技术。
一个试剂盒所包含的技术原理,从方法学的角度可以分解成3-4个部分:抗原抗体反应模式、分离模式、信号放大模式(有的试剂盒没有这一部分)、信号检测模式。
抗原抗体反应模式:即特异性反应的反应特征,不同试剂盒具体选择哪种免疫反应模式,一般取决于被检测标志物的类别(抗原或是抗体)及其分子大小。例如,我们常说的间接法、双抗体夹心法、双抗原夹心法、竞争法等等,就是以此为依据。当然,此部分特征的表述对于一些非免疫反应的生化试剂也是成立的,试剂中有效成分与被检标志物发生特征性反应。核酸试剂亦是如此。

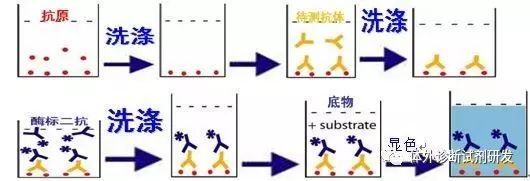
分离模式:即采取一定的方法保证特异性结合的分析物被保留,而未结合和无用的的反应物被清除。以双抗体夹心法ELISA试剂为例,第一次样本孵育和第二次加酶标记抗体孵育后的2次洗涤,均是为了让已经特异性集合的抗原抗体复合物与液相中未参与反应的抗体分离,确保最终酶催化显色底物的量与样本中标志物的量成比例。常用的分类方法有96孔板(ELISA使用的是透明的96孔板,板式发光使用的是白色或黑色的96孔板等)、磁颗粒/磁珠、纤维素膜(免疫层析)以及新兴的微流控芯片技术等等。
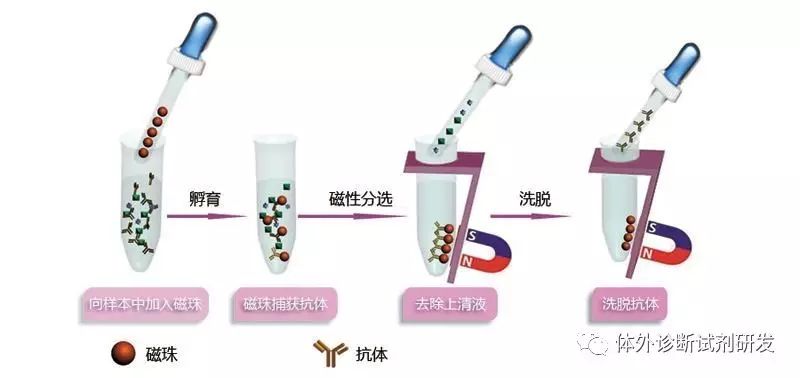
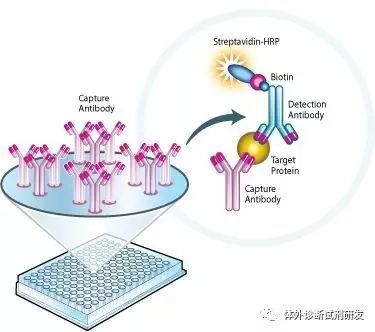
信号放大模式:主要是指应用生物素-亲和素/链霉素放大系统的检测试剂。当然,一些试剂中利用的酶促底物反应亦具有放大作用。
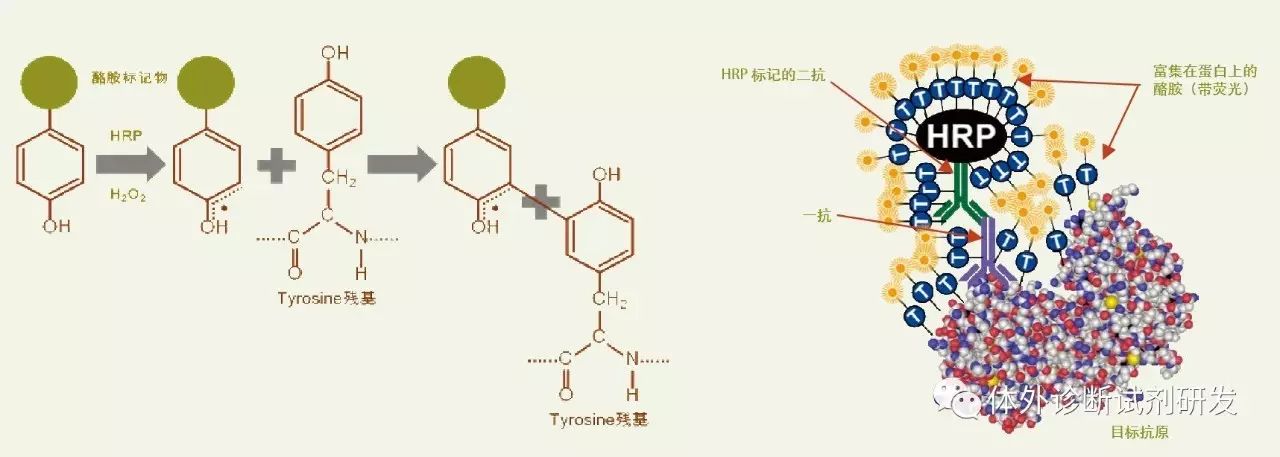
(酶促底物反应)
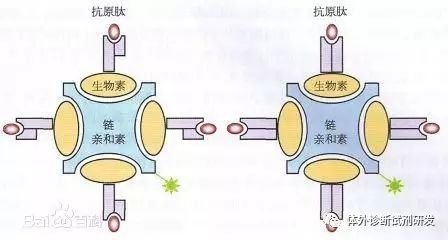
(生物素-亲和素 ——1)
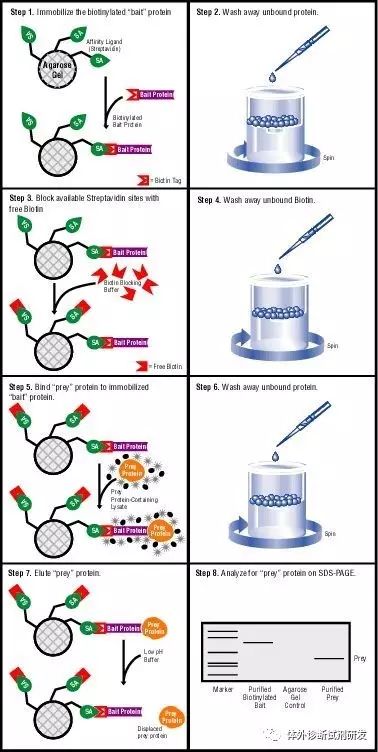
(生物素-亲和素 ——2)
信号检测模式:微量的抗原抗体反应,人的肉眼是无法直接看到,我们通过一定的标记技术,将微观的抗原抗体反应数量关系转化成分析化学中常用的检测方法,如光学检测、放射强度检测等。常用的标记物有荧光素、酶(与酶促发光/显色底物联用)、放射性同位素、胶体金等。试剂盒命名时括号中的方法学名称有很多就是依据这一部分而确定的,例如酶联免疫法、化学发光法、胶体金法、免疫透射比浊法等等。
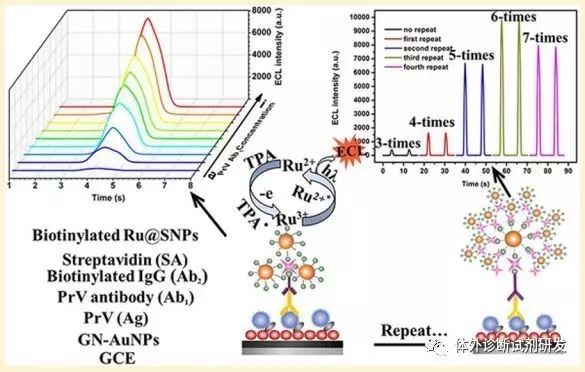
(电化学发光检测原理)
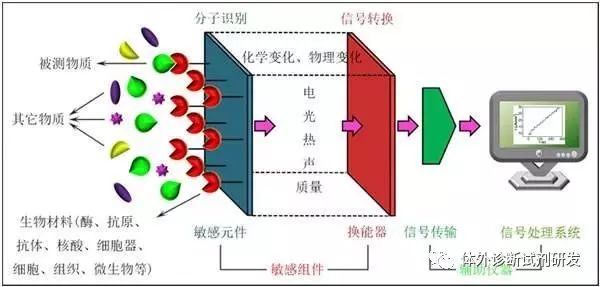
(生物传感器基本原理)
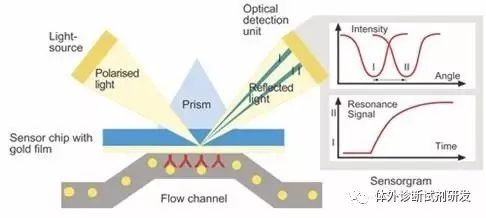
(微流控芯片检测原理 a)
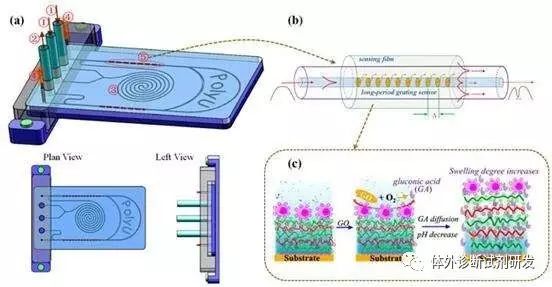
(微流控芯片检测原理 b)
在整个检测过程中,待检标志物是自变量。当初始包被抗体(捕获抗体)浓度、酶标记二抗浓度、显色底物浓度一定时,一定浓度范围内,样本中每个待检测标志物的数量与酶标记二抗的数量成比例,酶标记二抗的数量与其催化底物浓度成正比,被催化底物浓度与显色溶液吸光度成正比,通过多步转换,最终建立起待检标志物个数与反应体系终溶液吸光度的量值关系。
工艺反应体系研究就是通过生物学相关技术手段(例如生物化学、分析化学、仪器分析、制药工艺等),实现上述四个部分相应技术原理的过程。理解并充分了解试剂盒的技术原理是完成工艺研究的基础。
通常,试剂的主要生产工艺应至少包括:包被抗体板制备(抗原抗体反应和分离的实现)、酶标记抗体浓度(信号放大和信号检测的转化,将微观不可检测的抗原抗体反应转化成易于测定的酶浓度)、底物及终止液的配制(信号检测,通过酶催化效率的测定,间接的将抗原抗体反应的量值转换成可由仪器进行测定光学信号),以及其他辅助组分溶液的配制。组份的分装、半成品检定、包装、成品检定均为普适工艺,多数试剂的生产都含有这些生产工序。
有一点值得大家注意,部分试剂的配方浓度不单单涉及工艺配方上的研究,还涉及到反应体系研究的问题。例如,酶标板包被抗体浓度、酶标记二抗浓度,均与反应过程中样本量、试剂量的多少有关。所以,任何试剂的生产工艺研究与反应体系研究是密不可分的,难怪注册申报材料中就将生产工艺与反应体系研究合并在一起作为一份材料。
国家食品药品监督管理总局关于公布体外诊断试剂注册申报资料要求和批准证明文件格式的公告(2014年第44号) 附件3 体外诊断试剂注册申报资料要求及说明;
五、主要生产工艺研究资料主要生产工艺包括: 工作液的配制、分装和冻干,固相载体的包被和组装, 显色/发光系统等的描述及确定依据等。
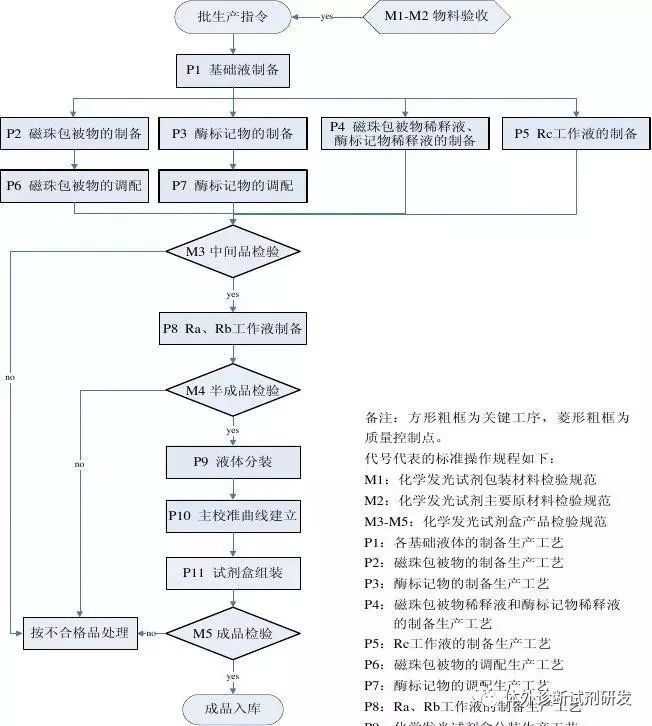
(1)确定工艺流程与关键工序
常规方法学的不同试剂,其基本工艺比较成熟且大同小异,大家可以通过查阅相关资料和参考文献并结合产品自身的特点进行适当地调整即可。
关键工序的确定,应从风险控制的角度考虑,凡是生产过程的环节,其控制效果直接影响到产品的质量(有效性、安全性等),都应该作为关键工序。具体一点来说,就是对工艺上有特殊要求或对下道工序有较大影响的工序、或工艺加工/操作难度大、质量较易波动或问题发生较多的工序。举一个例子,同样是分装操作,一个是ELISA试剂中的样品稀释液,一个是需要进行冻干的试剂校准品,对于前者往往实际分装的时候分装量较大且有一定的富余量,该分装过程对于分装误差的可接受范围较大;而对于后者,由于冻干的校准品在后续使用过程中要求复溶,该分装过程的误差对于复溶后的浓度影响较大。个人理解,前者是一般工序,后者可作为关键工序。因此,在确定关键工序时,研究及生产等相关人员应该结合产品的实际情况充分讨论,对整个工艺流程中各个环节工序予以确认,是否应该作为关键工序加强质量控制。
(2)工艺研究的确定依据
注册材料要求中明确工艺研究材料内容需阐述主要生产工艺的确定依据。一方面我们需要提供确定工艺的参考资料来源(常规方法学试剂的基本工艺大同小异),另一方面还需要提供一定的实验研究数据进行补充完善(但不同的原材料、生产仪器设备可能会引起生产工艺上部分参数的变化,我们应结合产品自身特点通过实验研究予以调整)。

(3)““大生产”与实验室试制
大家平时讨论时,经常遇到的一个话题便是分析性能评估和稳定性研究所使用产品来源和批次的问题。试生产、小试生产、中试生产,甚至大生产,等等,这些说法一定程度上是沿用了药品的习惯。但是体外诊断试剂和药品在工艺研究过程中还是有一定的区别,严格的说,体外诊断试剂在法规方面并不强调小试、中试和大生产,这些更多的是企业自己的界定。
法规上,体外诊断试剂强调的是在符合质量管理体系条件下厂房车间且按照文件规定进行的产品制备行为。
实验室阶段试制的产品理应完成分析性能评估和稳定性研究,为后续工作奠定基础,但是实验室研制工作基本完成后,还需对在符合质量管理体系条件下厂房车间里制备的产品再次进行分析性能评估和稳定性研究。
另外,不少产品在实验室阶段试制产品规模与车间正常生产阶段生产规模相比有一定的差距,导致在生产过程中所使用的仪器设备、计量器具的精度发生变化(例如,加热方式、不同配液量)。所以,我们完成实验室初步研究后,在符合质量管理体系条件下厂房车间进行试生产、工艺验证的过程中,研究人员和生产技术人员一定要结合实际情况,对工艺进行适当的调整和优化,以保证各工序能够满足产品的设计需求。
(4)工艺研究的基本思路
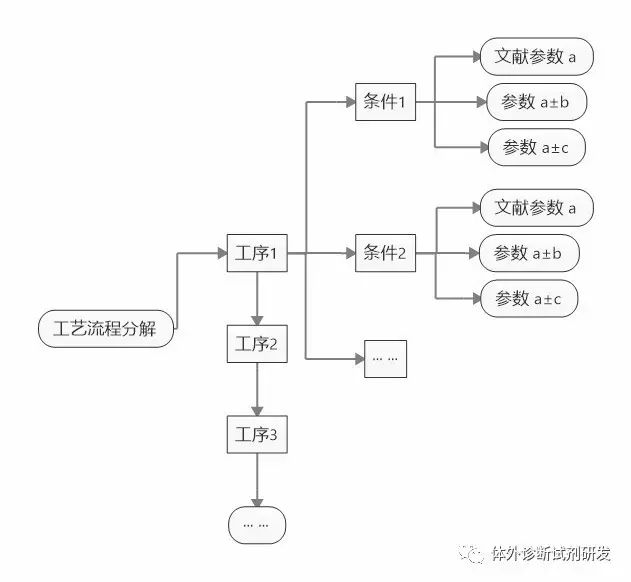
在掌握试剂盒方法原理的基础上,参考文献资料,并结合实践经验对工艺流程进行分解,对于一些关键工艺条件在合理范围内进行探究摸索。产品研制(包括工艺研究)常用到正交试验法、信噪比和加权等科学研究思路和方法,这一部分以后找时间单独写一篇文章聊聊。
原创不易,转载请标明出处!谢谢
持续更新中... ...
—《体外诊断试剂研发》
如果您有好的建议,请联系我:
以下是各种联系方式,欢迎骚扰!(回复可能会延迟,希望大家谅解)
微信:weishilin2999
QQ:924668455
Email:[email protected]
获取更多干货内容,欢迎关注我们的体外诊断试剂研发QQ群204178207。

















