
随着材料科学、医学、生物学的飞速发展,生物医用材料的研究取得了很大的进步,但是仍面临各种挑战,一些根本性的问题没有解决,其中,除了生物相容性问题,生物材料应用的主要障碍还有感染问题。在美国每年至少有10万人死于植入体相关的感染,相关医疗费用有30亿美元,因此生物材料感染的问题给患者带来极大的病痛和经济负担。细菌黏附和繁殖后最终发展成为生物膜,生物膜是细菌和细菌分泌的多糖、蛋白质等形成的复合体系,具有自己的营养物质和废物排泄通道,并通过基因和信号传递实现表型的变化,使细菌的耐药性提高1000倍以上。针对细菌黏附、细菌尸体和细菌生物膜难以清除的关键问题,
温州医科大学眼视光医院/学院的王佰亮副研究员的研究团队构建了温敏型可逆杀菌-释放细菌和基于细菌感染微环境响应的两类智能抗菌表面。
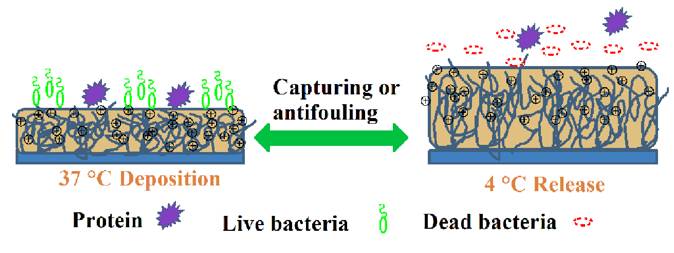
图1. 温敏型P(DMAEMA
+
-
co
-NIPAAm)聚合物刷的可逆杀菌-自清洁示意图
如图
1
和图
2
所示,采用表面引发的可逆加成
-
断裂链转移聚合反应技术,研究者首先构建了聚
(N-
异丙基丙烯酰胺
-(2-(
二甲基氨基)
-
甲基丙烯酸乙酯
)
) (P(DMAEMA
+
-
co
-NIPAAm)
)
二元共聚物,
在
37
℃
表面呈现一定的疏水性,细菌黏附并和季铵盐组分作用被杀死,降低温度到
4
℃
后表面发生从疏水到亲水的相转变,使黏附的细菌被清除,通过四次黏附
-
释放循环实验证实了该聚合物刷的温度刺激响应的杀菌
-
释放细菌尸体可调控性。该研究巧妙地将温敏性组分和杀菌组分复合于材料表面,基于相转变实现了细菌的可控
“
吸附
”
和
“
释放
”
,解决了目前大部分抗菌表面不能有效清除细菌尸体的关键问题,通过简单的温度调控实现材料的自清洁和杀菌功能的恢复(相关研究成果发表在
ACS Applied Materials & Interfaces
,
2016, 8:27207
−
27217
)。
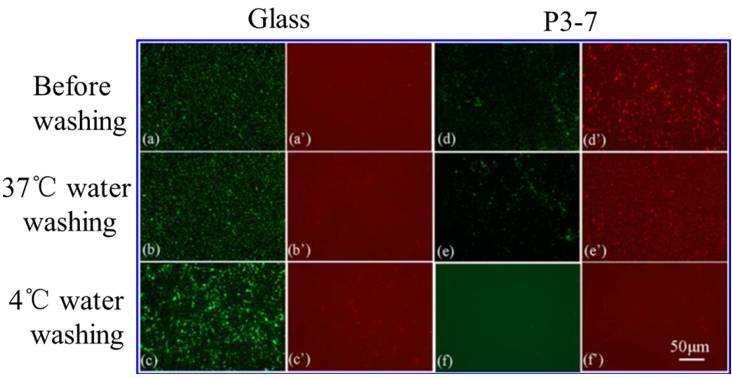
图2. 大肠杆菌和材料接触培养24h清洗前后的死/活染色荧光图(P3-7: DMAEMA
+
和NIPAAm摩尔比为3:7)
在此基础上增加亲水性组分,如图
3
所示,研究者构建了
N-
乙烯基己内酰胺
-(2-
甲基丙烯酰氧基乙基磷酰胆碱
)-(2-(
二甲基氨基
)-
甲基丙烯酸乙酯
)
(
P(VCL-
co
-DMAEMA
+
-
co
-MPC) )
三元共聚物,基于
MPC
的亲水性显著提高了表面的抗细菌黏附能力。通过对涂层组分的调控,增强了表面的在自清洁能力,使温敏性释放功能具有更高的可重复性
(
相关研究成果发表在
Biomaterials Science, 2016, 4: 1731-174
1
,封面报道,
并被中华医学会眼科学分会评选为
“2016
年度中国眼科十大创新成就
”
)。
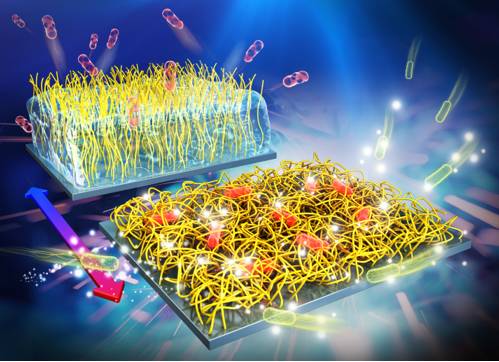
图3. 温敏型P(VCL
-
co
-DMAEMA
+
-
co
-MPC)聚合物刷的可逆杀菌-自清洁示意图
生物材料发生细菌感染后周围的微环境会发生很大的变化,出现pH值降低、细菌释放的毒力因子和多种酶等。依据细菌微环境的变化构建的抗菌响应型表面更具优势,近年来在国际上已经成为研究的重点和热点。如图4所示,研究者成功构建了细菌感染微环境响应性的智能抗菌表面,首先合成了甲氧基聚乙二醇-聚(ε-己内酯)-壳聚糖的嵌段共聚物(MPEG-PCL-CS),制成胶束的过程中负载疏水性抗生素,然后和聚丙烯酸(PAA)进行层层自组装,制备的纳米药物负载体系表现出明显的pH值响应性和细菌响应性药物释放。该研究的针对细菌感染的微环境特点,构建了对细菌感染自卫机制的载药体系,因此提高了药物传递的“靶向性”,在提高抗菌效率和抑制细菌耐药性方面具有重要意义(相关研究成果发表在
Journal of Materials Chemistry B, 2017, 5: 1498-1506
)。
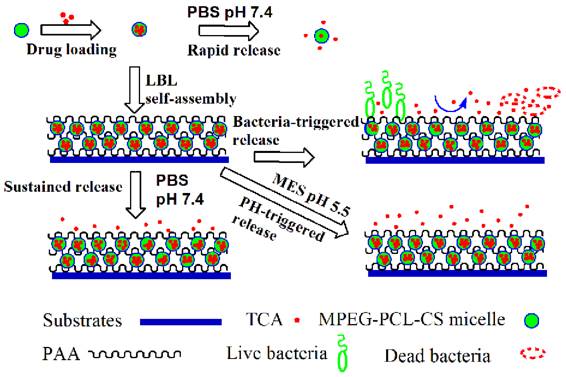
图4. 以胶束为纳米药物载体利用层层自组装技术构建细菌响应性智能抗菌表面
该研究得到国家自然基金青年项目(51403158)、国家自然基金面上项目(81271703)、科技部重点研发计划项目(2016YFC1101201)等项目的资助和支持。

来源:高分子科学前沿
声明:凡本平台注明“来源:XXX”的文/图等稿件,本平台转载出于传递更多信息及方便产业探讨之目的,并不意味着本平台赞同其观点或证实其内容的真实性,文章内容仅供参考。
我们的微博:
高分子科学前沿
,
欢迎和我们互动
。
在菜单中
回复
“
交流群
”:可加入
导师学术群
,
企业界
及
一系列技术交流群
投稿 荐稿 合作:[email protected]






