BioArt按:抗病毒天然免疫通路的激活,传统上认识是由蛋白泛素化和蛋白丝苏氨酸磷酸化所介导,对于蛋白酪氨酸磷酸化修饰的作用与生理功能,未有深入探索和认知。6月14日,浙江大学生命科学研究院徐平龙教授课题组在Cell Host & Microbe杂志上发表了题为“Lck/Hck/Fgr-mediated tyrosine phosphorylation negatively regulates TBK1 to restrain innate antiviral responses”的研究论文,该研究鉴定到了抗病毒应答关键激酶TBK1的直接酪氨酸磷酸化修饰以及修饰激酶,提出了酪氨酸磷酸化修饰和酪氨酸激酶在抗病毒天然免疫中的关键调控作用和生理功能,并深入解析了其抑制抗病毒应答和负反馈调控的分子机制。此外,该研究也首次指出了酪氨酸激酶抑制在抗病毒防治中的潜在重要价值。这些新发现为理解抗病毒免疫机制和发展抗病毒的防治手段提供了新的理论与实验依据。

论文解读:
细胞质核酸识别及其启动的抗病毒天然免疫存在于我们机体几乎所有类型的细胞中,是一类古老而进化上高度保守的细胞生物学机制,不仅对病毒感染防御至关重要,更在自身免疫疾病、神经退行性疾病及肿瘤发生中有重要功能。
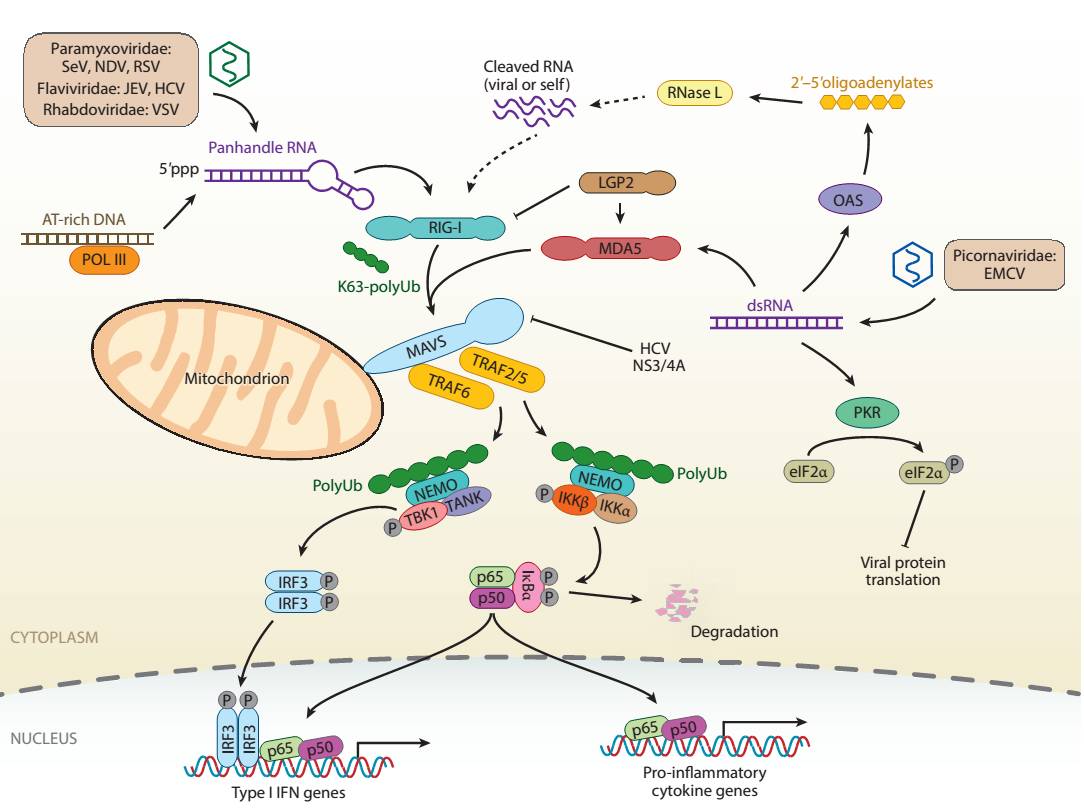
细胞质RNA感知系统。引自:Wu, J., & Chen, Z. J. (2014). Innate immune sensing and signaling of cytosolic nucleic acids. Annual review of immunology, 32, 461-488.
位于细胞质中的RNA/DNA模式识别受体,比如RIG-I(主要感知RNA,见上图)或cGAS(主要感知DNA,见下图),能够侦测到病毒或自身泄漏的核酸并激活,通过线粒体或内质网定位的接头蛋白MAVS或STING,逐次活化关键激酶TBK1和转录因子IRF3,并激活NF-κB通路,诱导表达I/III型干扰素、干扰素诱导基因、促炎症细胞因子等一系列抗病毒因子,从而建立自身和周边细胞的抗病毒状态【1】。抗病毒天然机制研究有重要的科学认知价值和应用前景,也是当前国际生物医学发展的主要前沿之一。
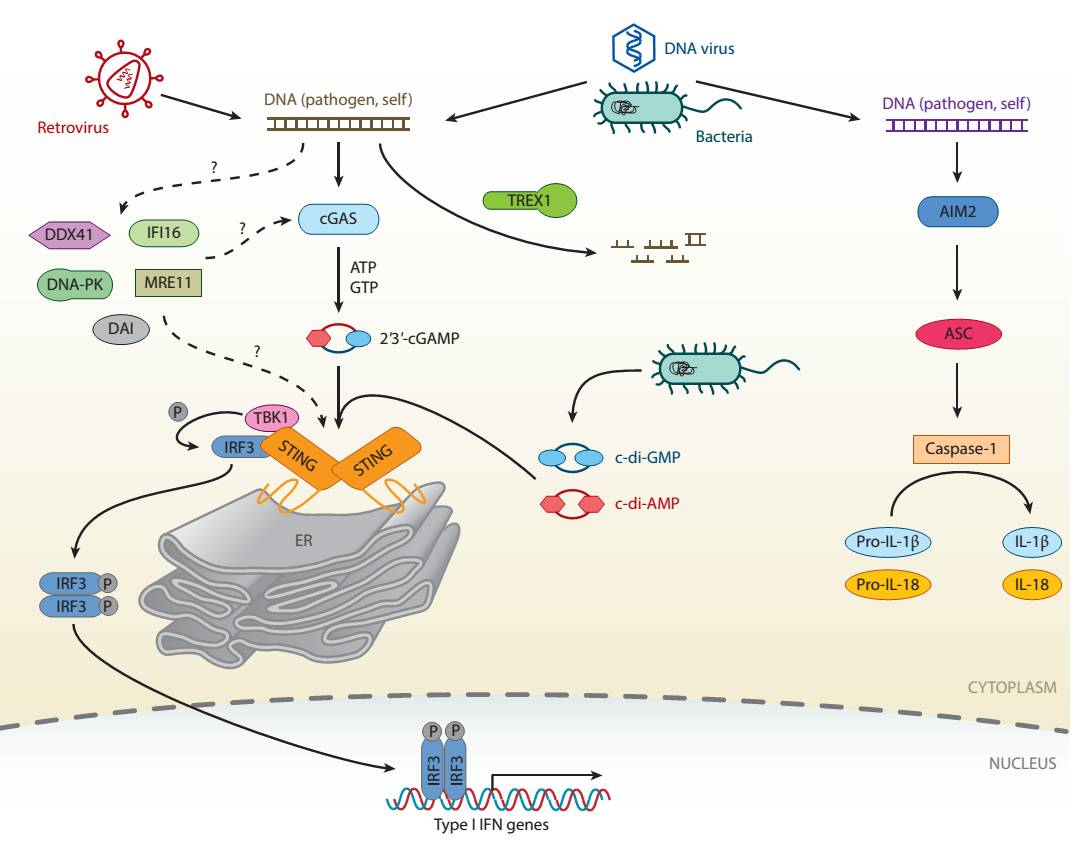
细胞质DNA感知系统。引自:Wu, J., & Chen, Z. J. (2014). Innate immune sensing and signaling of cytosolic nucleic acids. Annual review of immunology, 32, 461-488.
蛋白酪氨酸磷酸化修饰,尽管只占到所有蛋白磷酸化修饰的2.5%,但在细胞的几乎所有生理进程中都有关键调控功能【2】。关于抗病毒天然免疫通路的激活,传统意义上认为主要是由蛋白泛素化和蛋白丝苏氨酸磷酸化所介导,对于蛋白酪氨酸磷酸化修饰的作用与生理功能,尚未有深入的探索和认知。尽管此前的研究认为Src家族酪氨酸激酶(SFK,Src family tyrosine kinases)家族成员(例如Hck和Fgr)的缺失所产生的表型与宿主抵抗病原菌的侵染有关,但是相关的分子机理并不清楚【3,4】
在这项研究中,徐平龙实验室的研究人员发现,病毒感染过程中,在多种器官来源的细胞中都观察到细胞内源TBK1有动态的酪氨酸磷酸化修饰,并与TBK1激活与抑制紧密相关。随后通过小分子抑制剂和蛋白激酶文库筛选以及基因表达和CRISPR介导的基因敲除分析,确定Src家族酪氨酸激酶(SFKs)Lck、Hck、Fgr是导致静态和病毒感染过程中TBK1酪氨酸磷酸化修饰和功能抑制的主要激酶。
从分子机制上讲,Lck/Hck/Fgr与TBK1/IKKe相互作用并形成内源复合体,直接酪氨酸磷酸化修饰TBK1。Lck/Hck/Fgr主要修饰TBK1的394位和354位酪氨酸,破坏其形成TBK1同聚二体或TBK1/IKKe异聚二体的分子介面,导致TBK1失活。Lck/Hck同时也强烈修饰TBK1催化中心附近的153位酪氨酸,进一步阻抑TBK1激活(下图)。
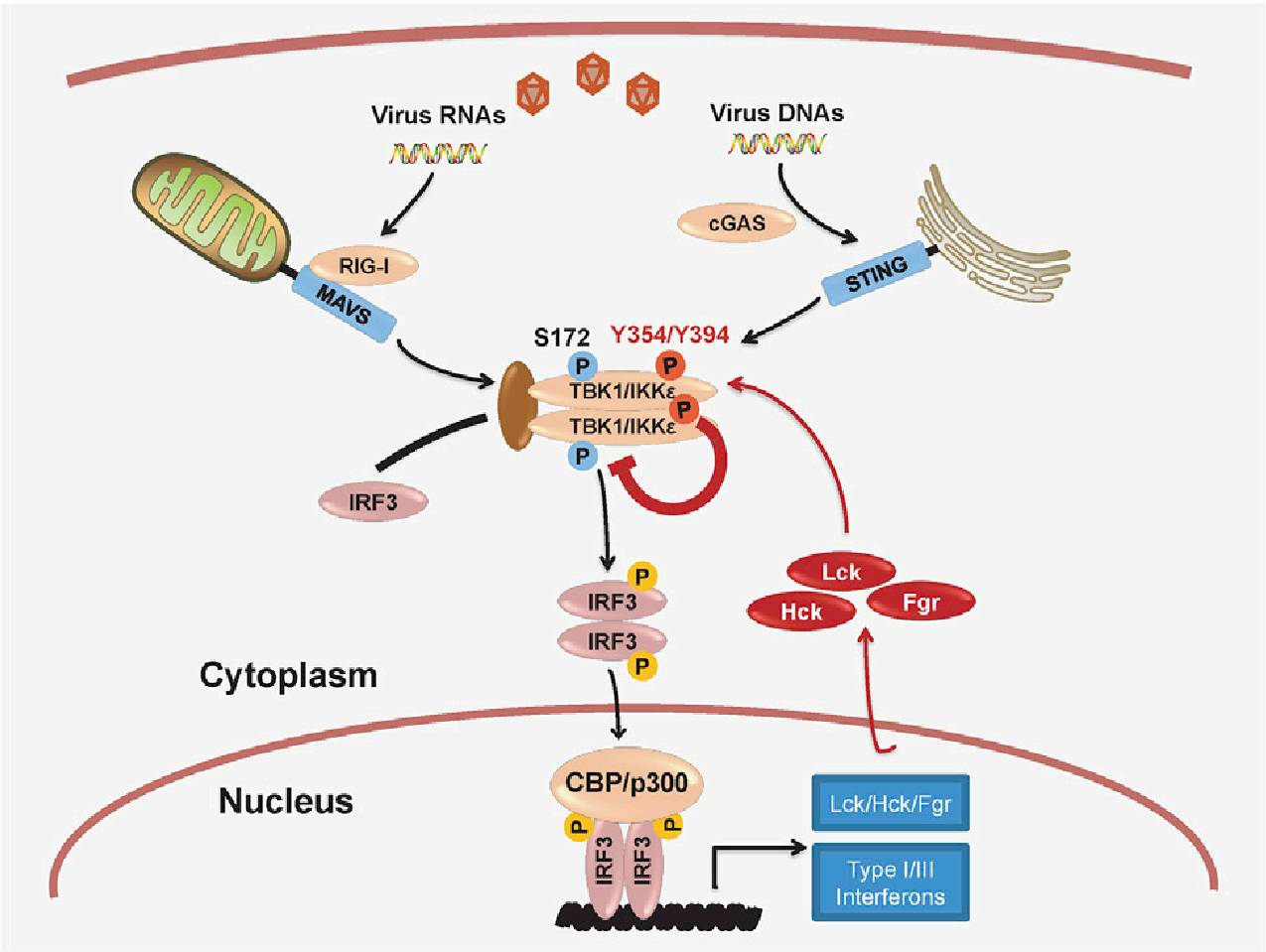
工作模型示意图
因此,Lck/Hck/Fgr的基因敲除或者使用小分子抑制剂能显著提高细胞核酸识别通路的激活和抗病毒免疫应答,以及对RNA病毒和DNA病毒的抵抗能力。更为重要的是,Lck/Hck/Fgr的小分子抑制剂能显著增强小鼠与斑马鱼对病毒感染的防御,而Lck过表达则明显削弱斑马鱼的抗病毒能力。
非常有意思的是,核酸识别通路的激活能直接通过IRF3介导的转录,强烈诱导Lck/Hck/Fgr蛋白表达,构成了对核酸识别通路的负反馈调控。
总的来讲,该研究鉴定到了抗病毒应答关键激酶TBK1的直接酪氨酸磷酸化修饰以及修饰激酶,提出了酪氨酸磷酸化修饰和酪氨酸激酶在抗病毒天然免疫中的关键调控作用和生理功能,并深入解析了其抑制抗病毒应答和负反馈调控的分子机制。此外,该研究也首次指出了酪氨酸激酶抑制在抗病毒防治中的潜在重要价值。这些新发现为理解抗病毒免疫机制和发展抗病毒的防治手段提供了新的理论与实验依据。
据悉,徐平龙实验室2014年博士生刘盛铎和2014年硕士生陈莎莎为论文共同第一作者,李欣然博士、吴世英同学和张倩同学也在工作中有重要贡献,通讯作者为徐平龙教授。研究工作也得到了浙江大学冯新华教授、邹键教授、夏总平教授、叶升教授、沈立教授等大力支持。该研究受到国家自然科学基金、科技部973计划和中组部青年千人项目等资助,在浙大生研院开展并完成。
BioArt后记:徐平龙老师2013年回国到浙江大学生研院任职(2015年才入选“青千”),当年10月份才启动实验室。在不足四年的时间里,徐老师作为通讯作者先后在Mol Cell、Gene Dev、 Science Advances、Nature Cell Biology和Cell Host & Microbe等杂志上发表多篇研究性论文,并且还受邀在Cold Spring Harbor Perspectives in Biology杂志上撰写综述论文(与冯新华教授合写),正所谓高产优质。特别值得一提的是徐老师实验室培养博士孟凡森同学今年还入选了国家“博士后创新人才支持计划”资助(两年60万元,其中40万元为博士后日常经费,20万元为博士后科学基金)。最后,BioArt祝贺徐平龙老师今后取得更大的突破!
参考文献:
1、Wu, J., & Chen, Z. J. (2014). Innate immune sensing and signaling of cytosolic nucleic acids. Annual review of immunology, 32, 461-488.
2、Hunter, T. (2009). Tyrosine phosphorylation: thirty years and counting. Current opinion in cell biology, 21(2), 140-146.
3、Meng, F., & Lowell, C. A. (1997). Lipopolysaccharide (LPS)-induced macrophage activation and signal transduction in the absence of Src-family kinases Hck, Fgr, and Lyn. Journal of experimental medicine, 185(9), 1661-1670.
4、Nelson, M. P., Metz, A. E., Li, S., Lowell, C. A., & Steele, C. (2009). The absence of Hck, Fgr, and Lyn tyrosine kinases augments lung innate immune responses to Pneumocystis murina. Infection and immunity, 77(5), 1790-1797.

徐平龙博士,浙江大学生命科学研究院教授、博导;细胞信号网络协同创新中心研究员;中组部青年千人;浙江省特聘专家。徐平龙博士于1998年本科毕业于四川大学生物系,2003年在中科院上海生化与细胞所汪垣教授指导下获博士学位,博士后受训于TGF-β领域奠基人之一UCSF的Rik Derynck教授,之后作为研究助理教授在UCSF工作,至2013年夏受聘于浙大生研院。实验室致力于采用细胞生物学,生物化学,免疫学及小鼠与斑马鱼模式动物等手段研究抗病毒天然免疫和肿瘤转移的细胞信号传导机制及其调控规律。主要研究兴趣为抗病毒天然免疫应答、TGF-β信号通路、ADAM家族金属蛋白酶和肿瘤增殖与转移,并取得了多项有国际影响力的原创性成果,包括阐明炎症肿瘤微环境和宿主防御体系控制肿瘤增殖和转移的全新功能和分子机制,以及动态磷酸化调控抗病毒宿主防御的功能与机理。2015年入选国家第11批千人计划(青年人才项目)及浙江省海外高层次创新人才长期项目。研究工作以通讯或第一作者发表在多篇国际权威学术期刊上。其中2013年回国后以通讯作者在Nature Cell Biology、Molecular Cell、Genes & Development、Science Advances等国际权威期刊发表数篇研究论文。2016年徐平龙教授还与冯新华教授与合作在国际权威期刊Cold Spring Harbor Perspectives in Biology 上应邀发表题为“Posttranslational Regulation of Smads” 的综述论文。研究工作并受同行广泛好评,被Molecular Cell专门评述、两次被选为Science Signaling编辑专评、并被生物和医学论文数据库Faculty of 1000推荐。


BioArt,一心关注生命科学,只为分享更多有种、有趣、有料的信息。关注请长按上方二维码。投稿、合作、转载授权事宜请联系微信ID:fullbellies或邮箱:[email protected]。













