
程序员敲出一行行特殊的代码,计算机会运行出相应的结果,某种程度上人类的身体亦是如此。人类所有的遗传信息都写在46条染色体上,你的发色、肤色、健康程度、甚至思维方式,在你还是一颗受精卵的时候就已经被写好。
那么问题来了,程序如果发生错误程序员可以及时修改,那人类生命的代码呢?
长久以来,遗传性疾病是人类无法避免又难以逾越的障碍。这段出现在生命里的错误像诅咒一样与患者终生相随,有的时候它甚至会影响到整个家族。直到上世纪60年代,DNA剪切酶和连接酶的发现让研究者异常兴奋——这也许就是重新编辑生命代码的那双手。
2016年5月,全球制药巨头葛兰素史克公司(GlaxoSmithKline,GSK)的基因疗法Strimvelis被欧盟批准上市,这是基因治疗走向市场的又一里程碑事件。
Strimvelis是由GSK公司与意大利科学家共同研发,用于腺苷脱氨酶-重症联合免疫缺陷症(简称ADA-SCID)治疗,其方法是首先获得患者自身的造血干细胞,在体外进行扩增培养,之后利用逆转录病毒将正常ADA(腺苷脱氨酶)基因导入其造血干细胞,最后将修饰后的造血干细胞回输到本人体内。Strimvelis并不是简单地药物治疗,其费用更是天价——594,000欧元,合约450万人民币。
就在本周二,GSK的新闻发言人Anna Padula称,他们在今年三月接收了第一名患者——在Strimvelis上市接近一年之际。
治疗案例如此惨淡的首要原因自然是极其昂贵的治疗费用,因此GSK公司一开始就把治疗场所设置于位于米兰的Ospedale San Raffaele——一个可以享受欧盟医疗政策的中心,这样来自28个国家的儿童可以由母国支付昂贵的治疗费用。
另一个原因不在于治疗本身。由于ADA-SCID的罕见性,每年欧洲只有大约15个儿童会患病。在这种情况下,各国的科研实验也试图分一杯羹,更多的患者愿意就近接受医院内的临床试验而不是去米兰接受商业化治疗。
 图 | 美国将在 2017 或 2018 年首次上市基因治疗方法
图 | 美国将在 2017 或 2018 年首次上市基因治疗方法
基因疗法——从胜天半子到绝处逢生
基因疗法,也称基因治疗(gene therapy)是利用分子生物学方法将外源正常基因通过病毒载体导入患者体内靶细胞,使之达成目的基因产物,以纠正或补偿因基因缺陷或异常引起的疾病,以达到治疗人类疾病的目的。
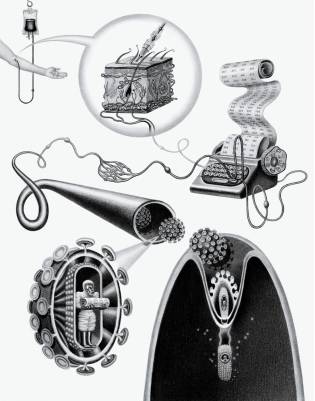
图 | 基因疗法示意图
研究者在经过了前期数十年的动物实验,基因疗法终于在1990年得到了实质性的进展——成功治愈一名患有严重免疫缺陷综合征的4岁女童。
严重联合免疫缺陷综合征(Severe Combined Immunodeficiency, SCID)是一种罕见遗传病,是由于基因突变导致T细胞和B细胞功能障碍引起的,患者的免疫功能几乎完全丧失,对细菌、真菌、病毒和原虫感染均缺乏抵抗力,目前已知导致缺陷的基因突变至少有9种,患有SCID的婴儿大多活不过两岁。
研究者从接受治疗女孩血液中提取白细胞,将正确序列插入错误基因中,得到修正的细胞,再将细胞注射回女孩体内。女孩被治愈了,基因治疗首次在人体实验中获得成功,研究者非常振奋,似乎看到了生命科学的舞台上,聚光灯就要聚集在基因治疗上。
 图 | 前排右一为 1990 年治愈 SCID 女孩(摄于 1992 年)
图 | 前排右一为 1990 年治愈 SCID 女孩(摄于 1992 年)
“以命相搏,胜天半子”,这大大的激励了研究者,他们将相同的治疗方法应用在其他类型的SCID患者的治疗中,遗憾的是,诅咒并不是那么容易被打破。
其他类型SCID患者在接受治疗后出现了白血病,甚至部分载体病毒载入错误的基因组诱发了原癌基因的表达。事情在1999年到达了冰点,18岁的Gelsinger在临床试验后对转录载体产生了严重的免疫反应。病毒载体将功能基因过多的转运到细胞中,引起免疫过度,最终导致了器官衰竭和脑死亡。
痛定思痛,科学家对可用的病毒载体进行了更透彻的实验。近来年随着腺病毒、腺相关病毒、慢病毒等的出现,基因治疗又重新回到了舞台的中央。
基因疗法的商业化---道阻且长
从科研到实业,注定是一条坎坷的道路,UniQure生物技术公司做了第一个吃螃蟹的人。他们的药物Glybera早在2012年就一路绿灯在欧洲上市,但上个月他们宣布将撤下欧洲市场的Glybera。
据悉,Glybera是一种治疗脂蛋白酯酶缺乏遗传病(LPLD,又叫做家族性高乳糜微粒血症)的药物,LPLD同样是一种罕见的隐形遗传病,表现为患者体内缺乏脂蛋白脂肪酶,进而使血液中的甘油三酯和乳糜微粒浓度升高。
Glybera治愈LPLD大概需要125万欧元,因此此药一出,就获得“最贵药物”的称号。但Glybera短暂的商业生命不仅由于高昂的价格,更由于受众少,整个欧洲只有不足200患者,接近5年的运营却只接收了1位患者,而Glybera的失败也同时宣告了基因疗法第一次商业化的铩羽而归。
 图 | 首个商业化基因治疗药物:Glybera
图 | 首个商业化基因治疗药物:Glybera
实际上,除了周二宣布的案例,位于伦敦中心的大奥蒙德街医院(Great Ormond Street Hospital)在ADA-SCID的治疗上也有了成功的案例。英国研究者采用另外一种基因疗法,成功治愈了一个患有耐药性白血病的一岁女孩,成为免疫细胞疗法治愈“不可治愈”的癌症的全球首个案例。对于美国和加拿大的患者,加州大学洛杉矶分校同样有ADA-SCID的临床试验。
虽然在某些罕见疾病的治疗上,基因疗法取得了可观的结果,但对于由多基因引起的常见疾病,基因疗法还有很长的路要走。但至少,我们真的找到了重新编辑基因的入口,逆转了某些本来毫无胜算的赌局。重新编写生命信息也许就在明天,而明天我们就是诅咒的终结者。
编译:沙吉惠
参考:
https://www.technologyreview.com/s/604295/a-year-after-approval-gene-therapy-cure-gets-its-first-customer/
http://www.bloodjournal.org/content/early/2017/03/28/blood-2016-12-756734
http://www.nature.com/nature/journal/v526/n7573/full/nature15818.html
-End-
「DeepTech深科技」招募全球记者、采编
申请加入:[email protected]
















