分子生物学的最新进展正在加速基因组测序来支撑精确医学。这种进展是将基因和基因修饰细胞治疗定位在当前满足患者医疗需求的革命性的尖端技术--并且是可以和单克隆抗体MAb相抗衡的重要新型治疗方法。然而,尽管基因和基因修饰的细胞疗法在临床试验中取得了巨大进展,但生物工艺群体正在努力奋斗,扩大其生产能力,以满足日益增长的需求,这也包括目前按药品生产质量管理规范CGMP进行生产的病毒载体。
在此,我们回顾基因治疗生物产品的基础科学,并评估关键的新兴生物工艺的机会和挑战。叙述病毒载体上游和下游生物工艺策略与其他治疗平台如嵌合抗原受体CAR-T细胞和诱导多能干细胞iPSCs的策略之间存在相互关系。
基因和基因修饰的细胞疗法是通过在体内活体或体外离体将治疗性DNA导入到患者的细胞中来治疗疾病。其治疗策略为替代或纠正缺陷性基因或导入编码治疗性蛋白。 新基因的引入通常是通过直接或基于细胞的基因治疗方式用病毒转导靶细胞来实现。
第一次基因治疗临床试验在1990年进行,治疗的是患有严重联合免疫缺陷病SCID的四岁患儿。此后,病毒基因转送系统的安全性和效率取得了巨大进步。正在研究的策略包括基因替代和基因敲除方法以及经典基因添加。然而,值得注意的是大多数正在进行的临床试验 - 其中超过60%用于癌症 - 使用基因添加法。
腺病毒相关病毒AAV和慢病毒载体两者都在基因治疗领域许多适应症的新开发产品中采用。 图1描绘了目前正在采用基于AAV的载体的研发产品的公司,图2描绘了开发基于慢病毒载体的机构。 采用两种病毒载体类型开发的治疗某类疾病的产品数量图3。
![]()
图1 开发AVV载体的组织机构
![]()
图2 开发慢病毒载体的组织机构
![]()
图3 AVV和慢病毒应用于基因治疗的适应症和药物数量AVV:上图,慢病毒:下图)
无论直接的基因治疗还是基于细胞的基因治疗,其第一步是将治疗用转基因包装到传送载体如病毒载体中,随后扩增其宿主细胞以产生足够高浓度的载体。在直接基因传送中,将治疗性转基因直接注射入活体靶组织; 基于细胞的基因治疗需要对靶细胞进行分离和离体培养,随后对其进行基因修饰,再进行扩增和富集重新回输患者体内。 图4提供了制造工艺概述。
![]() 图4 典型的病毒生产工艺概要
图4 典型的病毒生产工艺概要
为提高工艺经济性,批量之间可以组合以制备更大量的最终载体药物。 一旦亚批次产品的目标数量达到可用的有效滴度,在无菌生产过程中它们可以混合在一起形成一大批次产品,包括进一步处理的无菌过滤和无菌分装达到目标载体浓度。相比于离体应用,对于某些活体内基因治疗制剂,其可能需要更高的体积浓度例如,≤2,000倍。
有几种类型的病毒可以被用作载体将功能基因的拷贝转移到患者的细胞中(图5)。基于非致病性人细小病毒的AAV载体非常适合用于直接基因治疗。AAV载体的特征是低免疫原性,目前为止直接活体应用是安全的。来自uniQure公司荷兰阿姆斯特丹的Glybera alipogene tiparvovec是欧洲首例可商业化购买使用的基因治疗方法,其使用AAV1载体携带人类脂蛋白脂肪酶LPL基因。其肌内注射应用于患有家族性脂蛋白脂肪酶缺乏症LPLD和虽然饮食脂肪限制仍有严重或多发性胰腺炎发作的成年患者。
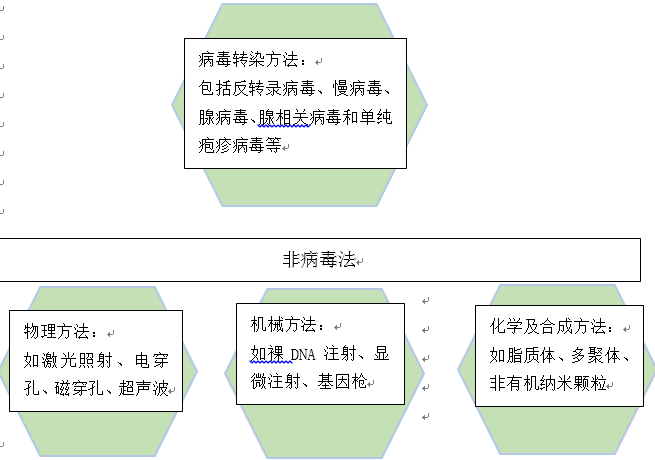
图5:基因治疗载体概况摘自《转染方法简介》
基于细胞的基因治疗的大多数方法使用的病毒载体可以感染分裂和非分裂细胞。它们从基因上修饰靶细胞,如T细胞以诱导免疫功能或成年体细胞以诱导多能性。成功使用取决于两个关键原则:鉴定合适的治疗性基因并成功地将其传送至靶位点并保持其有效性例如基因表达。
使用携带关键安全特征的第三代最小慢病毒载体至关重要。采取措施例如,密码子优化gag/pol以最小化载体组分之间的同源性并防止重组,和自我失活长末端重复LTR序列,并去除所有非必需的序列和辅助基因等共同防止复制慢病毒能力的重新获得。通常,gag/pol基因包装构建编码病毒结构蛋白gag和酶pol,其与具有编码来自异源的合适的包膜糖蛋白的其他病毒载体,形成“假型”载体颗粒。这需要产生第三构载体用于表达病毒辅助蛋白Rev与编码转基因以及有效逆转录,RNA包装和整合所需的其他序列的第四载体质粒一起工作。
鉴定合适的治疗基因并保持最佳的转基因表达在基因治疗产品开发中仍然是巨大的挑战,需要精确的转基因调控以减轻意外不良反应。两个关键的遗传元件调节转基因表达:启动子和增强子。启动子分为组成型和诱导型功能性分为普通型和特定组织型,能够实现特定基因的连续组成型或瞬时诱导型转录。虽然一些启动子如黑素细胞特异性酪氨酸酶启动子显示出强健的转录活性和高度特异性,但是其他启动子效果比较差,需要一定程度的“增强因子”来增强其作用。这种增强可以通过许多策略实现,包括除去无效启动子区域,显示阳性调节组分的位点复制,不同组织特异性启动子的组合和使用重组转录激活子RTAs以促进DNA和来自选择的特异性蛋白质的反式激活结构域的结合。一旦确定了合适的治疗基因,就必须将其有效传送到靶细胞。
载体传送:
靶向基因传递涉及扩大载体的趋向性以转导先前非许可的细胞或替代病毒趋向性专门转导特异性靶细胞。 这些方法具有增强治疗效果和减少副作用的潜在优势。将治疗基因提供给目标部位,必须选择合适的载体。载体传递可以大致分为病毒类或非病毒类(图5)。理想载体应该表现出以下关键特性:
•严格规范的表达
•低不良反应特征
•持续可控的治疗效果
•靶细胞特异性
•DNA容量。
质粒DNApDNA用作一些基因治疗的非病毒基因转送载体。pDNA具有良好的安全性,低毒性和提供更大的基因负荷能力,是病毒传导DNA方法的替代方案,可适应许多物理和机械传递策略。然而,它们受到“生物屏障”的限制,如肾清除,内体腐蚀和血清内切核酸酶的降解。因此,到目前为止,约70%的基因治疗临床试验采用病毒载体系统。
机械和物理传导:
已经设计了许多方式来机械地和物理地将基因治疗传送到其目标区。可用的技术存储库包括显微注射,粒子轰击“基因枪”技术,激光照射,电穿孔,超声穿孔和磁转染(表1)。这些方法试图将核酸传送到细胞,并提供有利替代方法替代基于载体的靶向和免疫原性相关并发症。例如,在心脏病学方面,一些机械/物理方案被专门用于治疗心血管疾病。它们包括使用导管用于顺行或逆行输注和直接注射经皮心肌内或手术侵入性给药并辅助以电化学测绘。
在1980年首先使用的显微注射技术是针对基因治疗目的设计的,其将外来DNA注射入哺乳动物细胞质和自身天然DNA内。在现代实践中生产转基因小鼠是一件普通的事情。尽管概念上非常简单,但单细胞转染方法每次操作仅允许转移几百个细胞,因此其大部分被机械,物理和载体传送方法所替代。
粒子轰击,也称为基因枪或弹道基因传递,其使用重金属颗粒将裸DNA质粒推进入靶细胞。这种技术已被谨慎地用于治疗许多临床适应症如癌症治疗,基因疫苗接种和促进伤口愈合。但是它的效果依赖于颗粒的最佳DNA负载,甚至到最终分布和递送时间等复杂因素。
物理基因传递方式也包括激光照射。将钛蓝宝石或钕掺杂的钇铝石榴石Nd:YAG源发出的激光聚焦在特定的靶细胞上,增加其在照射部位的渗透性。这使得存在于周围培养基中的任何基因能够穿过细胞膜并进入细胞。作为一个相对较新的概念,基于激光的基因传递方法缺乏广泛的临床应用,需要持续的研究。
电穿孔也增加细胞膜的渗透性--这是通过将靶细胞暴露于电场实现的。与激光照射一样,瞬时细胞膜破裂形成纳米尺寸的瞬时水孔允许存在于周围介质中的遗传物质进入细胞。已经有几种可用于此类用途的商业化设备,但是与这些多孔性开口相关的具体作用机制仍有争议。再次,需要进一步研究电穿孔机制,使其从临床前研究进入临床实践。
磁转染使用磁场来增强载有DNA和相关转染组分的可生物降解纳米颗粒的转染。外部磁场驱动这些颗粒进入到靶细胞中。这种技术的优势结果已经被报道,亮点在于其应用于原代细胞类型的效率能够得到保障。
最后,超声波也被用于通过称为声孔效应的方法诱导细胞膜中的孔形成。高强度超声波引起细胞外液体的物理运动,导致直接的膜空化或气泡塌陷和随后的孔感应。虽然这种方法已经成功的应用于许多细胞和组织类型,它受限于不精确的能量定位和不加选择的空泡化,导致转染效率较低。 如果成功解决这些限制,超声转染则可以提供一种可行的细胞转染技术手段。
对于能提供治疗选择可行的机械和物理基因传递方法,除了上述提及的技术特异性改进之外,必须克服与细胞膜和细胞内环境有关的许多挑战。有几种技术已经证明能产生细胞膜孔的功效; 然而,这些孔的精确特性例如直径和持续时间尚未得到很好的控制。正在进行的研究工作必须着重于建立关键质量属性CQAs,这将有助于研究者优化其基因传送应用和临床疗效。
病毒载体:
病毒是传递遗传信息的天然丰富,优化的运输工具,因此它们已成为重要临床研究工作的重点见表2。 病毒的自然生命周期可以分为两个不同的阶段:感染和复制。前者引起宿主细胞摄取病毒基因组,并导致随后的基因表达。在基因治疗中被利用的正是这种特性,其中病毒基因组被装载有治疗基因盒的修饰基因组所替代,并将其随后导入靶细胞。
|
表
1
物力和机械传递方法概要;操作的困难程度:高,
(
• • •)
中,
(
• •),
低
(
•)
|
|
显微注射
|
离子轰击
|
激光照射
|
电穿孔
|
磁感染
|
声孔效应
|
|
描述
|
用细玻璃针直接将
DNA
注射到细胞浆或细胞核
|
通过加速微粒载体将裸质粒
DNA
带人靶细胞
|
透镜聚焦激光增加靶细胞通透性
|
靶细胞暴露于电场引起细胞膜通透性增加
|
磁场驱动装载
DNA
的纳米磁珠进入靶细胞
|
高能超声波在细胞膜引起空洞
|
|
操作的困难度
|
• • •
|
• •
|
• •
|
•
|
•
|
• •
|
|
优点
|
直接核注射起效,高转染效率
|
多种用途,可以商业化获得
|
易操作,精确聚焦
|
DNA
广发分布于靶位点,高效率增加机油表达
|
高转染效率,能够转染困难的靶细胞
|
非侵袭性,超声波在临床上已经使用
|
|
缺点
|
不切实际,低质量细胞转染,技术困难
|
效率变异大,粒子载体分布变异大
|
费用昂贵,缺乏广泛使用
|
作用的精确机制不清楚,细胞活力不良
|
具有磁颗粒调节细胞功能的潜在风险
|
缺乏精确性,不均匀成空,低转染效率
|
|
表
2
病毒载体概要
|
|
反转录病毒
|
慢病毒
|
腺病毒
|
腺相关病毒
|
单纯疱疹病毒
|
|
举例
|
反转录肿瘤病毒,猿猴泡沫病毒,VSV
|
假型
VSV
,
HFV
|
2
型和
5
型人腺病毒
|
人类细小病毒,
AAVs1-6
|
HSV-1
|
|
基因组
|
RNA
|
RNA
|
dsDNA
|
ssDNA
|
dsDNA
|
|
外源性
DNA
插入
|
最长
8Kb
|
8-10Kb
|
大于
8Kb
|
5Kb
|
大于
30Kb
|
|
优点
|
有效整合入靶细胞染色质,临床测试中
|
有效转化非分裂细胞如
CNS
α),长期转基因表达,应用于过继性
T
细胞平台,临床测试中
|
临床试验期,可证明效率
|
无已知相关疾病与
AVV
感染有关,低毒,长期表达,临床测试中
|
有限感染多种细胞类型
|
|
缺点
|
限于体外使用,插入突变
|
插入突变,临床前期,限制插入基因盒的大小
|
预先存在免疫和炎症反应,操作复杂
|
T
细胞反应,抗体中和,
DNA
装载能力低
|
缺乏长期表达和病人实验,处在临床前期
|
|
生产注意事项
|
服从于无
RCR
放大和库存
|
易于大规模临床生产
|
达到
10L
到
50L
临床级生产
|
下游工艺复杂
|
滴度低
|
|
AAV =
腺相关病毒; HSV =单纯疱疹病毒; RCR = 可复制反转录病毒; CNS = 中枢神经系统 (包括神经元和胶质细胞); VSV = 水疱性口炎病毒; HFV =人泡沫病毒; DSP = 下游工艺
|
为了有效的疾病管理,进入靶细胞的治疗性遗传物质的量必须根据相应疾病的性质精确地控制。遗传性疾病的治疗可能需要长期而不是短期的基因表达。仔细选择和生产病毒载体对于实现这种效果至关重要。
为了生产病毒载体,用于培养目的的细胞通常采用两种方法:基于2D平面技术的贴壁细胞系统的扩展和在搅拌釜生物反应器中放大的3D悬浮细胞培养物。
对于大规模生产,贴壁细胞系统例如,T型瓶,滚瓶,中空纤维技术和多层烧瓶的常规实验室方法在扩大规模方面构成相当大的挑战。尽管预估满足临床需求所需的病毒载体的确切数量有所不同,但开发商正在逐渐放弃小规模生产,并越来越多地选择运行较大规模的设备如不锈钢或一次性生物反应器培养系统。在扩大规模中最重要的是必须认真考虑病毒的敏感性和稳定性。随着产量的扩大,剪切力、pH条件和温度等因素变得越来越重要。
慢病毒载体是做为γ-逆转录病毒载体的安全替代品出现在20世纪90年代。因为慢病毒具有将基因插入到分裂细胞和非分裂细胞中的能力,慢病毒作为基因和基因修饰细胞治疗的重要手段迅速获得发展。使用这些载体诱导多能干细胞iPSCs(图6)使其成为再生医学发展的基础技术,同时它也应用于直接基因治疗或者作为免疫治疗的活化剂。由于传统的实验室培养方法的局限性和对慢病毒载体的需求持续增加,越来越多地使用更新型更大规模的生产方法。它们包括一次性固定床生物反应器,封闭系统中空纤维生物反应器和一次性生物反应器。已经证明中空纤维生物反应器中的载体滴度与使用烧瓶或Nunc公司细胞工厂托盘培养物达到的滴度相当:每毫升1.7×10
8
个病毒基因组vg/mL至2.6×10
8
vg/mL。
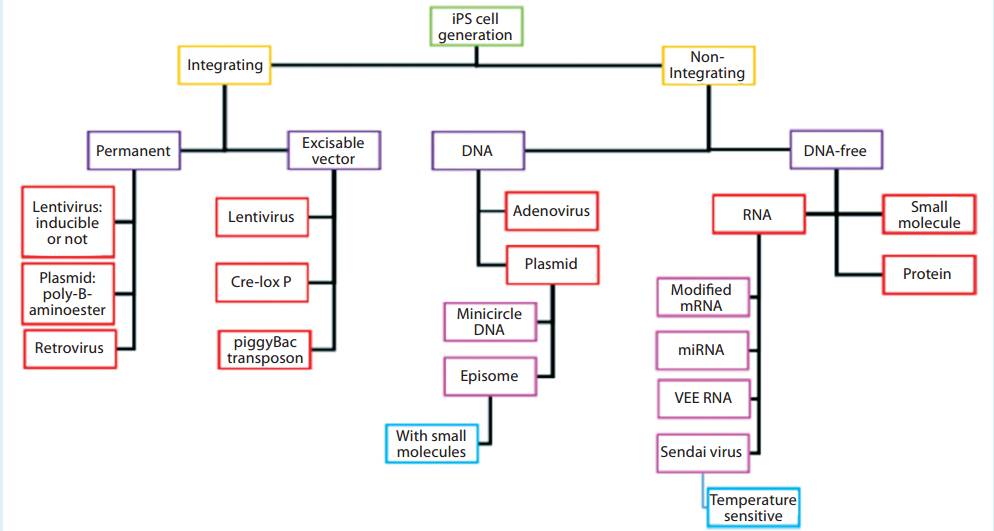
图6 基因传递方法和诱导干细胞生产技术
然而,在大规模生物反应器中培养的
悬浮适应性生产细胞系
由于其增强的可扩展性和消除了分离剂而更适宜于治疗产品的表达,这有助于促进管理的依从性。
腺病毒载体可以由人胚胎肾HEK293和人胚胎视网膜PER.C6细胞系产生,这两种细胞系也可用于慢病毒载体的生产。在不断增长的临床需求的推动下,腺病毒载体生产的技术也获得进步,以帮助企业提高其总产量。除了已经使用的固定床反应器,2D平面技术系统、多单元并行处理系统和包含微载体珠的生物反应器也已被使用。然而,本行业出现了有利于适应悬浮培养物的细胞例如,HEK293,其可以在无血清培养基中成功生长,从而提供更高的安全性和降低的成本CoG。无血清悬浮培养物在操作上是直接的,适合于在搅拌釜生物反应器中进行工业化规模放大,适宜1,000-L至10,000-L的生产能力。
对于AAV生产,报道的瞬时转染可获得的产量范围在10
15
-10
16
vg,其足以满足一般的基于AAV的基因治疗方案。而目前的专利转染技术会远远超过上述报告的产量。这可能需要扩大生产才能满足更广泛的临床适应症或更高的剂量要求。在uniQure公司荷兰阿姆斯特丹使用的杆状病毒表达载体系统BEVS用于生产alipogene tiparvovec的方法可提供合适的选择。由Kotin等人开发的BEVS使用草地贪夜蛾Sf9细胞感染含有载体基因组、辅助基因和衣壳的重组杆状病毒,在100L至200L生物反应器中能产生每升10
14
-10
16
个病毒基因组的产量。预计会随着生产规模的逐步扩大产生更高的收益率。其他可扩展系统包括采用Henrietta Lacks肿瘤HeLa和幼仓鼠肾BHK-21细胞的细胞系来生产5型腺病毒Ad5和单纯疱疹病毒1HSV-1。使用10L摇摆式一次性生物反应器,BHK-21系统已达到10
14
vg/L的产量。
对于
下游工艺
特别是病毒纯化,使用许多策略来选择目标产品并消除不需要的污染物。然而,由于其生物物理化学性质和表面特征的差异,必须仔细考虑每种不同类型的病毒载体。许多策略着重于病毒大小的区别或电荷特征。由于其可扩展性和劳动强度的限制,整体行业趋势是逐渐放弃传统的纯化过程如超离心,因此更适合放大生产规模的色谱技术越来越受欢迎。与病毒颗粒表面相关的选择性结合化学物质可以通过环境调节如悬浮液pH或加入带电荷交换介质和膜来影响。
与所有人用治疗制剂相关的生产工艺一样,质量控制Q和放行测试是确保产品安全性,纯度和效力的重要活动。病毒载体的结构复杂性使得QC测试具有挑战性。新的分析方法系统地处理每种病毒载体的各种疗法。可以采取某些措施来提高生产工艺的鲁棒性和质量。它们包括封闭系统工作减少操作员操作错误的可能性,尽量减少开放性手动处理步骤,合理化工艺流程,减少产品污染的机会,例如使用商业上可用的GMP级培养袋,连接器和附件;标准化输入细胞用原材料;和清楚确定的辅助试剂。工艺控制除了简化多步骤生产工艺例如,通过自动化和工艺简化将减少变异性,促进QC和放行测试,并帮助企业努力实现符合CGMP的产品。
基本上,基因治疗应该超过现有治疗方法的疗效,并为满足新的医疗需求提供治疗策略。但是,它不是一个独立的技术。天然病毒载体本身可以是治疗剂,但它们也可用作关键投入以制造快速出现的治疗平台包括CAR-T和其他形式的基因修饰的全细胞疗法。因此,预测未来生物制药对病毒载体的需求是一个挑战。然而,至少,生物工艺团体必须为自己做好准备,以满足“纯”基因疗法和研发中的过继免疫治疗图1和2的需求。最终,这将包括扩展的先进技术,例如规律成簇的间隔短回文重复CRISPR,CRISPR相关蛋白9 Cas9和锌指核酸酶ZFN以及新的临床适应症和它们指向的市场。为了确保有效的临床转化和商业化,生物高院长团体必须致力于载体生产的可扩展性。解决方案包括灵活设施管理中的流程调度,应用工艺分析技术PAT以最大化工艺控制,并支持QA技术的创新以减少其对CoG的影响。
参考文献:
David A. Brindley, Kim Bure, Maya Fuerstenau-Sharp, David Pettitt, James Smith and Jamie Ware.Scalable Purification of Viral Vectors for Gene Therapy: An Appraisal of Downstream Processing Approaches.
Monday, February 13, 2017
识别微信二维码,添加生物制品圈小编,符合要求即可有机会进入生物制品圈微信交流群
!
注明:姓名+研究方向!


版权为生物制品圈所有。欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容
须获得授权
且在醒目位置处注明“转自:生物制品圈”。









