8月30日,FDA正式批准诺华CAR-T疗法 Kymriah(tisagenlecleucel,CTL-019)上市,用于治疗儿童和年轻成人(2~25岁)的急性淋巴细胞白血病(ALL),FDA的这一决定比预定的审批期限提前了1个月(见:
里程碑!10:0全票通过,诺华CAR-T疗法获FDA专家一致推荐批准
)。
Kymriah被FDA
明确定性
为以细胞工程为基础的基因治疗产品
,
是FDA批准的第一个基因治疗药物。诺华将Kymriah的价格定为治疗一次
47.5万美元
。
特别值得指出的是,FDA将细胞因子突释综合征(CRS)列为 Kymriah的黑框警告,提供了风险评估与减轻策略,同时提供一种对抗CRS的有效解决方案——来自罗氏的Actemra(
tocilizumab
,IL-6R单抗)。为此,FDA甚至还直接扩大批准了tocilizumab的适应症,用于对抗2岁以上患者接受CAR-T治疗后产生的严重或威胁生命的细胞因子突释综合征。
tocilizumab之所以被发现能够对抗CAR-T引起的CRS,需要归功于费城儿童医院的
Stephan Grupp
教授。
Stephan教授作为CTL-019项目的临床开发负责人,在小女孩儿Emily Whitehead接受CTL-019治疗发生严重CRS而命垂一线的时候,与团队成员不分昼夜地寻找解决方案。在团队讨论的时候,很偶然地听闻一位医生自己家的孩子因为关节炎使用tocilizumab能够控制细胞因子释放,从而决意在Emily身上尝试一下,并最终挽救了她的生命,让
Emily
成为了lucky girl,也为CTL-019的成功上市奠定了基础。
11月17日,
Stephan Grupp
教授将亲临上海,在
2017国际细胞治疗上海峰会
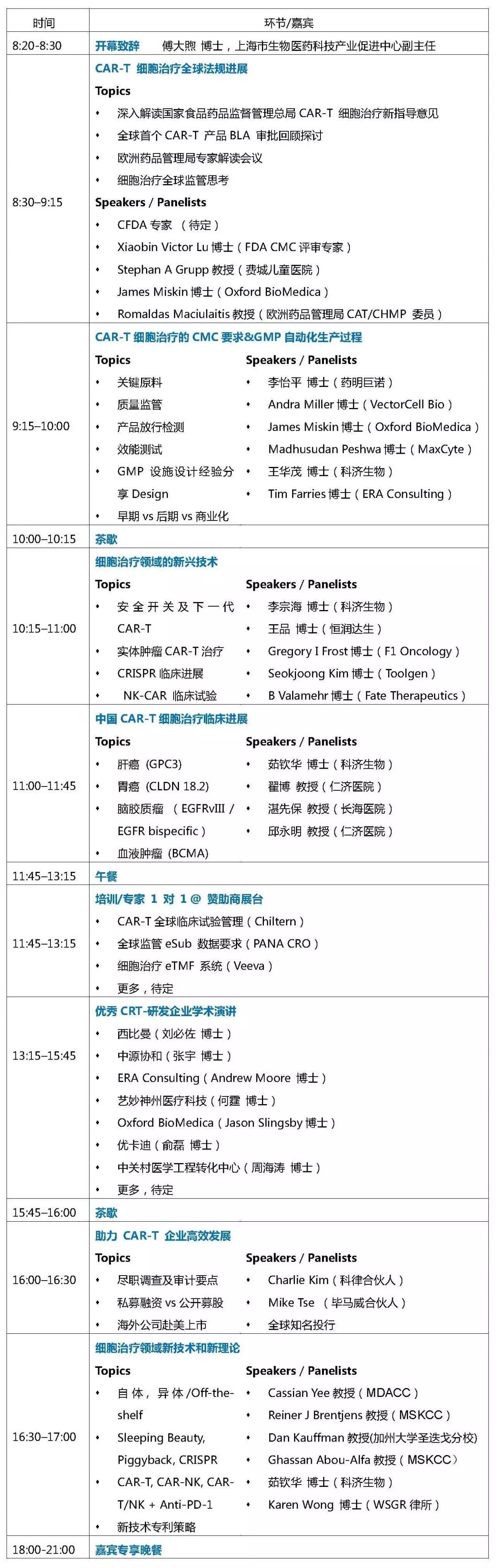
就CAR-T疗法的临床开发相关问题进行主题分享。本次峰会同时邀请了30多位国际顶级的CAR-T专家和临床KOL、三大药监机构审评专家、知名企业C-level高管、顶级律所专利律师,将从技术、生产、监管、知识产权、企业融资发展等各个角度为大家带来精彩主题分享。会议具体信息如下:
Xiaobin Victor Lu
博士,
FDA 生物制品评价和研究中心CMC评审专家,
FDA肿瘤药物咨询委员CTL-019项目CMC演讲专家
Romaldas Maciulaitis
教授,
欧洲药品管理局CHMP委员会成员,
立陶宛健康科学大学临床药理学教授
Stephan Grupp
教授,
美国费城儿童医院肿瘤免疫治疗&细胞治疗主任,
诺华CTL-019项目临床开发主要负责人
Reiner Brentjen
s
博士,
纪念斯隆·凯特琳癌症中心细胞治疗主任
Cassian Yee
博士,
美国德克萨斯州大学MD安德森癌症中心肿瘤免疫治疗研究/实体瘤细胞治疗中心主任
Ghassan Abou-Alfa
博士
,
纪念斯隆·凯特琳癌症中心消化道肿瘤专家
Dan Kaufman
教授,
加州大学圣迭戈分校细胞治疗转化医学主任
何霆
博士,艺妙神州医疗科技创始人、董事长 & CEO
J
ames Miskin
博士,Oxford BioMedica首席技术官,
FDA肿瘤药物咨询委员会CTL-019项目报告专家
Jason Slingsby
博士,
Oxford BioMedica商务发展负责人
Gregory I. Frost
博士,
F1 Oncology创始人
M. V. Peshwa
博士,
MaxCyte执行副总裁、首席科学官
Bahram Valamehr
博士,
Fate Therapeutics 副总裁
Andra Miller
博士,
VectorCell Bio总裁
Tim Farries
博士,
ERA Consultin药政总监
Ji Woong,
韩国KTB Network团队领导
Seokjoong Kim,
ToolGen
商务总监
刘昕
博士,
GREATER PACIFIC
中国区负责人
Charlie Kim
博士,
Cooley合伙人
时间:2017年11月17日
地点:上海市浦东新区世纪大道88号金茂君悦大酒店
报名及赞助事宜,请联系医药魔方(微信号:newdrug_bug)


-
点击“阅读原文”,提交个人参会信息。如需开具发票,请同时提交开票信息。
-
选择上述任意一种付款方式缴纳会议注册费(
需要开具发票的用户,务必以公对公银行转账形式的完成付款。
)
-
会务组收到你的注册费之后,以邮件形式确认您报名成功。
-
发票在会议签到处现场领取。
-
如有报名参会、企业赞助、媒体合作等问题咨询,请联系医药魔方(
微信号:newdrug_bug
)
对此次会议感兴趣的用户,可识别二维码加入微信群——细胞治疗峰会交流群






