 来源| 生物探索
来源| 生物探索
编辑| 飞过海
编者按:
6月27日,来自美国Dana–Farber 癌症研究所的4位科学家在Nature Reviews Clinical Oncology上发表了题为“Monitoring immune-checkpoint blockade: response evaluation and biomarker development”的综述。
本综述正文部分分了两大模块,第一部分内容介绍了免疫相关响应的评估策略这一关键概念:免疫相关响应标准(immune-related response criteria,irRC),由于免疫检查点抑制疗法引发了独特的抗肿瘤机制,因此,使用这类药物的患者可能会产生传统的肿瘤响应标准(tumour-response criteria,如WHO标准、实体瘤响应评估标准(RECIST))中没有包含的肿瘤响应模式。
在正文的第二部分,作者们汇总了迄今为止被研究过的数种免疫响应相关的生物标志物,并讨论了它们的优缺点。
前 沿
免疫检查点阻断疗法发挥抗癌作用是通过激活抗肿瘤免疫反应。其中,T细胞在对抗癌症的免疫防御机制中扮演着重要角色:它们识别肿瘤抗原,然后被激活、传播,最终消灭癌细胞。事实上,T细胞的激活受T细胞、树突状细胞、肿瘤细胞和肿瘤微环境(TME)中巨噬细胞上配体-受体(ligand– receptor)相互作用的调节。这些受体-配体对(receptor–ligand pairs)被称为免疫检查点。图1汇总了参与调节抗肿瘤免疫反应的免疫检查点分子。
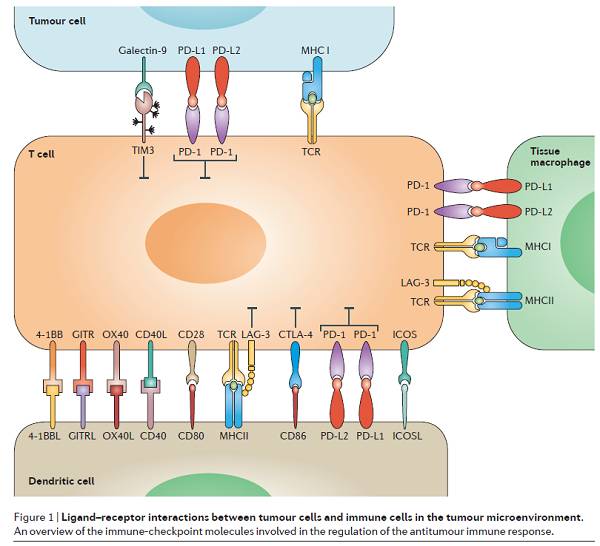
参与调节抗肿瘤免疫反应的免疫检查点分子汇总,来源《
Nature Reviews Clinical Oncology
》
目前,美国FDA已经批准靶向CTLA-4、PD-1、PD-L1三个免疫检查点的多款单克隆抗体上市。作者们认为,在临床肿瘤学实践中,免疫检查点阻断疗法的应用范围正在迅速扩大。随着新药的获批,这一趋势将继续增长。
然而,不可忽视的是,目前,只有少部分患者能够响应这种革命性的疗法。以至于目前免疫治疗领域有两大热门研究方向。一方面,科学家们在想尽各种办法,试图扩大响应人群,让更多的患者能够获益于这类疗法;另一方面,他们也在积极研究能够预测患者对免疫检查点抑制剂响应能力的生物标志物,希望能够实现精准的免疫治疗。
一.免疫相关响应的评估(Immune-related response evaluation)
由于免疫检查点抑制疗法引发了独特的抗肿瘤机制,因此,使用这类药物的患者可能会产生传统的肿瘤响应标准(tumour-response criteria,如WHO标准、实体瘤响应评估标准(RECIST))中没有包含的肿瘤响应模式。
举例来说,在用免疫检查点抑制剂治疗的一小部分患者中,响应可能在肿瘤负担初始增长后(after an initial increase in tumour burden,图2)或者新病变出现时或出现后(during or after the appearance of new lesions,图3)才被检测到。根据WHO标准和RECIST,这些事件将被归类为肿瘤进展,也被称为“假性进展”(pseudoprogression)。在假性进展的情况下,成像所检测到的肿瘤体积的增加被认为是T细胞浸润(免疫激活的结果)导致的,而不是由肿瘤细胞增殖引起的。
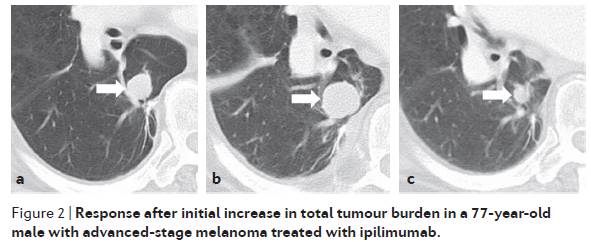 来源《Nature Reviews Clinical Oncology》
来源《Nature Reviews Clinical Oncology》
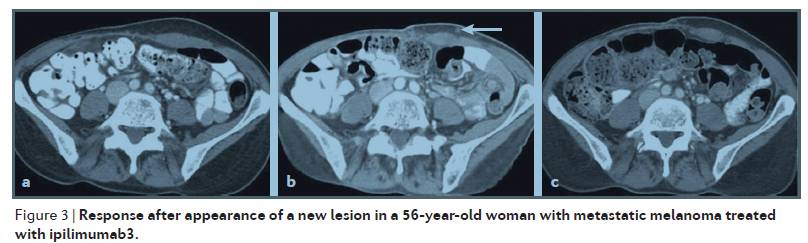 来源《Nature Reviews Clinical Oncology》
来源《Nature Reviews Clinical Oncology》
为了准确评估这些免疫相关响应,200名肿瘤学家、免疫疗法专家和监管专家举办了一系列研讨会,并在2009年提出了irRC的提议。irRC最先被用于CTLA-4抗体ipilimumab的一项II期临床试验中。现在,这一概念已经在免疫检查点抑制剂后续的临床试验中得到应用。
很明显,irRC是一个非常重要的概念,不过它依然存在很多不足和问题,包括肿瘤测量有关的方法问题、假性进展的定义等。作者们称,免疫相关响应评估的未来方向目前正在被积极讨论。业界希望改善irRC的缺陷和局限性。该部分内容提出了一些改进的方向。
二. 免疫疗法响应生物标志物(Biomarkers of immunotherapy response)
尽管在过去的十年里,免疫疗法的临床应用取得了显著成功,但是这些疗法的疗效在不同的患者和不同的肿瘤类型之间有很大的不同。现在,这一领域急需解决的问题是,开发能够预测患者对免疫疗法药物响应的生物标志物。这对响应率低的肿瘤的治疗尤其重要,如非小细胞肺癌(响应率≤20%)、肾细胞癌和泌尿上皮癌(两者响应率都≤30%)。
在正文的第二部分,作者们汇总了迄今为止被研究过的数种免疫响应相关的生物标志物,并讨论了它们的优缺点(图4)。具体来说,作者们分7类进行了总结,具体如下:
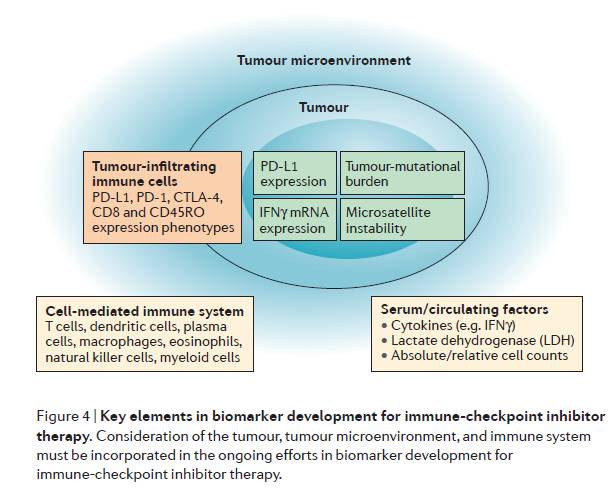
来源《Nature Reviews Clinical Oncology》
1.PD-L1和其它免疫检查点分子(PD L1 and other immune-checkpoint molecules)
将肿瘤细胞上PD-L1的表达水平作为免疫检查点抑制疗法的潜在生物标志物的研究在这类疗法发展的早期就已经开始了。下表是作者们汇总的一些相关临床试验结果。该部分内容讨论了将PD-L1作为生物标志物的合理性以及存在的一些问题。
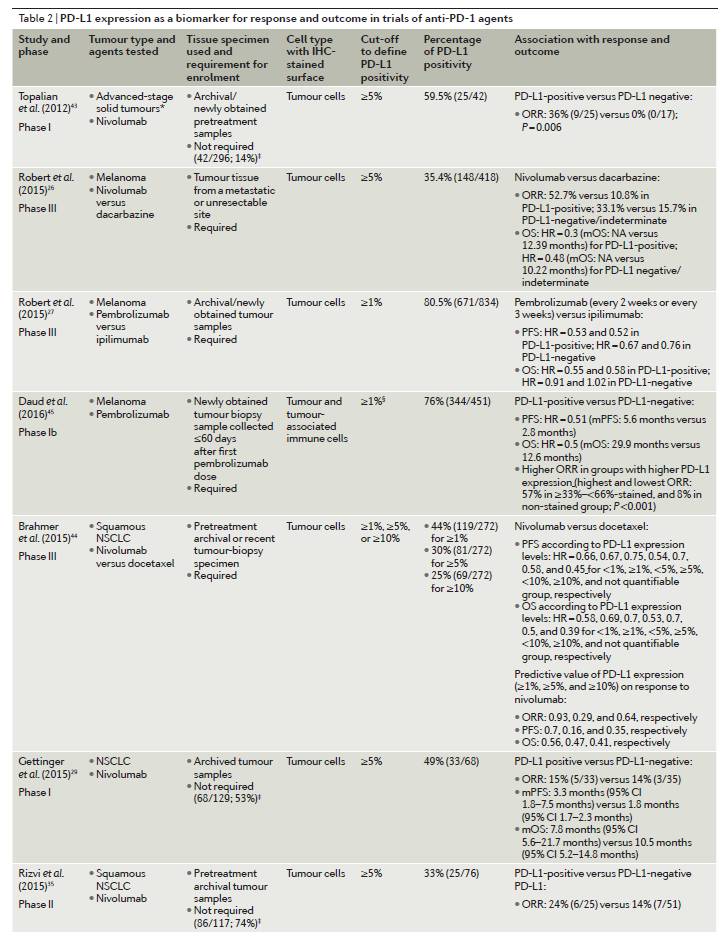
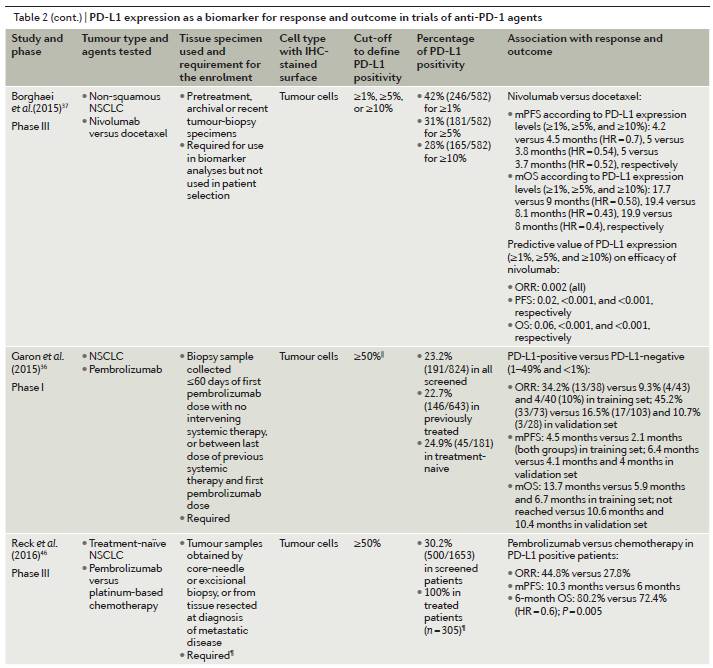
来源《Nature Reviews Clinical Oncology》
2.肿瘤浸润淋巴细胞(Tumour-infiltrating lymphocytes,TILs)
肿瘤内存在不可忽略数量的非肿瘤细胞。其中,肿瘤浸润淋巴细胞越来越被认为是抗癌免疫反应的重要参与者。大量的研究表明,TILs数量的增加与恶性肿瘤患者更好的治疗结果和更长的生存期有关。文章列举了大量相关的研究进展。作者们强调要进一步研究TILs的作用。
3.免疫得分作为生物标志物(The ‘immunoscore’ as a biomarker for immunotherapy)
免疫细胞分散在肿瘤的核心和边缘。研究表明,与对单个区域进行分析相比,分析TILs在肿瘤两种区域的存在提高了不同组早期结直肠癌患者生存预测的准确性。这些成果为对肿瘤核心和侵袭性边缘(invasive margin)进行免疫细胞浸润系统性的评估提供了理论基础。这种方法被称为免疫评分(immunoscore),已被建议作为描述肿瘤免疫微环境中免疫结构的一种方法。















