-
4 月受理量回落,回归去年稳定水平
-
安徽双鹤药业有限公司 4 月受理号 16 个,居本月受理号排行榜第一
-
辰欣药业申报 2 个 1 类化药,均为特殊审批
-
卫材药业治疗阿尔茨海默病药物 E2609 申报进口
-
科伦研发首个创新单克隆抗体药物 KL-A167 注射液
-
阿斯利康制药的 Tralokinumab 注射液国内首次获批临床
4 月受理量回落,回归去年稳定水平
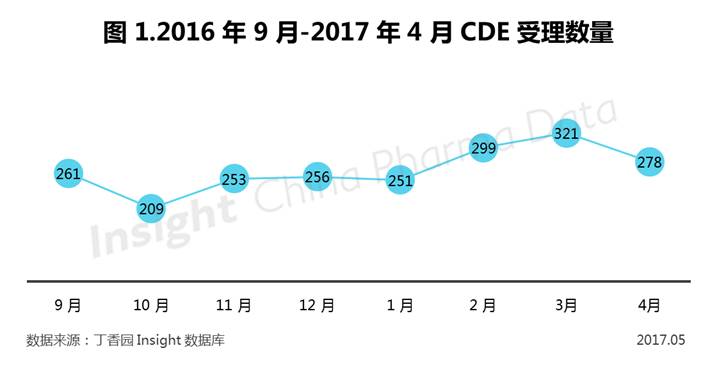
根据丁香园 Insight-China Pharma Data 数据库最新统计, 2017 年 4 月 CDE 共承办新的药品注册申
请以受理号计有 278 个,较上月有所下降,降至接近去年稳定水平后的受理量,约 260 左右
。CFDA办理状态中,本月办理状态中多了一个「在审评审批中」状态,除青岛金峰制药有限公司的复方电解质葡萄糖处于「在审批」,其余均为
「
在审评审批中」。本月上市申请共 27 个受理号、临床申请共 66 个受理号。
以下,分别来分析 2017 年 4 月化药、中药、生物制品的申报受理及审评审批情况。
一、化药
安徽双鹤
药业有限公司 4 月受
理号 16 个,居本月受理号排行榜第一
根据 Insight 数据库统计,2017 年 4 月 CDE 共承办新的化药注册申请以受理号计有 217 个,和上月基本持平。化药各序列申报受理情况如下表:
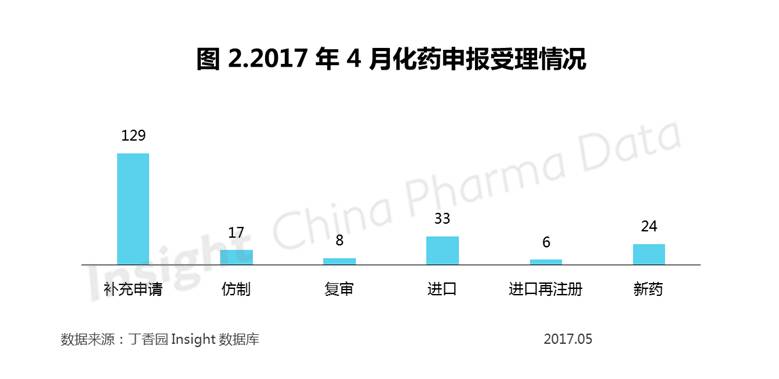
在本月 CDE 承办的新的化药注册申请的受理号中,安徽双鹤药业有限公司 4 月受理号 16 个,居药企受理号排行榜第一,其他药企 CDE 化药申报数量排名(前 15)情况如下:
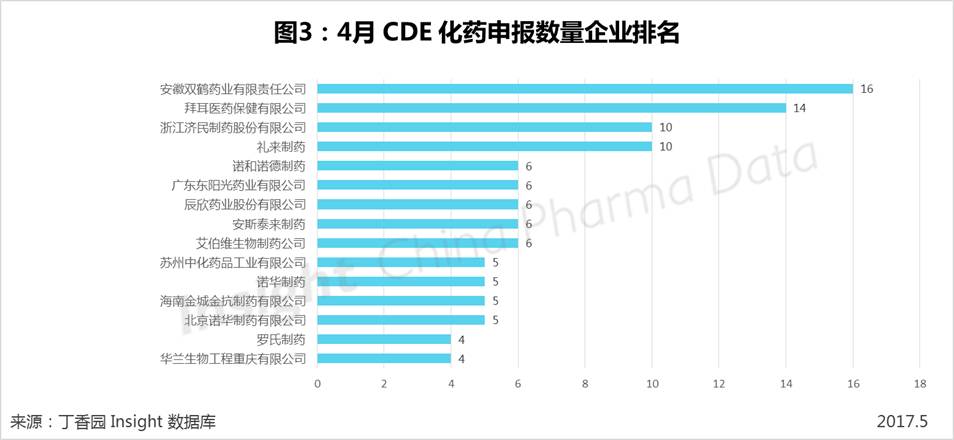
1. 新药
根据 Insight 数据库统计,2017 年 4 月 CDE 共承办化药 1 类新药申请以受理号计有23 个,涉及 10 个品种,虽较2017年第一季度的创新药申报受理品种数略微有减少,但相比去年来说仍算比较多的。
下面让我们来看 17 年 4 月申报受理的具体品种有哪些?
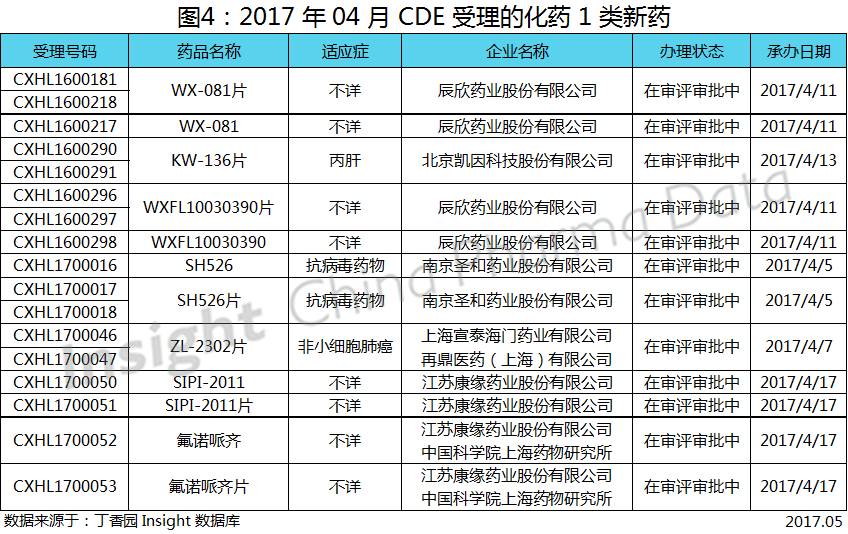
辰欣药业申报 2 个 1 类化药,均为特殊审批
辰欣药业在本月申报的两个 1 类化药,一个是 WX-081 及其片剂,受理号为 CXHL1600217、CXHL1600181、CXHL1600218;另一个是 WXFL10030390 及其片剂,受理号 CXHL1600298、CXHL1600297、CXHL1600296,这 2 个药品均为特殊审批,但目前关于这 2 款药物的相关信息还未见放出。
由上海宣泰海门药业有限公司、再鼎医药(上海)有限公司提交的 1 类新药 ZL-2302 片是一种多靶点激酶抑制剂,对野生型 ALK 克唑替尼抵抗的 ALK 基因突变均有活性。主要用于治疗肿瘤,目前主打适应症是非小细胞肺癌。
其它药物暂无消息。
2. 仿制
2017 年 4 月,CDE 共承办化药仿制药申请以受理号计共有 17 个,涉及 15 个品种,较上月减少了近半,其中按旧的 6 类申报的仿制药以受理号计有 2 个,涉及 2 个品种;按新的 4 类申报的仿制药以受理号计有 11 个,涉及 9 个品种。
按新的 3 类申报的仿制药以受理号计有 4 个,涉及 4 个品种。它们分别是:
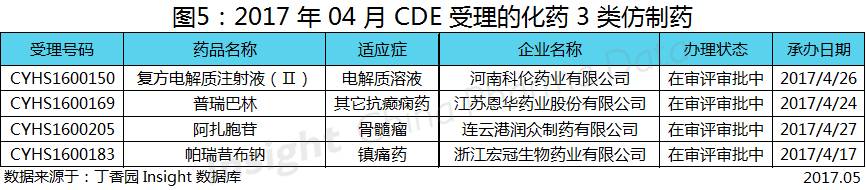
3. 进口化药
2017 年 4 月,CDE 承办新的化药进口注册申请以受理号计有 33 个,所有申请共涉及 21 个品种。其中 5.1 类申请以受理号计有 8 个,涉及 7 个品种。5.2 类申请以受理号计有 7 个,涉及 6 个品种。具体情况如下图:

卫材药业治疗阿尔茨海默病药物 E2609 申报进口
盈帆达医药咨询有限公司申报 1 类进口化药 E2609,是由卫材和百健共同研发,英文名为 elenbecestat,FDA 已授予该药品快速审批资格。本品是一种β-淀粉样蛋白裂解酶(BACE)抑制剂,用于治疗阿尔茨海默病。





