
当前,中国药企面临着仿制药质量提升、仿制药一致性评价以及全球化市场竞争环境的巨大挑战。在行业众议解决之道之时,学院以行业发展需求为导向,集全球智慧与技术资源,为中国制药行业提供一堂“高品质仿制药的研发与研发管理”系列课程;通过直面我国仿制药研发与管理的瓶颈,聚焦痛点,以科学理念与理性思维,为全面提升仿制药的研发能力提供思路和工具。
高层经理研修课程
高品质仿制药的研发及研发管理
模块3:以治疗等效为目标的注射剂研发过程与关键技术
2017/8/24-27,北京
支持单位:药物信息协会(DIA)
如何以治疗等效为目标,科学开展仿制注射剂的研发?
如何全面系统剖析原研产品信息,精准定位注射剂仿制药的研发目标?
如何基于科学知识、信息收集、风险评估及试验数据等分析,完成普通和特殊注射剂仿制药的处方和工艺开发?
如何在充分理解国内外相关临床研究技术要求的基础上,实现临床研究豁免?
如何基于注射剂产品特点,进行包材选择和相容性研究?
如何结合产品处方工艺特点,进行无菌保障?
厘清仿制注射剂研发的目标及一致性的评价标准;
理解并掌握普通和特殊仿制药注射剂研发的主要内容、基本流程、方法及工具;
理解并掌握仿制注射剂和特殊注射剂药学研究中的关键问题和关键技术;
深入理解特殊注射剂临床研究要求与豁免的科学考量;
提升解决仿制注射剂研发中常见问题的能力,丰富研发管理决策中的知识资源。
医药研发、注册和生产领域的技术人员
医药研发、注册和生产领域中高层管理者
医药市场、商务拓展和投融资领域相关人员
药品监管机构相关人员
建议有五年以上相关工作经验
理解仿制注射剂研发的目标、思路和流程,提升研发的整体规划能力;
理解普通和特殊仿制注射剂药学研究的主要内容及内在联系,提升研发方案设计的科学性和针对性;
理解特殊注射剂临床研究要求与豁免的科学考量;
通过案例分析和讨论,提升解决普通和特殊仿制注射剂研发过程中常见问题的能力。
课程主席:
陈 震 博士
郑州大学药学院教授
原国家药品审评中心药学一部负责人
具有丰富的药品技术审评经验,曾在国家药品审评中心工作,先后担任多个技术审评部、室的负责人,领导起草了十余项技术指导原则和技术标准,为推动我国药品注册技术要求的发展发挥了重要作用。
课程教授(按授课顺序):
崔 勇 博士
南京浦辰医药开发有限公司总经理
拥有丰富的药物研发及管理经验,曾在VERTEX制药公司和罗氏集团基因泰克公司制剂研发部担任组长、资深科学家;还长期担任罗氏集团--基因泰克公司的原料药晶型选择部门的负责人,是药学材料学领域的资深专家。
李又欣 博士
绿叶制药集团副总裁
“长效和靶向制剂国家重点实验室”负责人
长期从事创新药物与新制剂的研究,在新药研发尤其是长效缓释微球制剂的开发方面积累了丰富的经验,发明多种用于长效缓释微球制剂的生物可降解材料;曾在赛诺菲-安万特、UCB/Schwarz等制药公司从事新药开发工作,回国后致力于长效和靶向制剂的研究,已主持两个产品研发至临床阶段。
陈 涛 博士
西安力邦医疗产业集团有限公司董事长
西安力邦医药研究院院长
在新药研发及管理方面具有丰富经验,长期从事新型脂质体技术和脂质体药物的开发,对脂质体多肽和蛋白药物的开发等进行了广泛而深入的研究,在脂质体药品研发方面拥有数十项发明专利;曾在国外制药厂内长期担任科研部门高管并负责新药开发的研究工作。
张袁超 博士
新药研发和美国FDA药品注册法规咨询顾问
在药物开发和药品审评审批监管方面具有丰富经验。曾任辉瑞全球研发中心实验室PK/PD高级研究科学家,并曾任美国FDA高级临床药理学审评员,参与多个FDA指南的起草和修订。美国药学科学家协会(AAPS)和美国临床药理学和治疗学会(ASCPT)的成员。
马涛 总工程师
费森尤斯卡比华瑞制药有限公司
长期从事注射剂的生产质量管理、产品开发等工作,在注射剂生产质量管理和无菌保障方面具有丰富经验。曾应CFDA药品认证中心的邀请,参与我国GMP的调研与修订以及相关培训材料的编写等工作,多次参加我国药品检查员的培训交流活动。
Day 1
普通注射剂仿制药的开发:处方设计与工艺开发(崔勇 博士)
普通注射剂仿制药研发简介
原研产品的剖析
处方前研究
处方设计与优化
工艺开发
小组讨论与案例分析
Day 2
特殊注射剂仿制药的开发:注射用微球(李又欣 博士)
特殊注射剂导论
原研产品的剖析
处方前研究
注射用微球的主要质量指标
处方设计与优化
工艺开发与工艺放大
质量控制策略
Day 3
特殊注射剂仿制药的开发:注射用脂质体(陈涛 博士)
原研产品的剖析
处方前研究
注射用脂质体的主要质量指标
处方设计与优化
工艺开发与工艺放大
质量控制策略
Day 4
特殊注射剂仿制药的临床研究与豁免(张袁超 博士)
国内外对特殊注射剂仿制药临床研究的基本要求
特殊注射剂仿制药审评案例分析
特殊注射剂仿制药的临床研究豁免
注射剂的无菌保障(马涛 总工程师)
无菌保障的基本理论
常见灭菌、除菌方法及其应用
普通注射剂灭菌/无菌工艺验证
特殊注射剂灭菌/无菌工艺验证
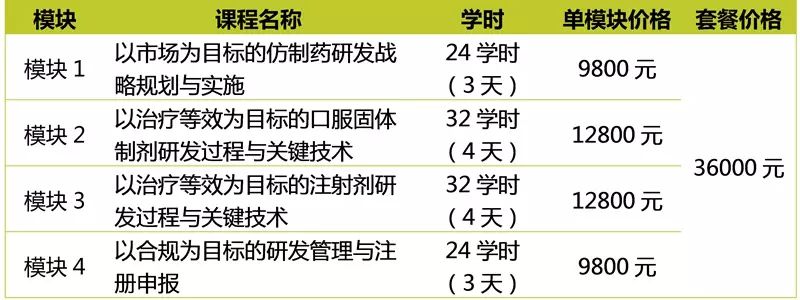 注:
注:
Early Bird:2017年7月15日前报名,单模块课程可享受限时减免800元优惠;符合条件者,可尊享“亦红包”优惠(←点击查看)
套餐优惠:四个模块同时报名,可享受超值打包价格36000元;
审评机构、一致性评价办公室、审核查验机构、药典会及药检机构人员报名,请直接联系学院工作人员。
注:优惠政策不可同享,若同时满足多种优惠条件,按最低折扣实行。
联系电话:010-65541577-836/814
电子邮箱:[email protected]
在线申请:登陆学院网页(http://www.yeehongedu.cn)在线填写申请信息并提交。
微信报名:猛戳下方阅读原文,急速报名吧!














