抗病毒药letermovir 的合成工艺改进
Improved Synthetic Process of Antiviral Drug Letermovir
张大军1,翟 鑫2,荆同飞2,邹 斌2,王 辰1
(1. 沈阳医学院化学教研室,辽宁沈阳 110034;2. 沈阳药科大学基于靶点的药物设计与研究教育部重点实验室,辽宁沈阳 110016)
摘要:
2- 甲氧基-5- 三氟甲基苯胺( 2) 与固体光气反应得2- 甲氧基-5-( 三氟甲基) 苯基异氰酸酯,不经处理直接与2-
溴-6- 氟苯胺缩合得N-(2- 溴-6- 氟苯基)-N'-[2- 甲氧基-5-( 三氟甲基) 苯基] 脲(5)。5 与丙烯酸甲酯在二噁烷中以N,N-二异丙基乙胺为缚酸剂,经Heck 偶联和Michael 加成“一锅法”合成[8- 氟-3-[2- 甲氧基-5-( 三氟甲基) 苯基] -2- 氧代-1,2,3,4- 四氢喹唑啉-4- 基] 乙酸甲酯(7),反应时间由16 h 缩短至9 h,收率由68.5%提高至79.4%。7 经三氯氧磷氯代得[2- 氯-8- 氟-3-[2- 甲氧基-5-( 三氟甲基) 苯基]-3,4- 二氢喹唑啉-4- 基] 乙酸甲酯(8)。此外,二乙醇胺经氯代、N- 烃化反应得3- 甲氧基苯基哌嗪(9)。8 与9 反应后经(2S,3S)-2,3- 双(4- 甲基苯甲酰基) 酒石酸手性拆分、水解得抗病毒药letermovir(1)。改进后的工艺总收率12.7% ( 以2 计),纯度99.7%。
关键词:
letermovir;抗人巨细胞病毒;喹唑啉;Heck 偶联;Michael 加成;工艺优化
Letermovir(1),化学名为(S)-[8- 氟-2-[4-(3-
甲氧基苯基) 哌嗪-1- 基]-3-(2- 甲氧基-5- 三氟甲基苯基) -3,4- 二氢喹唑啉-4- 基] 乙酸,是默克公司研发的治疗人巨细胞病毒(HCMV) 感染的抗病毒药物[1],于2014 年7 月进入Ⅲ期临床研究,临
床试验表明1 有望在近年获得批准上市。现有的抗
HCMV 药物( 如更昔洛韦、膦甲酸和西多福韦等)存在一些严重的不良反应( 如引起血液异常、引起肾损害以及致癌、致畸等),并出现了耐药性。而1 对HCMV 有高度的专一性,通过阻碍细胞核中的病毒DNA 装配到病毒衣壳中,从而阻止病毒复制,对耐药HCMV 病毒仍具有效力[2]。
目前1 的合成路线主要有3 条。① 2- 溴-6- 氟
苯胺(4) 与丙烯酸甲酯(6) 经Heck 偶联后,与三苯基磷反应,再经与2- 甲氧基-5-( 三氟甲基) 苯基异氰酸酯(3) 缩合、与3- 甲氧基苯基哌嗪(9) 环合烃化、手性柱拆分以及水解生成1[3]。该法在缩合反应过程中易生成含有碳二亚胺结构的活泼中间体,从而可能导致多种副产物的生成;采用手性色谱柱拆分的方法获得S- 对映体,大大提高了工业生产的成本。②以4 为起始原料,经与6 进行Heck偶联、与氯甲酸苯酯缩合、与2- 甲氧基-5- 三氟甲基苯胺(2) 进行氨解并进一步经五氯化磷消除、再与9 缩合、手性柱拆分及水解生成1[4]。该法同样会生成碳二亚胺类中间体而导致副产物较多,此外采用手性柱拆分,以及Heck 偶联时使用价昂的氯[( 三叔丁基磷)-2-(2- 氨基联苯)] 钯作催化剂,成本较高,不利于工业化生产。③以4 为起始原料,经与3 缩合得N-(2- 溴-6- 氟苯基)-N'-[2- 甲氧基-5-( 三氟甲基) 苯基] 脲(5) , 与6 进行Heck 偶联及Michael 加成“一锅法”合成环合产物[ 8- 氟-3-[2- 甲氧基-5-( 三氟甲基) 苯基]-2- 氧代- 1,2,3,4-四氢喹唑啉-4- 基] 乙酸甲酯( 7),再经三氯氧磷氯代得[2- 氯-8- 氟-3-[2- 甲氧基-5-( 三氟甲基)-苯基]-3,4- 二氢喹唑啉-4- 基] 乙酸甲酯(8),8 再与9 反应、经(2S,3S) -2,3- 双(4- 甲基苯甲酰基)酒石酸手性拆分、以及水解生成1,总收率10.5% ( 以4 计)[5]。该法经Heck 偶联与Michael 加成一步成环,缩短了反应步骤,降低了反应成本,是一种高效的一步制备喹唑啉酮的方法;且反应中间体易于制备,纯度较高,可行性强。
本研究对路线③进行了优化。1) 由于3 和9
的价格较昂贵,故本研究以价廉易得的2 为原料,与固体光气(BTC) 反应得3 后,不经分离直接与4 反应合成5;并参考文献方法,以二乙醇胺为原料,氯代后与3- 甲氧基苯胺反应合成9[6],收率
78.7%。2) 制备7 时,以二噁烷代替较昂贵的异丁
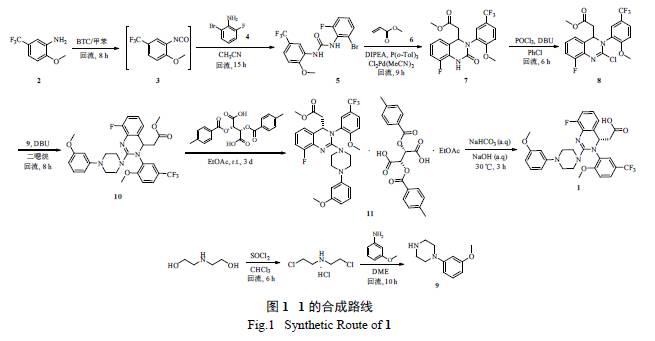
腈作溶剂,缚酸剂以N,N- 二异丙基乙胺(DIPEA)代替三乙胺,降低了反应成本,反应时间由16 h 缩短至9 h,收率由68.5%提高至79.4%。本研究原料价廉易得,成本较低,反应条件温和,总收率12.7% ( 以2 计),终产物纯度99.7%。反应路线见图1。
实验部分
N-(2- 溴-6- 氟苯基)-N'-[2- 甲氧基-5-( 三氟
甲基) 苯基] 脲(5)
[8- 氟-3-[2- 甲氧基-5-( 三氟甲基) 苯基]-2-
氧代-1,2,3,4- 四氢喹唑啉-4- 基] 乙酸甲酯(7)
[2- 氯-8- 氟-3-[2- 甲氧基-5-( 三氟甲基) 苯
基]-3,4- 二氢喹唑啉-4- 基] 乙酸甲酯(8)
3- 甲氧基苯基哌嗪(9)
[8- 氟-2-[4-(3- 甲氧基苯基) 哌嗪-1- 基]-3-[2-
甲氧基-5-( 三氟甲基) 苯基] -3,4- 二氢喹唑啉-4-基] 乙酸甲酯(10)
(2S,3S)-2,3- 双(4- 甲基苯甲酰基) 酒石酸 [8-
氟-2-[4-(3- 甲氧基苯基) 哌嗪-1- 基]-3-[2- 甲氧基-5-( 三氟甲基) 苯基]-3,4- 二氢喹唑啉-4- 基]-乙酸甲酯(1:1- 盐)(11)
Letermovir(1)
基金项目:辽宁省教育厅科学研究一般项目(L2015543)、沈阳市科
技计划创新专项基金项目(F15-139-9-02)、沈阳医学院博士科研启动基
金(2014-3057)。
作者简介:张大军(1983—),男,博士,讲师,从事创新药物及化
学仿制药研究与开发。
Tel:024-62215711
E-mail:[email protected]