
1
压焓图
1、焓
是一种能量,用来表明制冷剂所处状态的热力状态参数,它表示制冷剂所具有总能量的大小;即:
制冷剂的焓等于制冷剂内能与外能的总和(H=U+pV)。
焓用符号“
h
”或“
i
”表示,单位是“
J/kg
”或“
kJ/kg
”。
在热力学中,
焓的物理意义是指在特定温度下物质所含有的热量
。
在制冷过程中,制冷工质在系统中流动时,其内能和外功总是同时出现的,所以,引入“焓”这个状态参数,可以使热力计算得到简化:
dQ =dh
(式中
Q
为热量、
h
为焓、
d
为变量)
焓是状态参数,只与系统的初、终状态有关而与过程无关。
例如:某一制冷剂由状态
1
(含热量为
h
1
)通过吸热变化为状态
2
(含热量为
h
2
),那么,其在吸热过程中所吸收的热量(热变量)
dQ
就是吸热前与吸热后两个状态点的焓差;
即:
dQ = h
2
– h
1
,而与吸热的过程没有关系。
2、制冷系统热力计算——焓的使用
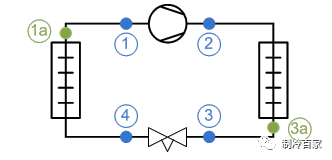
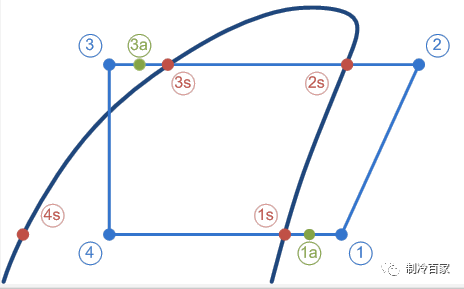
上图为某制冷系统的压焓图,再来看看这些状态点的参数:
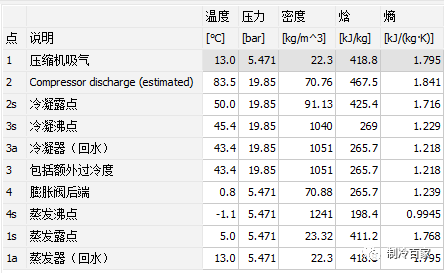
那么制冷系统的单位制冷量我们就可以算出来了:
如果有了制冷剂的流量,我们就可以计算出制冷系统的制冷量了。
2
温熵图
1、熵
是一种用来表明制冷剂所处状态的热力状态参数,用符号“
s
”表示,单位“
J/kg
·
K
”或“
kJ/kg
·
K
”。
熵所描述的是在某一温度条件下制冷剂所具有的热量。
当制冷剂吸收热量时,熵值增大;
制冷剂放出热量时,熵值减小;
制冷剂既不吸热也不放热,熵值就不会变化。
压缩机在压缩的过程,是制冷剂从低压到高压的过程,此时的制冷剂既不吸热也不放热,所以压缩机的压缩过程是一个等熵压缩的过程。
制冷剂在状态变化过程中吸收或放出的热量“
dQ
”和此时制冷剂的热力学温度“
T
”的比值,就是熵的变化量,即:
ds =dQ/T = s
2
– s
1
那么:
dQ =ds
·
T =
(
s
2
– s
1
)
T
也就是说,物质吸收或放出的热量,等于物质的热力学温度和熵的变化量的乘积。
2、制冷系统温-熵图: T-S 图
制冷系统热力循环在T-S 图上的表示:
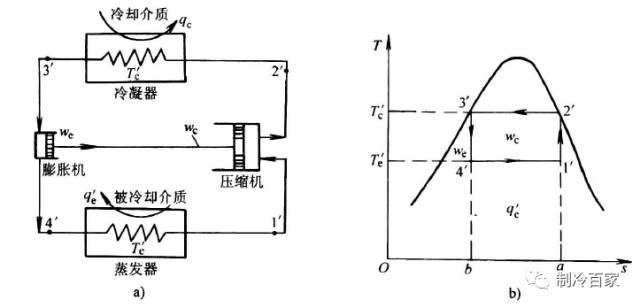
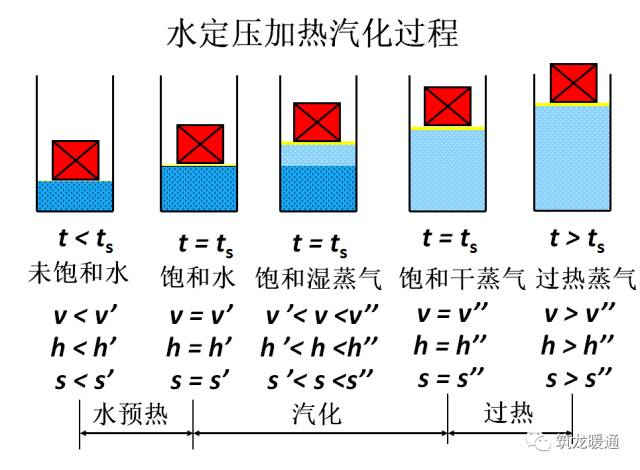
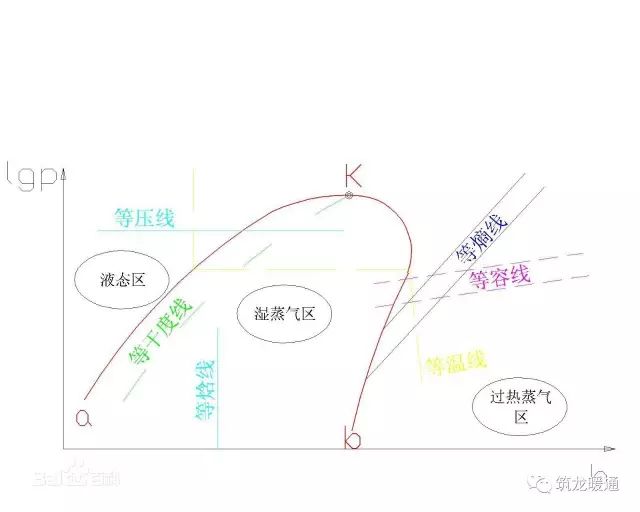
压焓图曲线的含义可以用一点(临界点)、二线(饱和液体线、饱和蒸汽线)、三区(液相区、两相区、气相区)、五态(过冷液状态、饱和液状态、过热蒸汽状态、饱和蒸汽状态、湿蒸汽状态)和八线(等压线、等焓线、饱和液线、饱和蒸汽线、等干度线、等熵线、等比体积线、等温线)来概括。
临界点K和饱和曲线
临界点K为两根粗实线的交点。在该点,制冷剂的液态和气态差别消失。
K点左边的粗实线Ka为饱和液体线,在Ka线上任意一点的状态,均是相应压力的饱和液体;K点的右边粗实线Kb为饱和蒸气线,在Kb线上任意一点的状态均为饱和蒸气状态,或称干蒸气。
三个状态区
Ka左侧——过冷液体区,该区域内的制冷剂温度低于同压力下的饱和温度;
Kb右侧——过热蒸气区,该区域内的蒸气温度高于同压力下的饱和温度;
Ka和Kb之间——湿蒸气区,即气液共存区。该区内制冷剂处于饱和状态,压力和温度为一一对应关系。
在制冷机中,蒸发与冷凝过程主要在湿蒸气区进行,压缩过程则是在过热蒸气区内进行。
六组等参数线
制冷剂的压-焓(LgP-E)图中共有八种线条:















