
文章摘要
目的:
卵巢癌是按组织学类型分类的一组不同的疾病。
随着组织型特异性治疗的发展,精确的分类将成为最佳精确药物治疗方法的关键。
实验设计:
为揭示高分级浆液性癌(HGSC)和子宫内膜样癌(EC)两种最常见的组织类型之间的差异,研究者采用新鲜冷冻的肿瘤组织(HGSC,n=10;
EC,n=10)进行了labelfree定量蛋白质组学研究。
应用免疫组化技术对361例EC或HGSC的8种候选蛋白标志物进行了验证。
结果:
500多种蛋白在EC和HGSC肿瘤蛋白质组中存在显著表达差异(p<0.05)。
免疫组化结果表明KIAA1324是最具特异性的EC新标志物。
与现行WT1+TP53标准相比,8个marker的panel能更好的区分EC和HGSC的差异,HGSC的诊断率由90.7%提高到99.2%。
EC特异性诊断标志物PLCB1、KIAA1324和SCGB2A1也与EC的良好预后密切相关,提示该组织类型具有生物学异质性。
蛋白质组数据的通路分析显示,EC和HGSC在雌激素和干扰素信号方面存在差异。
结论:
使用多个标志物集来鉴别诊断类似于EC和HGSC的疑难病例具有很好的指导意义。
主要结果如下:
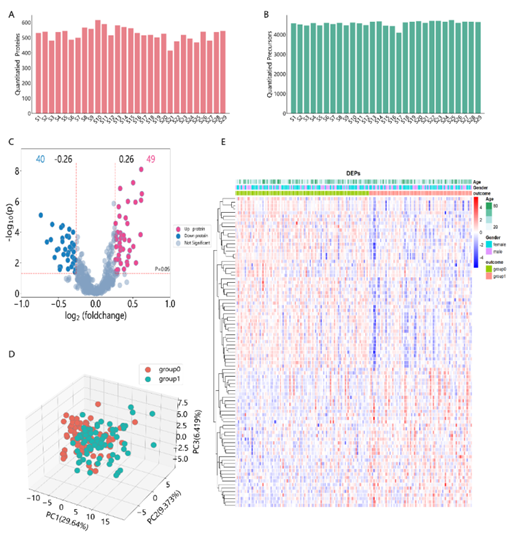
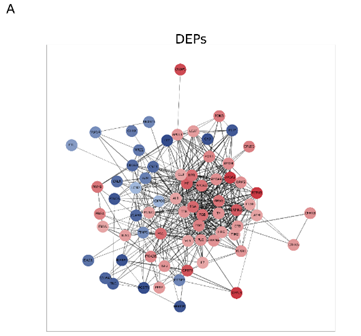
1.利用蛋白组学的技术手段对10个EC和10个HGSC样本进行检测,一共鉴定到537个差异表达蛋白,统计学分析结果如下图。
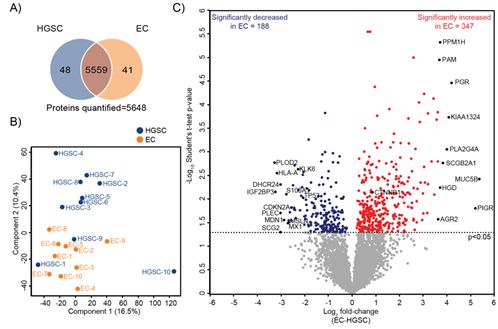
2.选取在EC中高表达的几个蛋白进行免疫组化验证,EC和HGSC有很好的区分度。
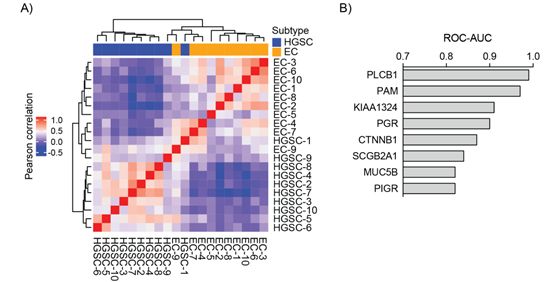
3.
在正常样本和
EC
中验证
10种差异
蛋白的表达水平,其中
PGR
和
KIAA1324
表现出很高的特异性。组合标志物能潜在的提高诊断的准确性,并且
PLCB1,KIAA1324
和
SCGB2A1
表现出很好的预后情况。
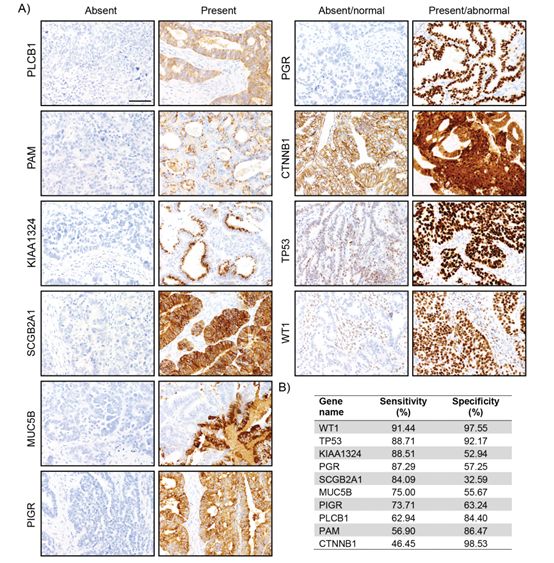
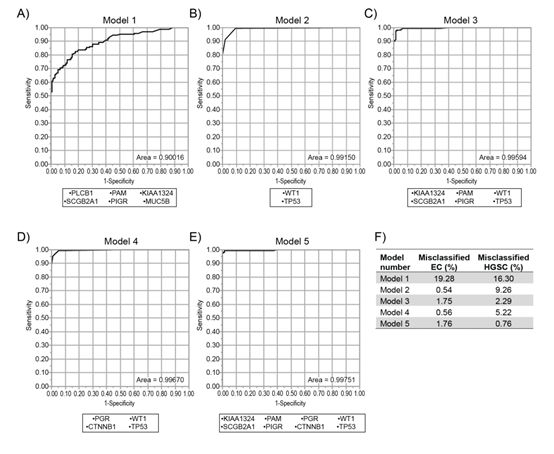
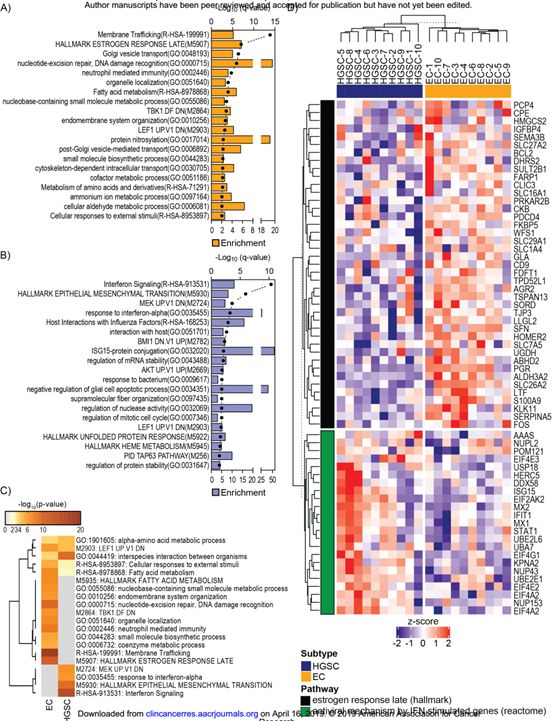
4. 生物信息学分析
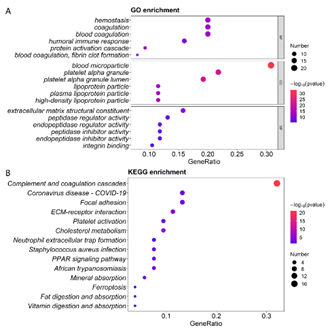
对EC和HGSC的差异蛋白参与的主要富集通路进行分析。
在(A) EC或(B)HGSC样本分析显示了前20条显著富集的通路。
(C)对显著变化的蛋白参与的生物学过程和通路进行聚类分析。
(D)显示与IFN刺激基因的雌激素反应或抗病毒机制匹配的核心蛋白的标准化(z评分)表达的热图。
越来越多的肿瘤研究在基因组学/转录组学
的基础上,同时进行蛋白组的分析。

蛋白质组学(Proteomics)是从整体水平研究细胞、组织或整个生命体内蛋白质组成及活动规律的学科。质谱技术、生物信息分析技术、人工智能技术的不断升级进步,使得蛋白质组检测技术也有了突破性的进展,并已广泛应用于生命科学研究的各个领域,特别是疾病标志物和分子机制的研究。随着我国精准医疗政策的推广,癌症和慢性疾病“早筛早诊”的观念逐渐深入人心,而目前诊断标志物的普遍缺乏,使得蛋白质组学技术迎来了蓬勃发展的新契机。
对于疾病的研究,蛋白质组学有其独特的优势。首先,蛋白质是几乎所有生命功能的直接执行者,它会随着年龄、生理活动、生活习惯和外界刺激发生相应改变,随时反映机体状况,又相对RNA和代谢物更加稳定,因此无论是发现疾病标志物还是研究疾病机理都是绝佳的研究对象。其次,蛋白质组学提供无偏见的高通量检测数据,通过科学的统计分析,可以多角度揭示分子机制,迅速筛选锁定关联因子,使得科学假设更加精准,且使研究周期大大缩短。另外,蛋白质组学研究不限样本类型(血液、唾液、尿液、石蜡切片、新鲜组织、毛发……)、不限疾病类型,对于所有的研究者来说都是有助力的研究技术。而对于有兴趣将研究成果转化的研究者来说,蛋白质因其生化检测技术成熟多样,也极具转化优势。我们还注意到,越来越多的基金申请书、高分文章都将蛋白质组学分析作为其中的重要环节,且呈现逐年递增的趋势。
要充分发挥蛋白质组学技术的优势,助力医学科研,我们不仅仅需要了解蛋白质组学的相关概念、应用场景及对应的技术,更需要掌握如何在前期进行科学合理的实验设计,选择合理的模型和样本、控制偏性、降低成本、避免弯路。
我们邀请到了临床蛋白质组学领域的资深专家团队(主持多项国家自然科学基金+顶刊文章+多项发明专利),召开“蛋白质组学助力医学科研”学习班,欢迎广大的研究人员报名参加。
2. 了解如何将蛋白质组学应用于医学研究,理清研究思路;
3. 结合流行病学基本原理,通过丰富的实操案例,掌握临床蛋白质组学实验的设计方法;
4. 掌握疾病标志物研究和疾病机制研究的常见思路,高分文章的研究策略
6. 掌握蛋白质组学数据分析的流程,看懂蛋白质组学报告,并实现关键图表的绘制;
7. 基于蛋白质相技术的2022年国自然标书整体思路框架和撰写要点。




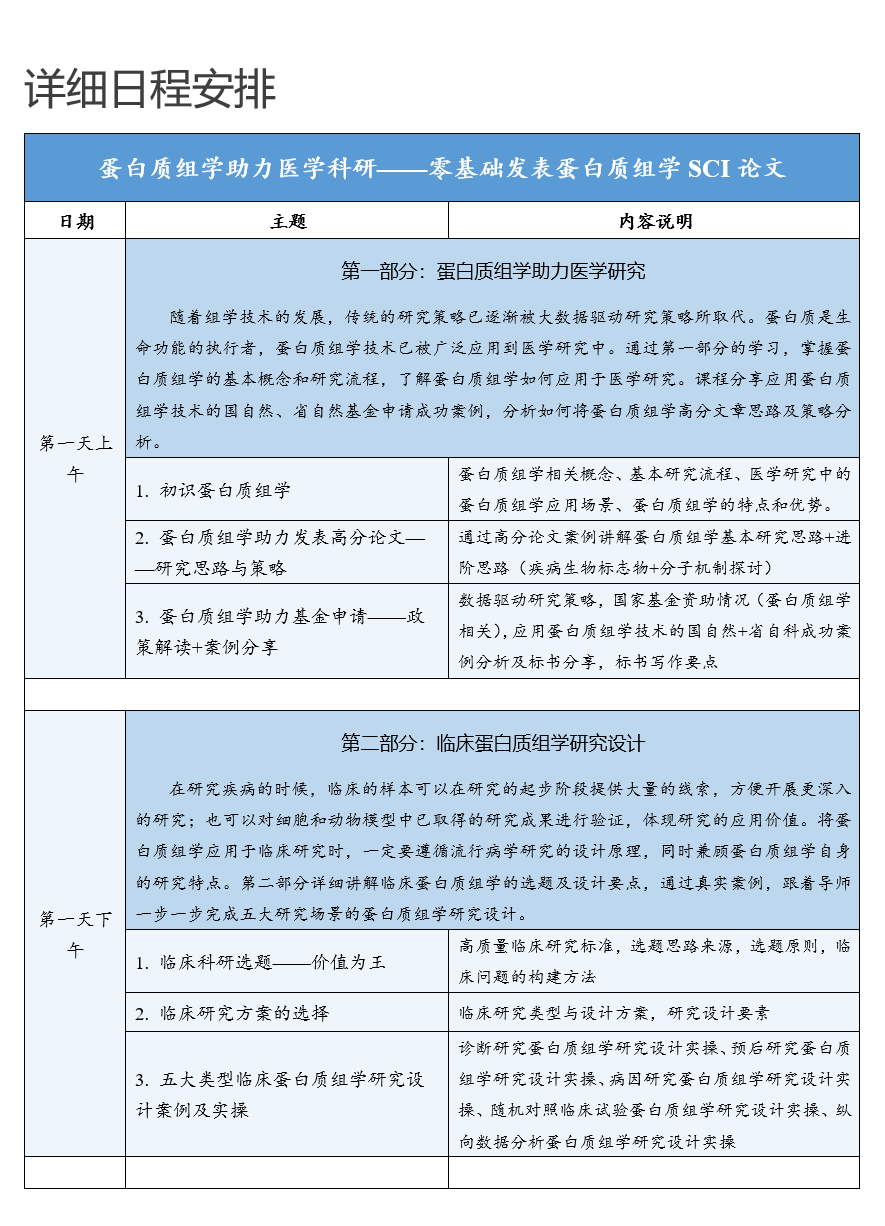

课程内容示例图

项目书立项依据分析
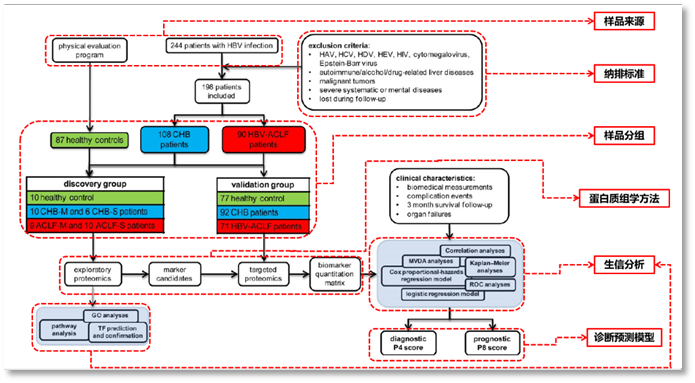
研究技术路线
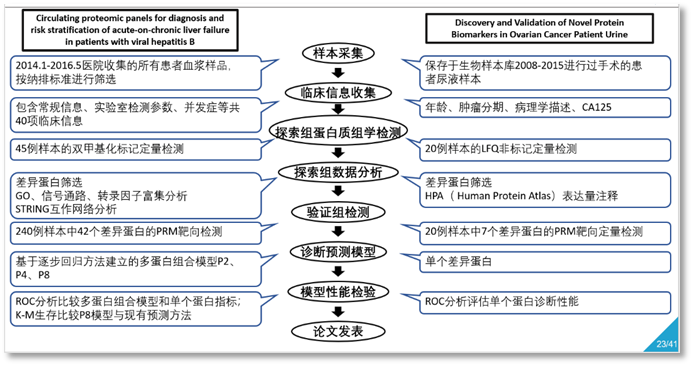
临床研究设计案例总结
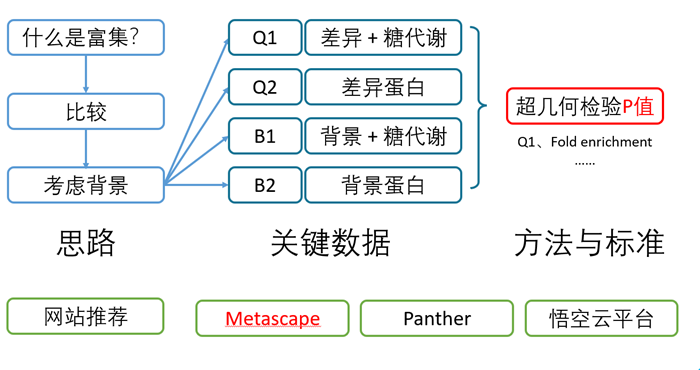
富集分析原理

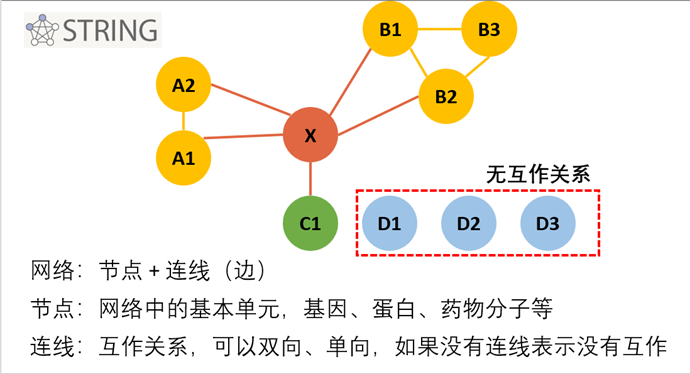
互作分析结果解读
诊断模型分析流程

蛋白质鉴定情况及差异分析
富集分析及互作网络分析
临床模型构建

模型评价
会议地点
:中兴和泰酒店 上海市浦东新区科苑路866号
联合主办方
:医药加平台与谱度众合(武汉)生命科技有限公司













