

谢立信,1942年12月12日出生于山东省莱州市,男,汉族,中共党员,中国工程院院士,一级教授、主任医师、博士生导师。1965年毕业于山东医学院,后在美国路易斯安那州立大学眼科中心从事角膜病研究,2001年当选中国工程院院士。现任山东省眼科研究所名誉所长、青岛眼科医院院长、亚太角膜病学会名誉主席、中华医学会眼科学分会荣誉主任委员。是第八、九届全国人大代表,中共十六大代表,全国劳动模范。
耐多药(MDR)细菌及其相关生物膜是眼部感染的主要致病因素,常常导致失明并带来巨大的全球健康挑战。目前,机械杀菌系统显示出很好的潜力,它结合不同的拓扑几何形状和机械力来物理诱导细菌凋亡。然而,目前的机械杀菌系统与细菌之间的物理相互作用过程通常基于被动扩散或布朗运动,缺乏生物膜穿透所需的力致使抗菌效果低。
针对此问题,来自山东第一医科大学附属眼科研究所的谢立信教授团队
受蝉翼和蜻蜓翅膀表面可机械性破裂附着的细菌细胞膜现象启发,报道了一种“靶向自热泳动机械破裂”策略,构建了一种新型机械杀菌纳米马达(称为VMSNT),用于治疗眼部MDR细菌感染。VMSNT以VMSN纳米粒子为基质合成,通过酰胺反应用羧基聚乙二醇苯硼酸(COOH-PEG-PBA)进行功能化,然后再部分修饰金纳米壳以实现高效的自热泳动。PBA 修饰的机械杀菌剂可以与细菌表面肽聚糖中的顺式二醇结构共价结合,并选择性地靶向细菌(方案1)。
相关研究成果以
“A Bioinspired Virus-Like Mechano–Bactericidal Nanomotor for Ocular Multidrug-Resistant Bacterial Infection Treatment”
为题于2025年1月14日发表在
《Advanced Materials》
上。
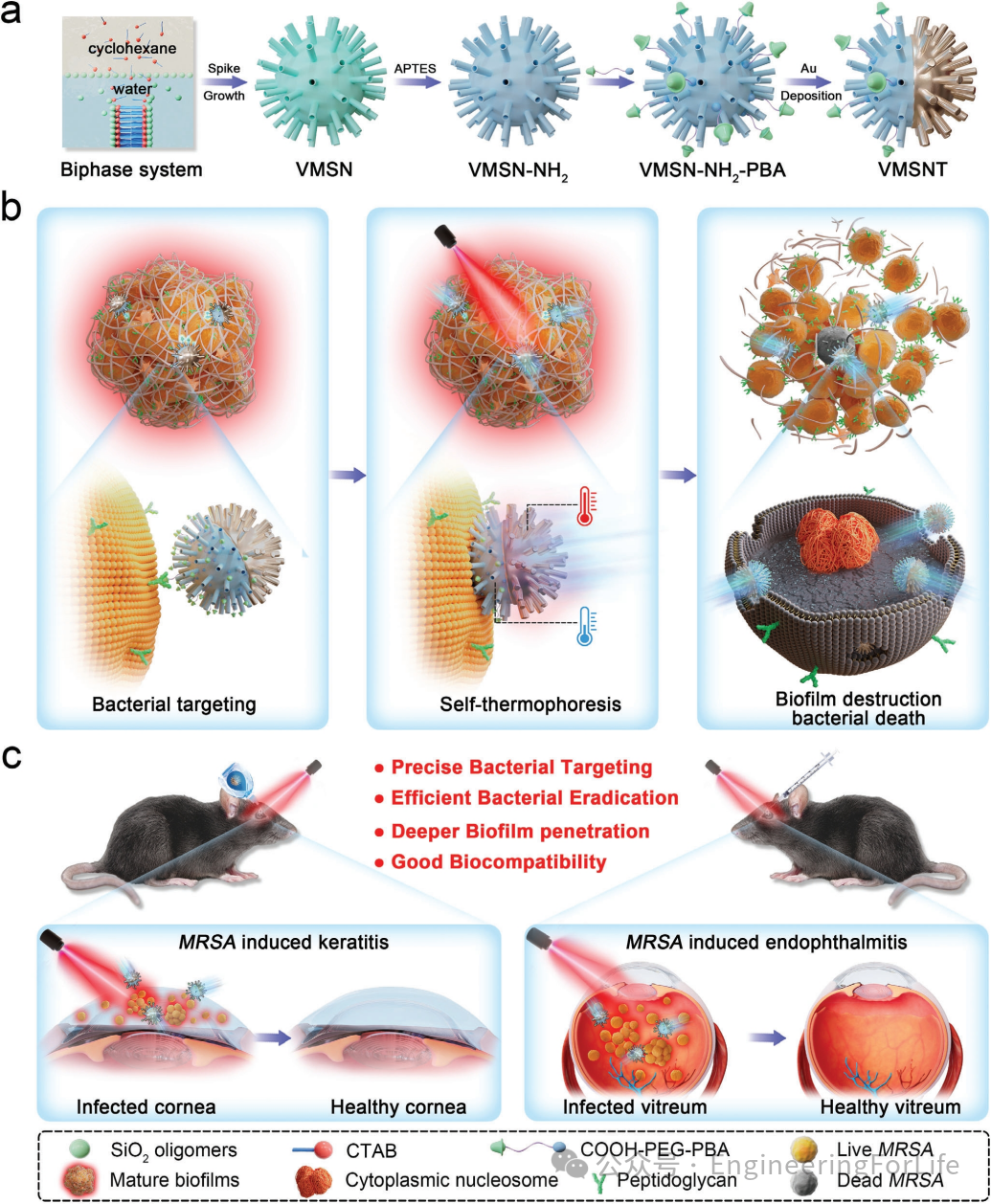
方案1 构建类病毒机械杀菌纳米马达(VMSNT)及其用于抵抗细菌感染的示意图
受益于其独特的拓扑结构和金半壳固有的光热特性,在808 nm近红外光照射下,所制备的纳米粒子可以产生更大的自热泳力和与接触细菌的更小的接触面积。因此,近红外激光有效地为VMSNT提供动力,使其物理破坏细胞膜并通过自热泳力深入渗透生物膜。通过尖刺拓扑几何形状和自热泳效应的协同作用,机械杀菌剂在消灭MDR细菌和生
物膜方面表现出高性能(方案1)。
1.VMSN的制备与表征
首先,作者展示了VMSNT的制备过程(图1)。首先,通过单胶束外延生长法在油/水双相反应系统中制备了VMSN纳米颗粒。在外延生长过程中,仅通过调节反应时间即可获得不同长度的纳米管,延长反应时间会增加纳米管的长度。透射电子显微镜(TEM)图像显示,VMSN具有均匀的球形形貌,表面粗糙且呈尖刺状(图1A)。测量表明,均匀纳米管的外径/内径和长度分别为5.2/4.3 nm和37.4 nm(图1B)。FTIR表明VMSN上成功引入了氨基,证实了材料的成功合成。图1E中的TEM图像证实了半涂覆Au层的厚度为10 nm,并集中在纳米马达的一侧。元素分析明确表明纳米粒子中存在所有预期元素,包括Au、B、N、Si和O(图1F)。
根据上述结果,构建了具有尖刺形态和在NIR光下自主运动的 VMSNT,为 MDR 细菌根除提供了先决条件
。
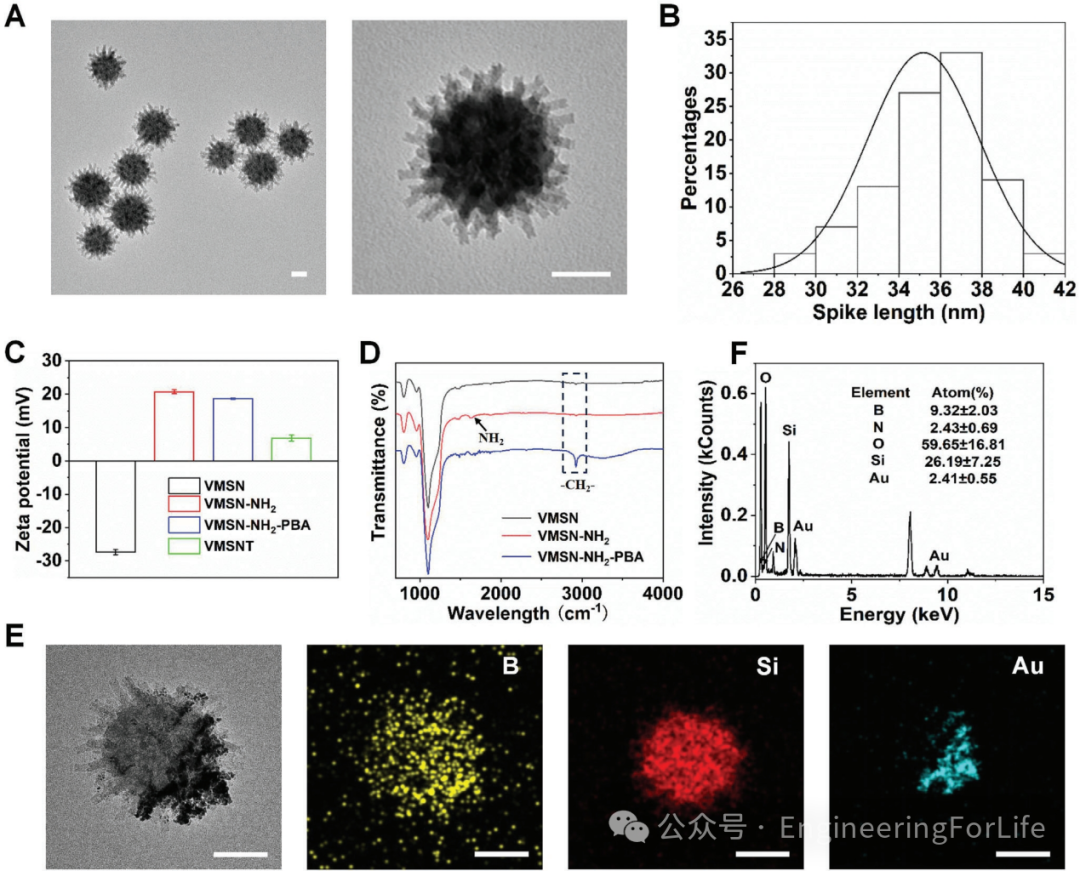
图1 VMSNT 的制备与表征
2.VMSNT的光热和运动特性
根据《美国户外激光安全使用国家标准》及实验条件和位置,作者选择了0.25 W/cm²作为NIR激光辐照的优化参数。红外热成像结果显示,NIR激光照射5分钟后VMSNT的温度从25.1 ℃升高至38.2 ℃(图2A,B)。另外,基于加热–冷却曲线及相关时间常数(图2C),得出VMSNT的光热转换效率(PCE)高达42.3%。这一优异的光热转换性能归因于VMSNT独特的刺状形貌,这些尖刺结构环绕在Au帽周围,显著增强了局部表面等离子体共振。作者还通过五次加热–冷却循环实验评估了VMSNT的光热稳定性,在此过程中未观察到性能下降,表明VMSNT具有优异的光热稳定性(图2D)
。
接下来,通过分析运动视频系统地研究了机械杀菌纳米马达的光热诱导自热泳动。图2E显示了有或没有NIR照射的PBS溶液中机械杀菌纳米马达的代表性跟踪轨迹。结果表明,VMSNT表现出优异的近红外光驱动性能,可作为抗菌治疗的机械杀菌平台(图2G-H)。
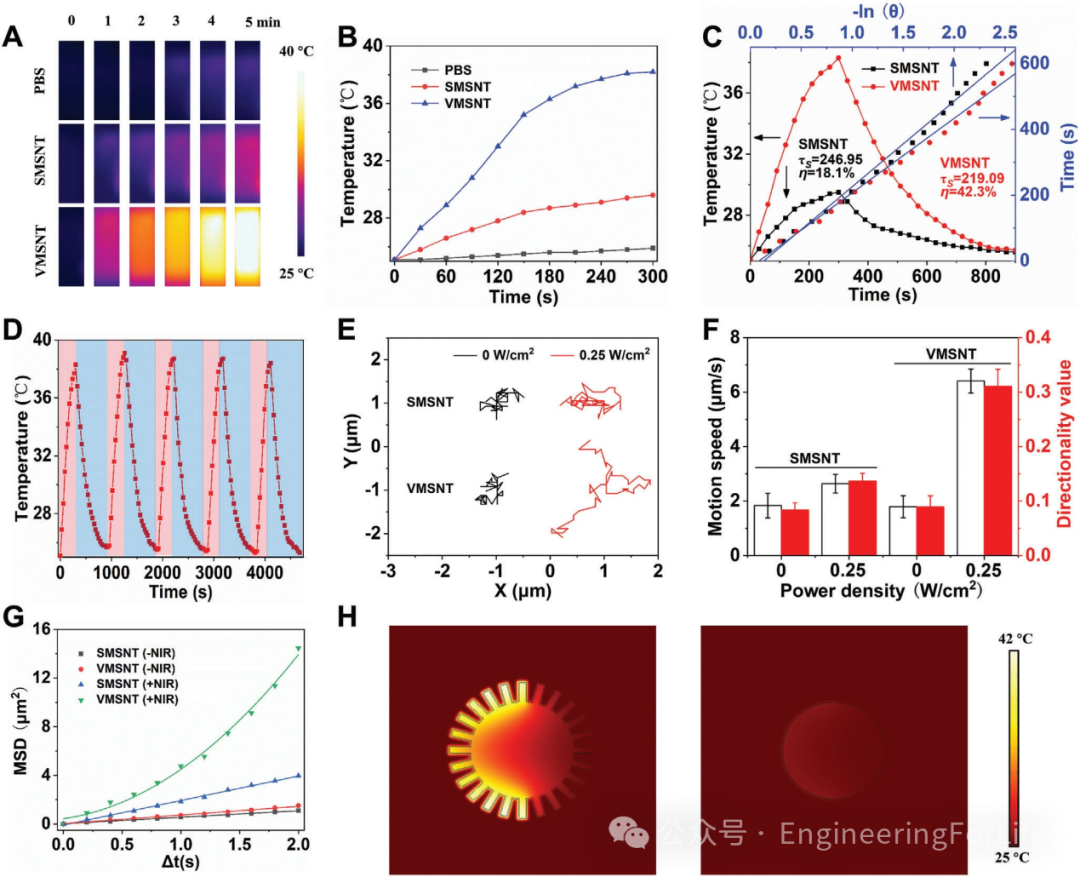
图2 VMSNT的光热和运动特性评估
3.VMSNT的细菌靶向性和生物相容性
VMSNT表面的PBA分子可以可逆地与细菌细胞壁上的肽聚糖结合,从而实现对细菌的特异性黏附。为了评估PBA识别在细菌中的关键作用,分别将革兰氏阳性菌耐甲氧西林金黄色葡萄球菌(MRSA)和革兰氏阴性菌耐多药铜绿假单胞菌(MRPA)与VMSNT和VMSN-NH
2
一起孵育。在VMSN-NH
2
组中可以观察到一些散在的纳米粒子;而大量的VMSNT附着在细菌表面,这表明结合力来自于PBA分子而不是纳米粒子的形貌(图3A)。
为了进一步探索VMSNT在体内复杂环境中对细菌的靶向能力,作者利用transwell小室模拟感染微环境。上室放置人角膜上皮细胞(HCEC);而下室放置细菌(图3B)。将罗丹明B标记的VMSNT和VMSNT-NH
2
分别加入上孔中,并进一步用NIR激光照射。荧光成像显示VMSNT处理组中的细菌中红色荧光大量积累,而VMSNT-NH
2
组没有表现出类似的富集(图3C)。这些荧光结果证实 VMSNT纳米粒子对细菌具有高度特异性的结合亲和力。
良好的生物相容性是抗菌材料长期使用的前提。为了验证VMSNT的细胞毒性潜力,作者采用了活/死细胞共染色试验和CCK-8试验。通过活/死细胞染色观察到的活细胞数量(绿色)与CCK-8试验的结果一致,进一步验证了它们优异的生物相容性。在0.25 W cm
−2
的低功率密度下,对照组(PBS)的细胞存活率不会随着照射时间的延长而发生明显变化(图3E)。值得注意的是,在VMSNT组中,当照射时间达到3分钟时,细胞活力明显下降(图3F、G)。这可能是因为VMSNT表面的照射时间越长,产生的热量就越多,从而导致细胞毒性显著增强。此外,还使用H&E染色来评估局部应用VMSNT并随后进行NIR光照射后角膜结构的变化,证实了7天局部给药期后VMSNT与小鼠角膜具有出色的生物相容性(图3H)。
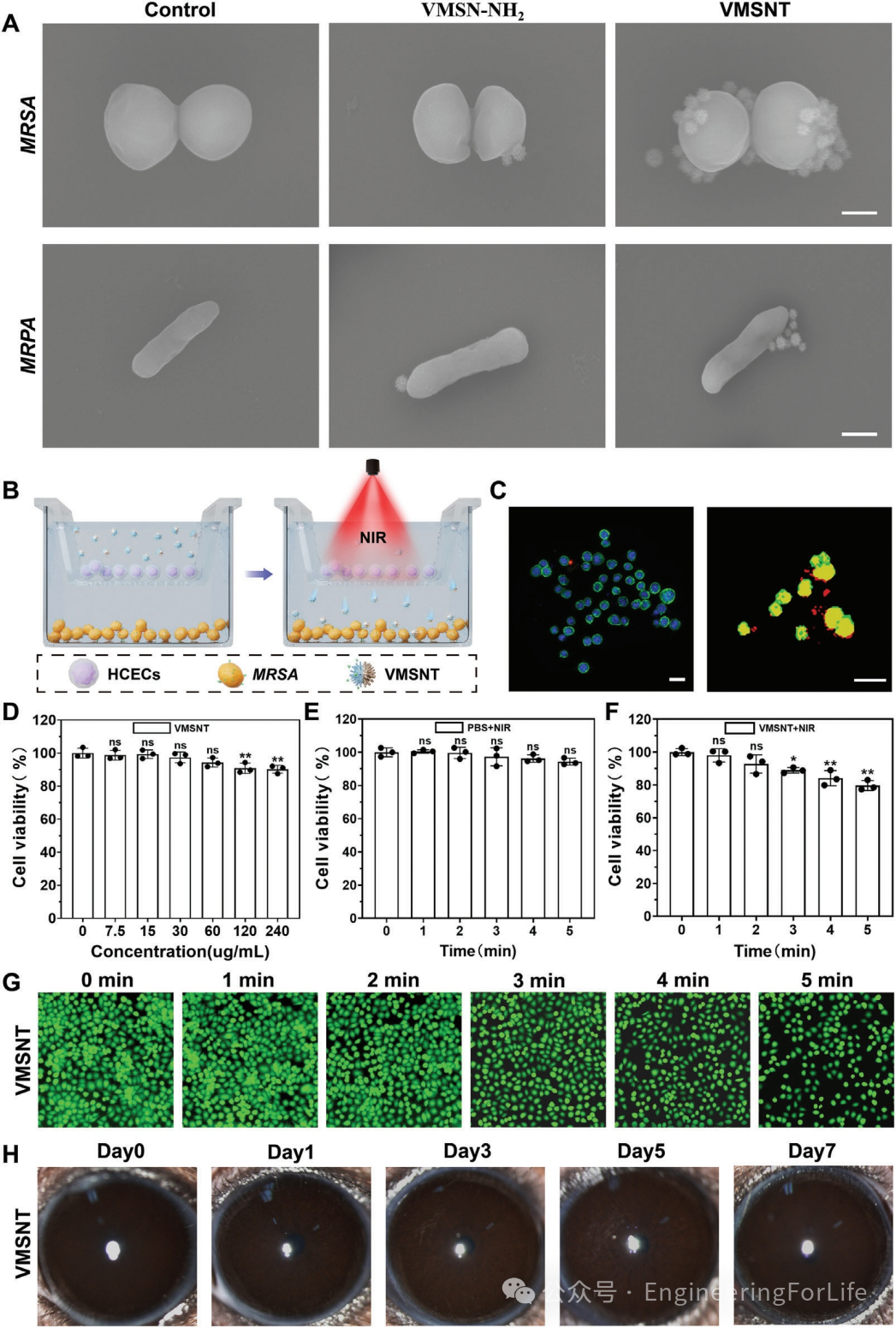
图3 VMSNT 的细菌靶向性和生物相容性
4.VMSNT的体外抗菌能力
基于设计的机械-杀菌纳米马达在光热转换与运动性能上的优异表现,其抗菌活性在耐甲氧西林金黄色葡萄球菌(MRSA)和多重耐药铜绿假单胞菌(MRPA)中进行了评估。不同浓度的VMSNT溶液与MRSA和MRPA混合后,在0.25 W cm⁻²的NIR光照射下处理3分钟。实验测得VMSNT对MRSA和MRPA的最小抑菌浓度(MIC)分别为7.5 µg/mL和15.0 µg/mL,表明其具有出色的抗菌能力
通过平板计数法和相应的存活率分析进一步证实了VMSNT的抗菌能力(图4A-B)。为了进一步评估所得纳米马达的机械杀菌能力,进行了活/死染色。如图4C所示,VMSNT 组细菌中红色荧光占主导地位,而对照组和Au-NPs组中细菌均发出强烈的绿色荧光,突显了其卓越的机械杀菌性能,与平板计数测定结果一致。
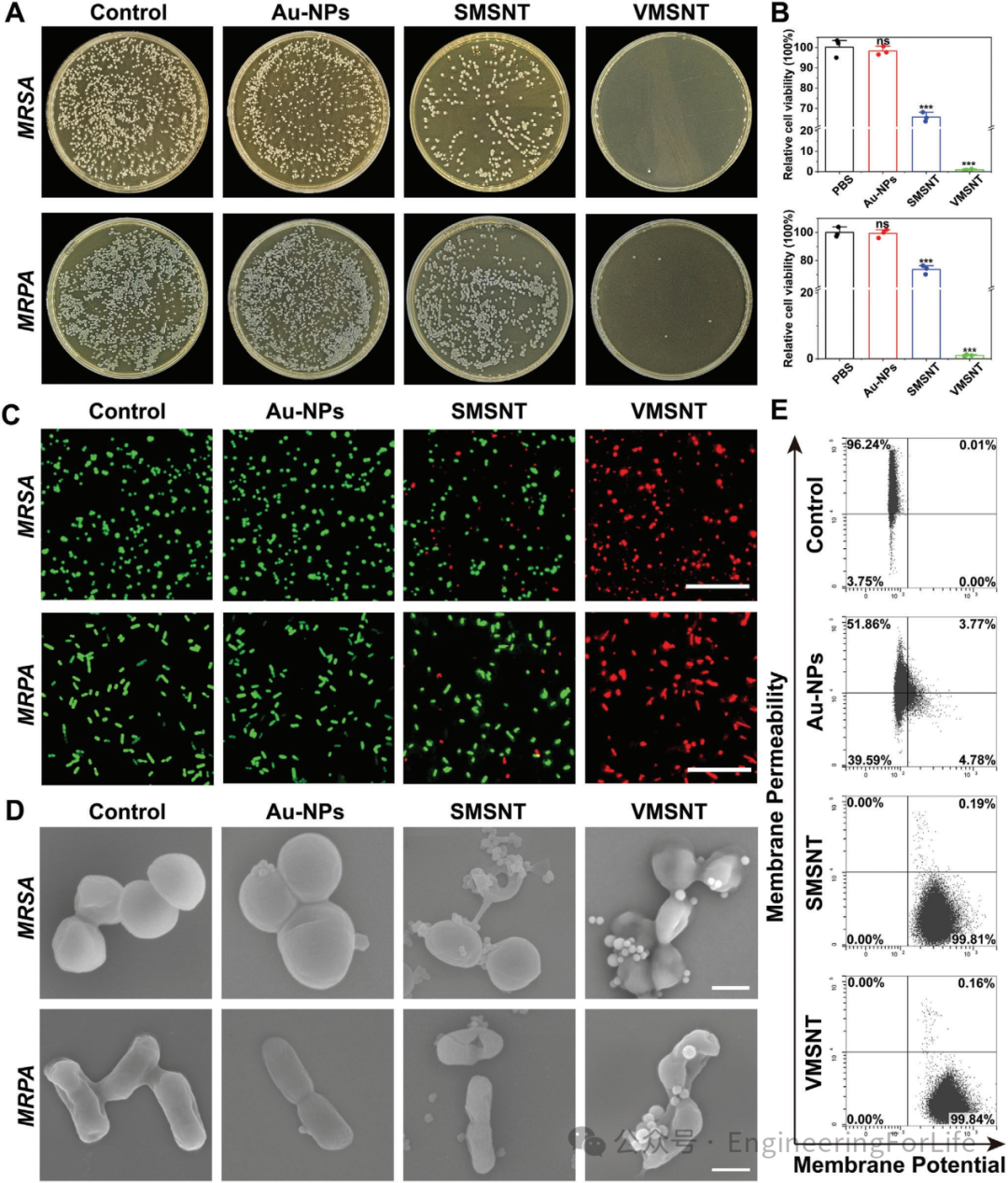
图4 VMSNT体外抗菌活性
5.VMSNT的生物膜渗透性和抗生物膜活性
对于物理清除生物膜而言,机械杀菌剂能否穿透深层生物膜是前提和关键。因此,通过CLSM成像在没有或有NIR光照射的情况下评估了罗丹明B标记的VMSNT对MRSA生物膜的渗透性。如图5A所示,在没有激光照射的情况下,有限量的VMSNT随时间的推移渗透过生物膜,证明了MRSA生物膜的屏障功能。相反,用罗丹明B标记的VMSNT处理并经激光照射的生物膜的CLSM图像在更深的生物膜层面显示出强烈的罗丹明B红色荧光,表明VMSNT在整个生物膜中有效扩散。对荧光强度的定量评估证实了这些发现(图5B)。
接下来,系统地验证了VMSNT破坏成熟生物膜的性能。图5C中的CLSM图像显示VMSNT组显示出轻微的绿色荧光斑点,厚度明显减少,表明具有优异的机械杀菌效果和有效的生物膜消除效果。在不同干预措施下测量的生物膜中的荧光强度结果相似(图5D)。
为了定性评估对生物膜的消除效果,进一步进行了SEM观察,观察结果与活/死染色试验的结果一致,证实了VMSNT在生物膜中的功效
。
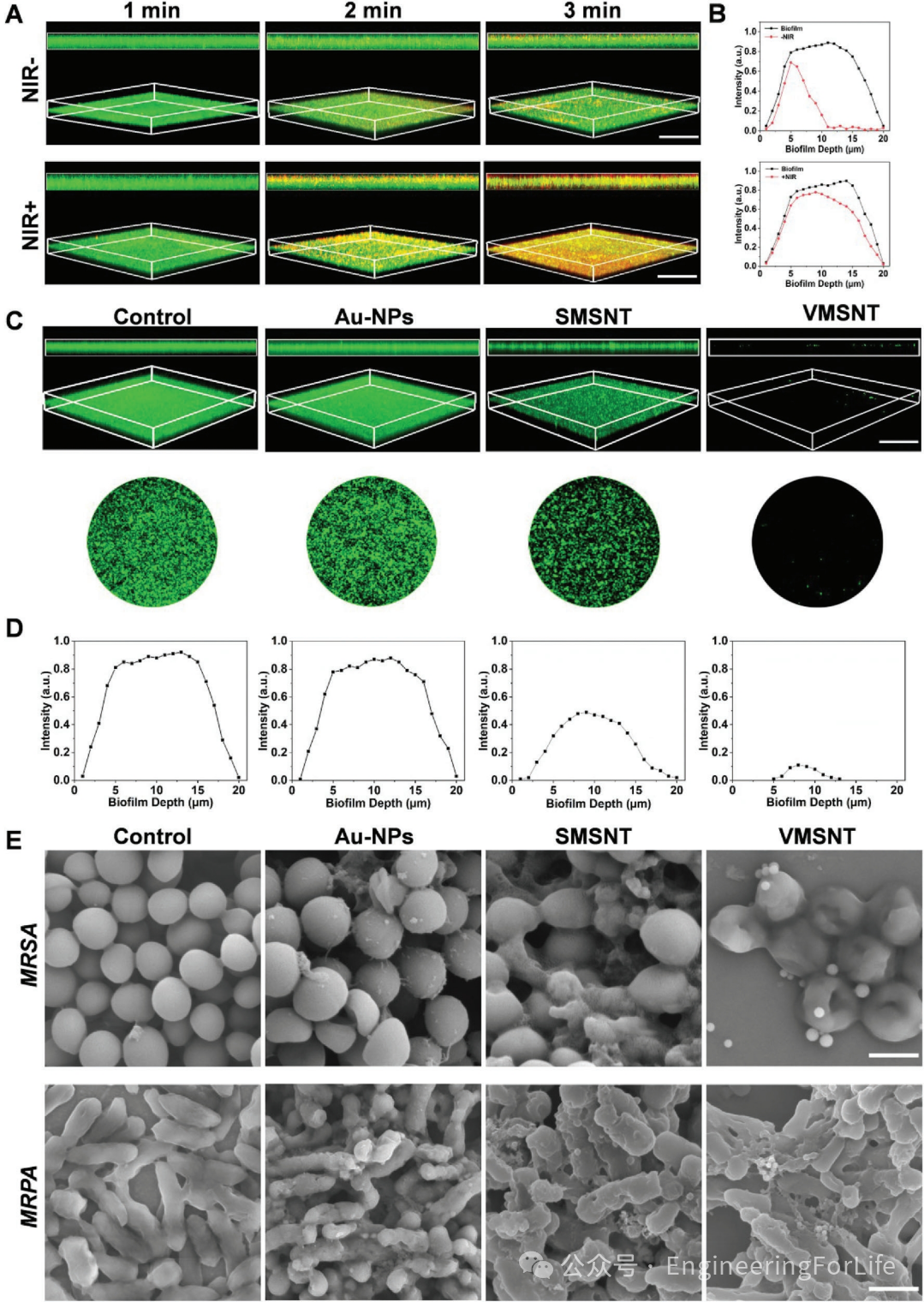
图5 VMSNT体外生物膜渗透性和抗生物膜活性
6.VMSNT的抗菌机理
为了进一步探究VMSNT的抗菌机制,我们通过原子力显微镜(AFM)测量了MRSA细胞膜的机械性能,该技术能够在近生理环境下研究活细胞的力学特性。采用穿刺实验方法,获取了细菌细胞的力–位移曲线(图6A)。结合模拟(图6B)表明VMSNT产生的阈值应力在理论上足以破裂细菌细胞膜,也解释了VMSNT优异的杀菌性能。
SMSNT通过协同作用达到了一定的杀菌效果。这一发现与抗菌实验结果是一致的,说明具有大长径比和尖端的MNRs能产生更好的机械杀菌效果
。
为了深入了解设计的机械杀菌纳米马达在信使RNA (mRNA)水平上的抗菌机制,对VMSNT处理后的MRSA进行了差异表达基因(DEG)分析。基因本体(GO)分析表明这些DEG与分子功能、细胞成分和特定生物过程相关,从而将VMSNT组与对照组区分开来(图6D)。此外,KEGG通路富集调查显示,DEG 主要存在于与氨基酸合成和代谢相关的通路中(图6E-F)。
综上所述,VMSNT可能通过机械破裂效应破坏细胞膜,削弱毒力,阻碍生物膜的形成
。
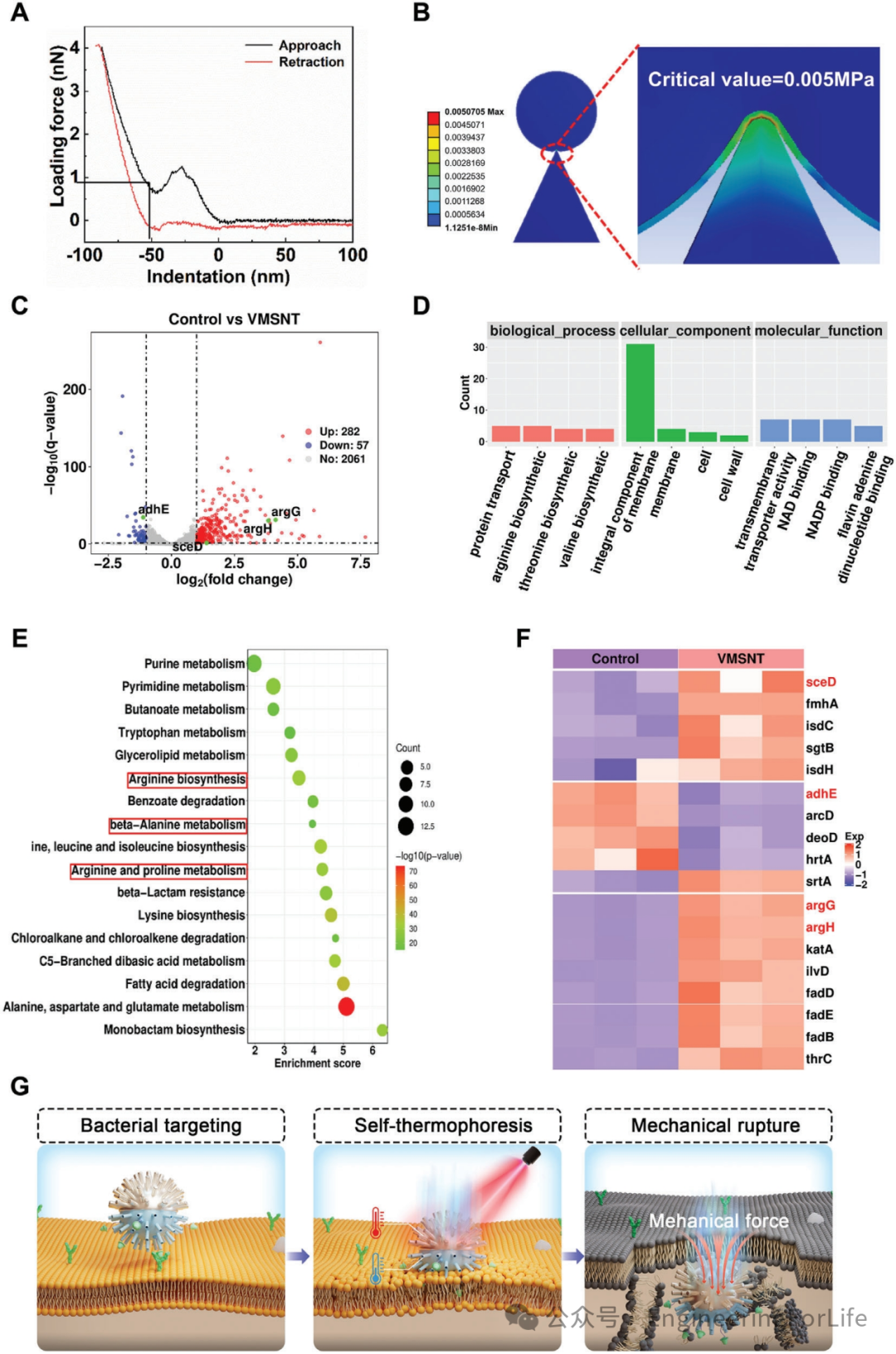
图6 VMSNT介导的细菌破裂机制
7.VMSNT在IK小鼠模型中的治疗效果
感染性角膜炎(IK)是全球视力丧失和失明的主要原因,由于细菌对药物产生耐药性的增加,恢复视力面临挑战。作者构建了IK模型,24小时后,将小鼠分成四组,每天分别局部给药PBS、Au-NPs、SMSNT和VMSNT四次。给药5分钟后,用NIR激光(808 nm,0.25 W cm
−2
)照射感染角膜3分钟,以触发机械杀菌运动以消除细菌(图7A)。
在7天的治疗期间,以不同的时间间隔监测和拍照不同组的愈合过程。PBS和Au-NPs治疗组未能对抗MRSA感染(图7B)。相反,SMSNT治疗组在7天后出现轻度缓解,表明其在一定程度上具有抗菌作用。为了定量评估机械杀菌纳米马达的抗菌活性,还通过标准甘露醇盐琼脂平板法评估了各种治疗后角膜组织中的残留细菌(图7C)。VMSNT处理并接受激光照射的角膜显示出最少的细菌菌落计数,存活率为 3.1%,说明VMSNT对IK的显着治疗作用。
此外,对不同处理后从MRSA感染角膜上切除的组织切片进行组织学分析。H&E染色图像显示在接受VMSNT治疗的组中,角膜结构保存得类似于健康对照,表明与其他治疗相比,治疗效果更有效(图7D)。对TNF-α、IL-1β和IL-6进行免疫荧光染色,以评估伤口的感染程度和愈合情况(图7E),VMSNT组TNF-α、IL-1β和IL-6显著降低。此外,利用RT-qPCR技术进一步测定各炎症介质的mRNA水平(图7F),在VMSNT治疗组中明显减少,表明VMSNT的治疗效果最好。
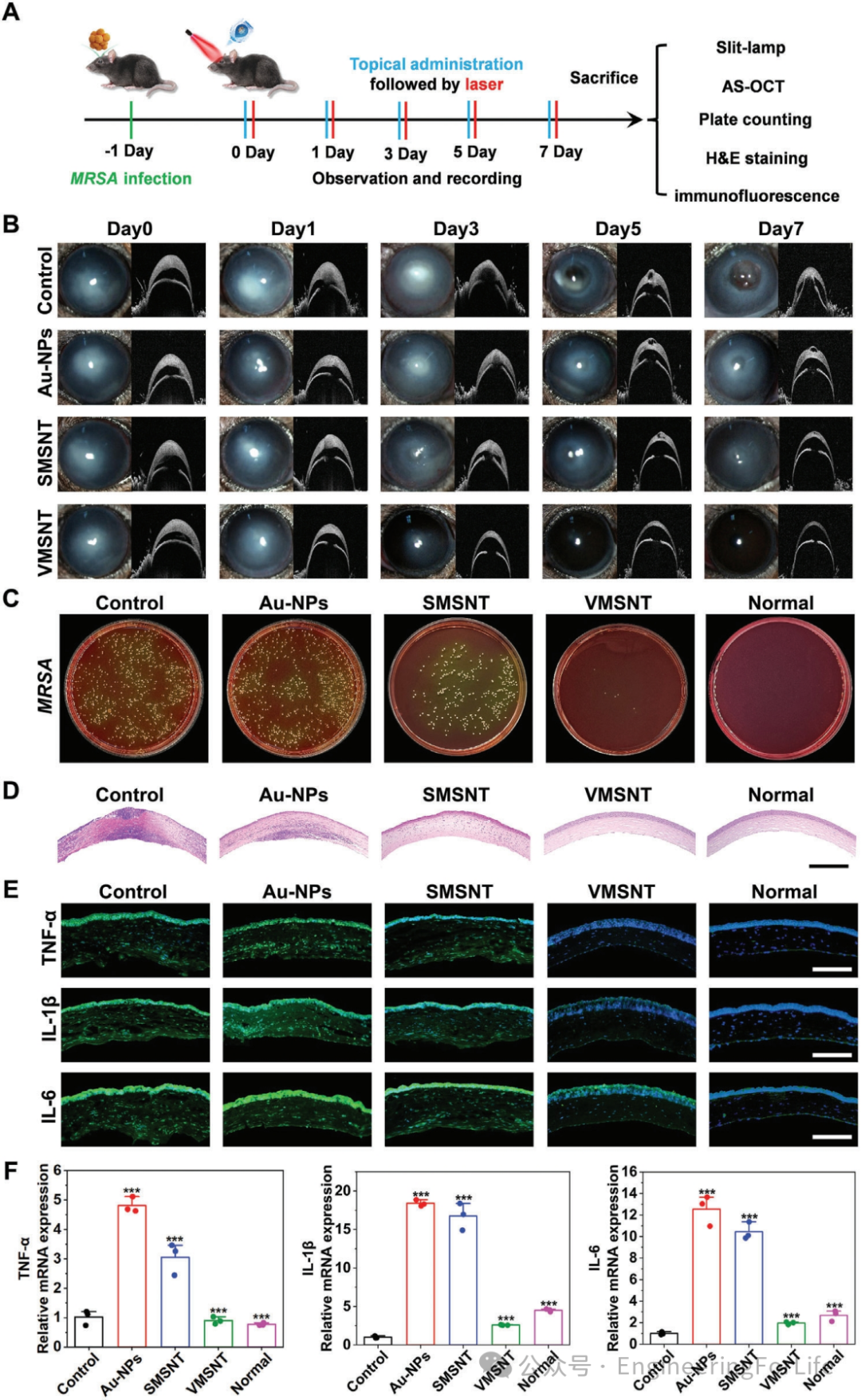
图7 VMSNT治疗MDR细菌性角膜炎的疗效评价
8.VMSNT对小鼠眼内炎模型的治疗效果
为了证明机械杀菌作为一种抗菌技术的多功能性,作者继续评估VMSNT在更具挑战性的MRSA感染眼内炎小鼠模型中的治疗潜力(图8A)。在第0天进行治疗,然后在随后的间隔内获取裂隙灯和OCT图像以评估治疗结果。
如图8B、C所示,VMSNT治疗的眼睛看起来很清晰,并且在评估结束时几乎没有炎症,这表明细菌性眼内炎完全消退。此外,VMSNT治疗组的临床评分在第7天下降到1(图8D)。此外,代表性菌落形成试验表明,VMSNT是所有治疗方法中消灭细菌最有效的,并解释了VMSNT对眼内炎的优异治疗效果(图8E、F)。
H&E染色结果说明VMSNT处理的小鼠的视网膜形态和结构基本保持完整。与其他组相比,VMSNT组的炎症细胞水平下调(图8G)。VMSNT治疗后,振幅值增加到正常水平(图8H)。这些结果再次证实了VMSNT纳米粒子在体内具有优越的机械杀菌治疗作用。
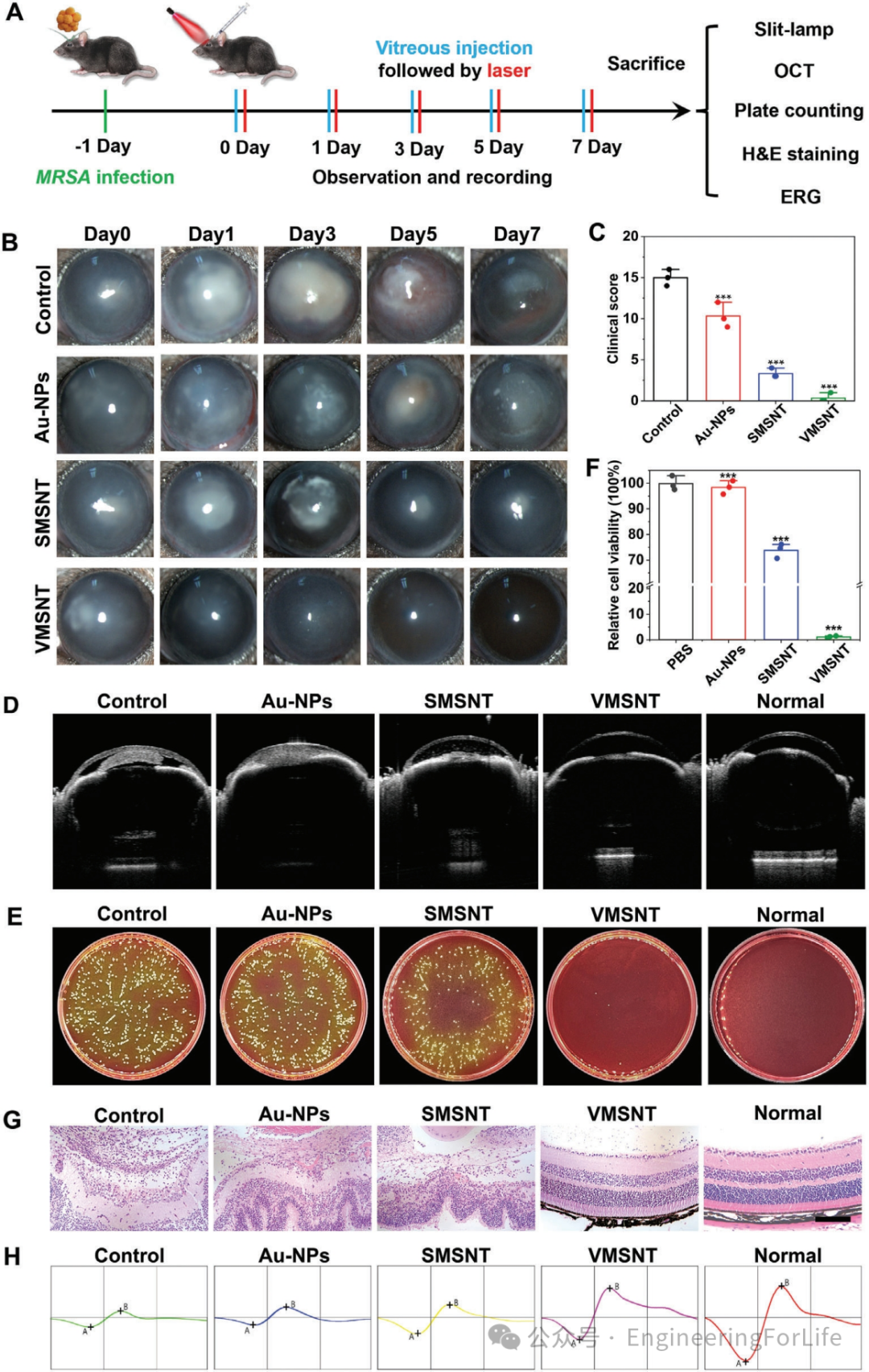
图8 VMSNT治疗MDR细菌性眼内炎的疗效评价
综上,本文成功开发出一种创新的机械杀菌纳米马达(VMSNT),它具有生物膜渗透能力和对抗眼部MDR细菌感染的有效抗菌性能。VMSNT的表面可以通过靶向分子进行策略性修改,利用其适应性表面化学特性主动靶向细菌。这项研究发现,具有类似病毒拓扑特征的光热纳米马达可以通过增加自热泳动力的引发和减少接触面积来弥合MNR和机械杀菌系统之间的差距。由于具有机械抗菌能力,纳米马达可以成功解决现存的MDR细菌和相应的成熟生物膜根除难题。此外,VMSNT具有良好的生物相容性,在治疗小鼠模型中的MRSA感染角膜炎和眼内炎方面表现出显著的治疗效果和生物安全性。
参考资料:
https://doi.org/10.1002/adma.202408221
来源:EngineeringForLife
声明:仅代表作者个人观点,用于研究用途,作者水平有限,如有不科学之处,请在下方留言指正!






