神经损伤(SNI)是一种严重的神经系统损伤,常导致下肢功能障碍和泌尿功能障碍,严重影响患者生活质量。传统的治疗方法包括非手术治疗(如神经营养药物、物理治疗)和手术治疗(如神经移植),但效果有限,且存在技术要求高、恢复时间长等问题。因此,开发新的治疗方法具有重要的临床意义。
基于此,来自同济大学医学院的陈爱民&上海长征医院朱磊&沈阳军区总医院神经外科金海等人
开发了一种使用了载负载抗皮肤生长因子受体(EGFR)水凝胶和神经干细胞(NSCS)的PCL神经导管,以治疗大鼠的神经损伤。使用3D打印的支架进行了交联水凝胶和NSC的组合移植疗法有效地改善了SNI,同时还能改善因神经损伤导致的膀胱功能障碍。
相关研究成果以
“Biocompatibility and Therapeutic Efficacy of Crosslinked Hydrogel Filled 3D-Printed Nerve Conduit for Sacral Nerve Injury Repair”
为题于2025年3月3日发表在
《Biomaterials》
上。
1.构建具有较低尿路症状的SNI大鼠模型
作者首先构建了大鼠神经损伤模型,使用了8周龄的SD大鼠,通过在显微镜引导下对神经根进行压迫损伤来模拟SNI(图1)。尿动力学测试(显示,SNI组大鼠的膀胱压力-时间曲线(P-T曲线)平滑且无明显波动,表明膀胱功能受损(图1G)。此外,SNI组大鼠的漏点压力(LPP)、最大膀胱容量(MBV)和膀胱顺应性在术后1周和4周时均显著高于假手术组(图1I-K),表明SNI导致了膀胱功能障碍。腹部超声检查(图1L)也发现SNI组大鼠的膀胱体积在术后1周和4周时显著增加(图1M),进一步证实了膀胱功能障碍的存在。
这些结果表明,通过双侧骶神经压迫损伤构建的SNI模型能够成功模拟仅具有下尿路症状的骶神经损伤,为后续的治疗研究提供了可靠的动物模型。
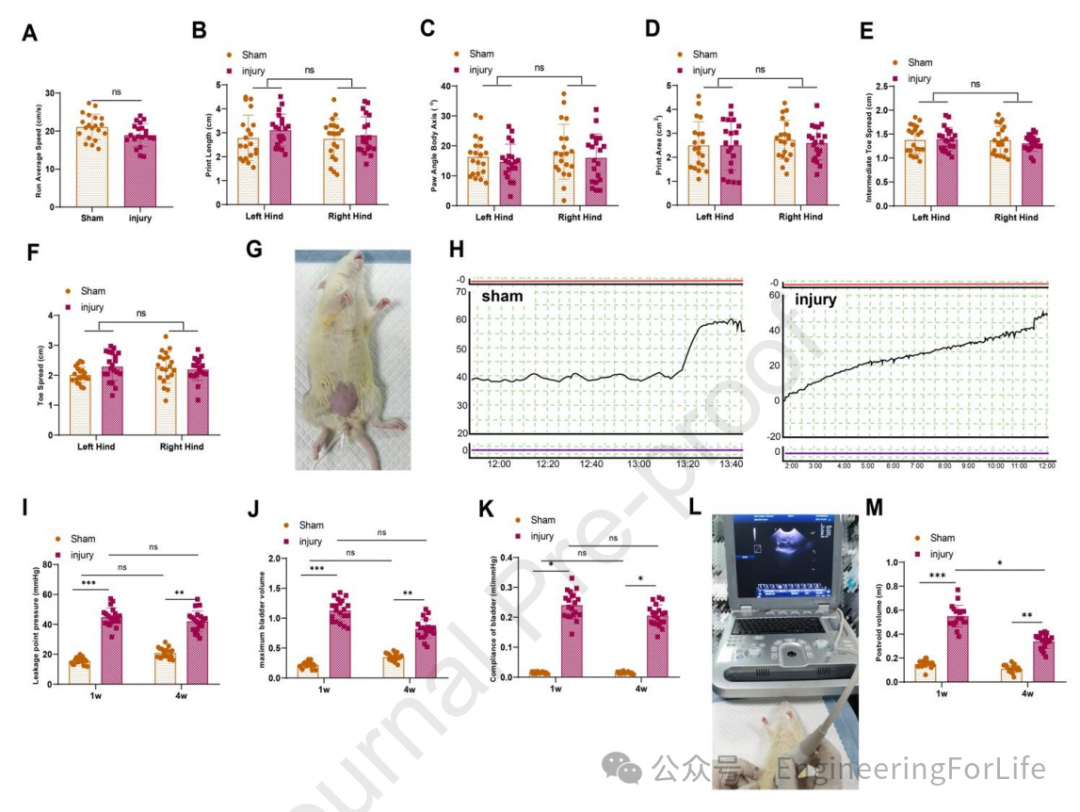
图1 SNI大鼠模型的构建和验证
2.腓肠神经移植在大鼠骶神经损伤修复中的应用
接着,作者通过腓肠神经移植手术来修复大鼠受损的骶神经,并对其疗效进行了评估。术后4周,对治疗组、损伤组(SNI组)和假手术组(Sham组)大鼠进行了尿动力学测试(图2A-C)和腹部超声检查(图2D)。与损伤组相比,治疗组大鼠的漏点压力(LPP)、最大膀胱容量(MBV)和膀胱顺应性显著降低,膀胱体积也明显减小,表明膀胱功能得到了显著改善。
此外,治疗组大鼠的膀胱重量较损伤组减轻(图2E),Masson三色染色(图2F)和H&E染色(图2G-H)结果显示,治疗组膀胱组织中胶原纤维减少,肌层结构清晰,膀胱壁增厚和炎症反应得到缓解。神经组织的H&E染色(图2I)和免疫荧光染色(图2J-K)也表明,治疗组骶神经的结构部分恢复,神经纤维密度增加,提示神经连续性得到改善。
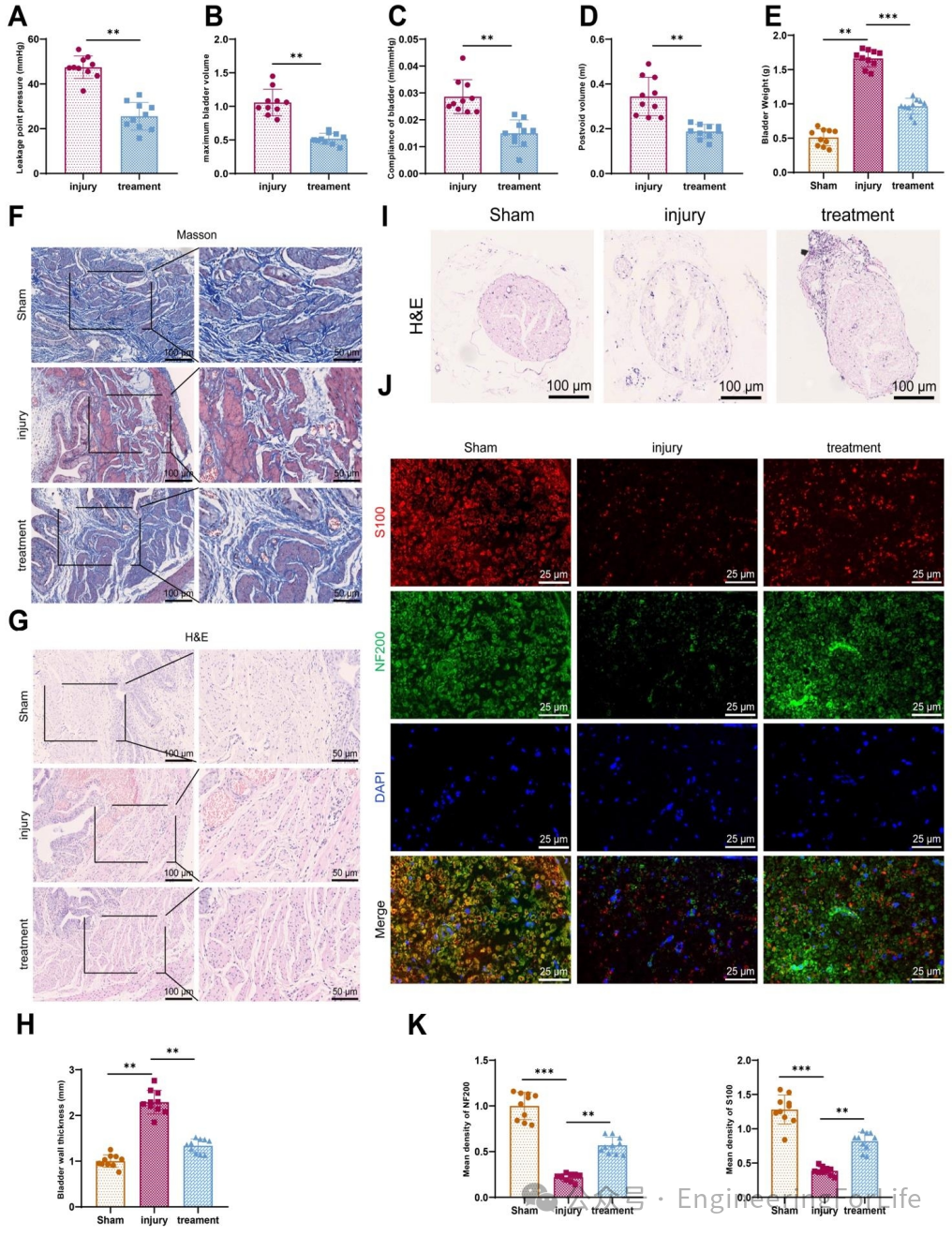
图2 SNI大鼠的手术神经移植的治疗作用
3.生物组学分析
作者进一步通过对大鼠骶神经损伤(SNI)模型的转录组分析,揭示了表皮生长因子受体(EGFR)基因在SNI治疗中的关键作用。
研究中收集了假手术组(Sham组)、损伤组(SNI组)和腓肠神经移植治疗组(治疗组)的受损神经组织进行高通量测序分析。GO和KEGG表明,这些基因主要涉及离子跨膜运输、神经递质运输、神经活性配体-受体相互作用和钙信号通路。
其中,EGFR基因在损伤组中显著上调,而在治疗组中显著下调,提示其可能通过钙信号通路抑制神经干细胞(NSCs)的神经分化。此外,蛋白质-蛋白质相互作用(PPI)分析显示EGFR在神经分化相关基因网络中具有最高的连接节点数
。
转录组学表明,EGFR在SNI中通过激活钙信号通路发挥重要作用,而抑制EGFR信号通路可能是治疗SNI的有效策略。
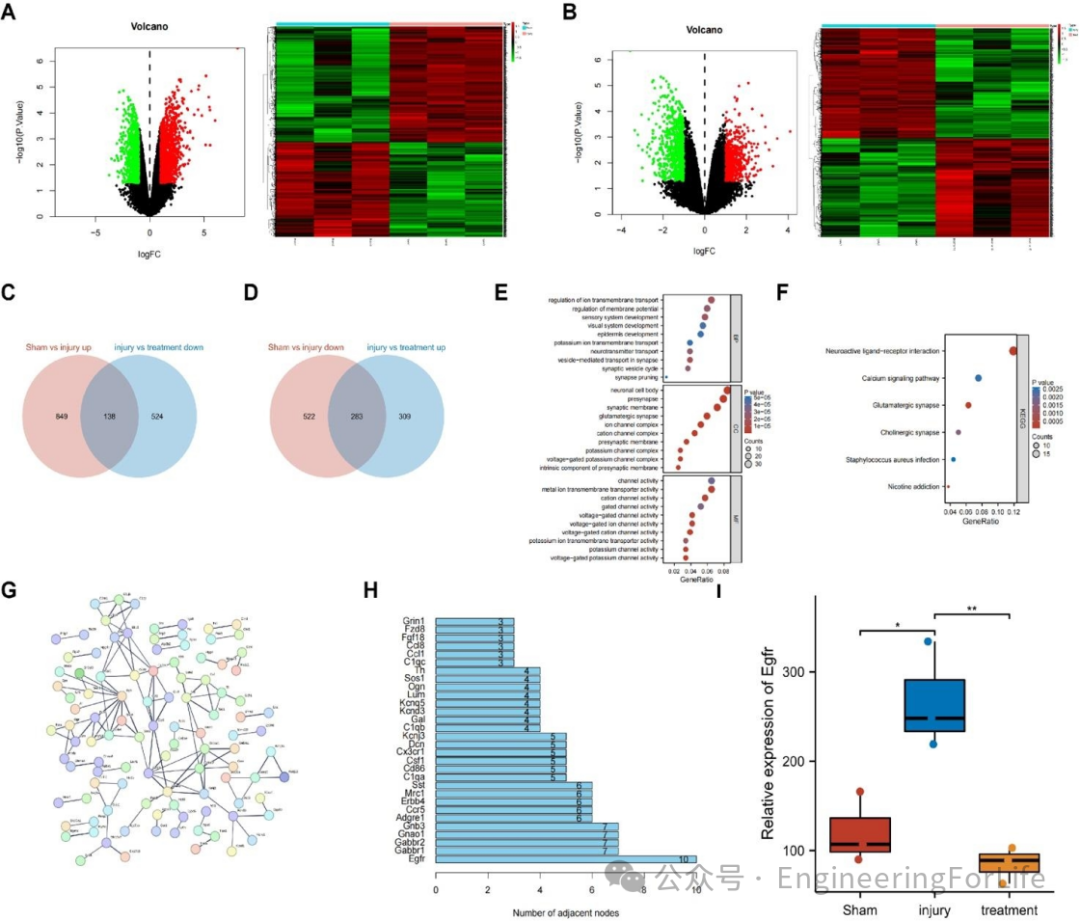
图3 通过生物信息学分析来治疗SNI的关键因素
4.水凝胶支架和交联对神经缺陷修复的影响和表征分析
基于EGFR对神经的修复作用,作者开发了一种用于神经缺损修复的交联水凝胶,并对其性能和修复效果进行了详细表征。研究中通过合成乙酰化透明质酸(Ac-HA)作为交联剂,制备了负载抗EGFR抗体的水凝胶(图4A)。
通过差示扫描量热法(DSC)测定了水凝胶的下临界溶解温度(LCST),发现其在生理温度附近(图4B),表明水凝胶具有良好的热响应性。此外,通过溶胀率和保水率测试评估了水凝胶的吸水和保水能力(图4B-C),表明水凝胶在37 ℃时具有显著的脱水特性,适合用于体内应用。流变学测试显示水凝胶具有剪切变稀行为,使其易于注射(图4D-E)。SEM分析揭示了水凝胶的多孔结构(图4F-G),这有助于细胞的附着和生长。
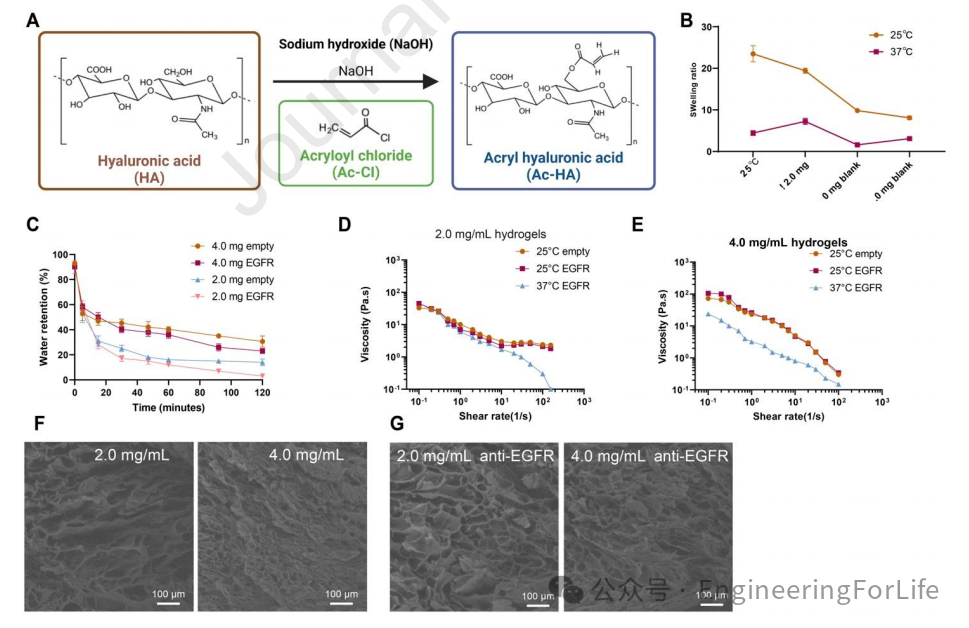
图4 交联水凝胶的制备和表征测试
5.水凝胶的体外生物相容性和神经分化潜力
在此部分,作者对水凝胶进行了体外生物相容性和神经分化潜力的评估。
通过活/死细胞染色实验(图5A-B),研究者发现水凝胶对神经干细胞(NSCs)的存活率无显著影响,细胞存活率均在90%左右,显示出良好的生物相容性。CCK-8实验进一步证实了NSCs在水凝胶中的活性(图5C)。EdU实验表明,NSCs在不同水凝胶中均能增殖,且增殖率无显著差异(图5D-E)。
此外,通过免疫荧光染色(图5F-J)和RT-qPCR分析(图5H、K),研究者发现抗EGFR负载的水凝胶能显著促进NSCs向神经元分化(Tuj-1和MAP-2表达增加),同时抑制其向胶质细胞分化(GFAP表达降低),尤其是4.0 mg/mL的抗EGFR水凝胶效果最为显著。
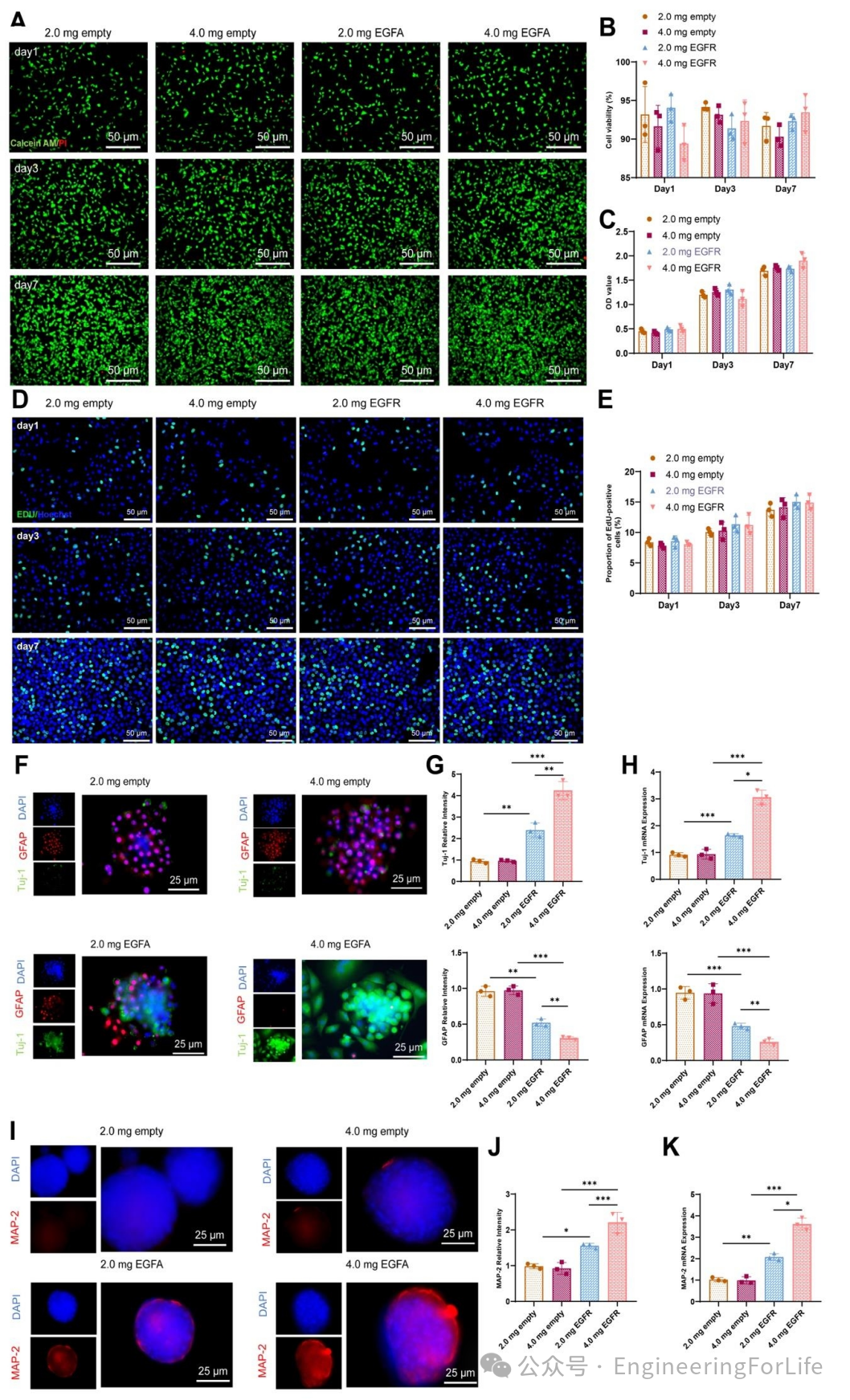
图5 研究水凝胶的体外生物相容性和分化促进能力
6.PCL神经导管/装有抗EGFR抗体交联的水凝胶和NSC用于修复神经缺陷
进一步,作者将抗EGFR抗体交联水凝胶和神经干细胞(NSCs)装载到3D打印的聚己内酯(PCL)神经导管中,用于修复神经缺损。
通过电生理分析(图6B)评估了不同处理组大鼠的神经功能恢复情况,装载抗EGFR水凝胶和NSCs的PCL导管组(治疗组)的神经动作电位(NAP)波幅最高,表明其神经再生效果最佳。免疫荧光观察也表明治疗组在神经再生轴突的连续性和密度方面表现最优,神经纤维标记物NF200和S100的阳性密度最高(图6C-D);H&E染色进一步证实了治疗组在神经结构修复方面的优势(图6E)。
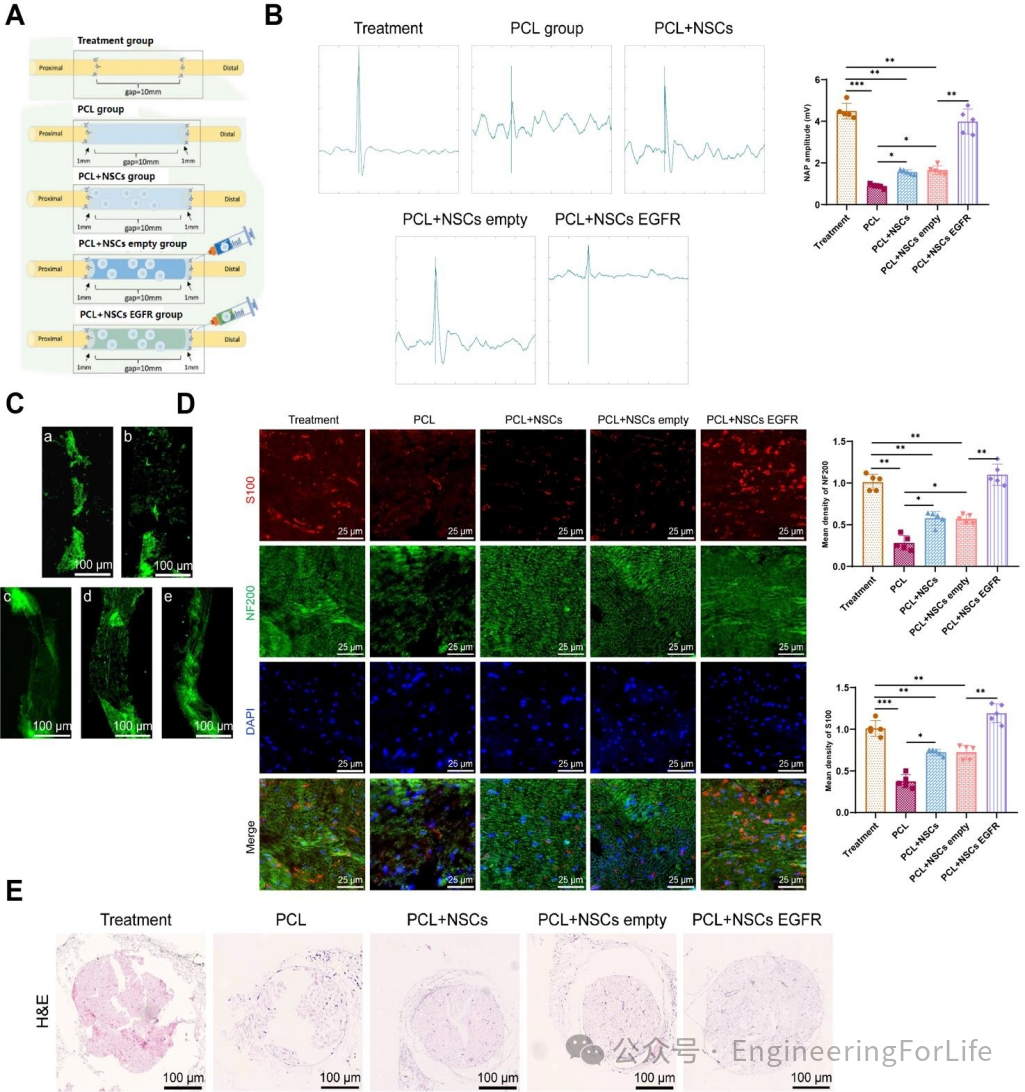
图6 PCL神经导管、水凝胶和NSC的联合处理对大鼠神经的影响
重要的是,该材料对骶神经损伤(SNI)大鼠膀胱功能也有着良好的改善效果。
通过尿动力学测试评估了各组大鼠的膀胱功能,结果表明接受联合治疗的大鼠在漏点压力(LPP)、最大膀胱容量(MBV)和膀胱顺应性方面与治疗组(腓肠神经移植组)无显著差异,而其他对照组的这些参数则显著高于治疗组,表明联合治疗能够显著改善膀胱功能(图7A-C)。此外,腹部超声检查(图7D)也发现联合治疗组的膀胱体积与治疗组相近,明显小于其他对照组。组织学分析方面,Masson三色染色(图7F)和H&E染色(图7G-H)显示联合治疗组的膀胱组织中胶原纤维减少,肌层结构清晰,膀胱壁增厚和炎症反应得到缓解,与治疗组相似。上述结果表明,PCL神经导管、抗EGFR抗体交联水凝胶和NSCs的联合治疗能够有效改善SNI大鼠的膀胱功能,促进膀胱组织结构的恢复。
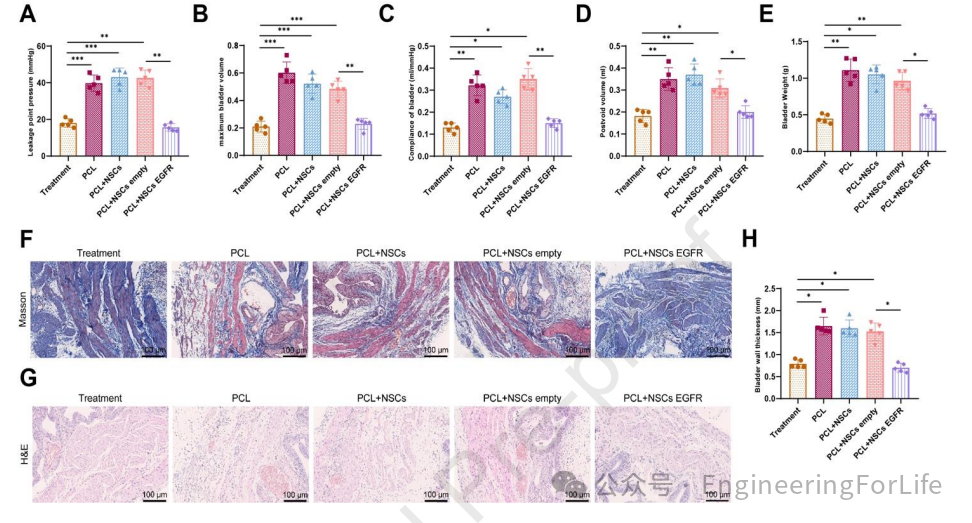
图7 PCL神经导管、水凝胶和NSC的联合处理对大鼠膀胱功能的影响
综上,本文通过将抗表皮生长因子受体(EGFR)抗体交联水凝胶和神经干细胞(NSCs)装载到3D打印的聚己内酯(PCL)神经导管中,形成了一种新型的联合治疗策略,能够有效促进骶神经损伤(SNI)的修复,并显著改善受损神经功能和膀胱功能。这种联合治疗方法在体外和体内均显示出良好的生物相容性和神经再生能力,能够通过抑制EGFR信号通路促进NSCs的神经分化,从而加速神经再生和功能恢复。此外,该策略还能显著改善因神经损伤导致的膀胱功能障碍,包括降低膀胱残余尿量、改善膀胱顺应性,并恢复膀胱组织的正常结构。
参考资料:
https://doi.org/10.1016/j.biomaterials.2025.123230
来源:
EngineeringForLife
声明:仅代表作者个人观点,用于研究用途,作者水平有限,如有不科学之处,请在下方留言指正!






