

第一作者:李玉楠,郭玲玲
通讯作者:李丽娜,南兵,蒋罗震
通讯单位:中国科学院上海应用物理研究所,中国科学院上海高等研究院
论文DOI:10.1038/s41467-024-49968-6
原位探究催化剂在催化反应过程中的动态结构演变在揭示反应机制和设计高效催化剂方面发挥着关键作用。在这项工作中,作者通过共同浸渍的方法制备了MgO负载的PtCu双金属催化剂,其与单金属Pt/MgO或Cu/MgO催化剂相比展示出良好的催化CO氧化活性。通过原位XAFS等多种表征方法揭示了PtCu/MgO催化剂从Pt
x
Cu
y
O
z
二元氧化物团簇(空气煅烧后)到PtCu合金(H
2
活化后)再到PtCu合金-CuO
x
(CO氧化反应过程中)的结构演变。在CO氧化反应过程中PtCu合金和CuO
x
物种发挥协同作用。通过原位DRIFTS、CO-TPR以及
18
O
2
同位素标记实验发现在低温下,M-vK机制在CO氧化反应中占据主导地位(约63%),PtCu合金表面的CuO
x
物种可以提供活性氧物种与CO反应生成CO
2
。然而在高温下,L-H机制在CO氧化中起主导作用(约60%),CuO
x
和PtCu合金可以共同活化O
2
参与CO氧化反应。这项工作可以为双金属或多金属催化剂在氧化反应中的结构演变提供有意义的指导。
CO氧化反应是一种重要的催化反应,其在机动车尾气净化,工业废气处理中得到了广泛应用。同时CO氧化也常作为基础催化研究的典型模型反应。近几年,负载型铂基催化剂由于其在相对较高温度(> 150 °C)下表现出优异的CO氧化活性和稳定性而引起了广泛关注。然而,在低温下CO在铂位点上强的竞争吸附使得O
2
的吸附活化较为困难,从而影响了催化反应的进行。
在CO氧化反应中,有很多方法可以改善铂基催化剂的催化性能,如构建合金组分、建立金属-载体相互作用、金属-氧化物和金属-金属氢氧化物活性位点。在这些方法中,与另一种金属合金化形成双金属合金纳米颗粒已被证明是改善催化性能的有前途的方法之一。众所周知,电负性相似的两种元素更容易共享电子而形成合金。铜(Cu)作为代表性过渡金属因其丰富的表面氧物种而受到广泛关注。从合金的角度来看,铜元素与铂元素的电负性差距较小,原子半径差距也较小,这样有助于两种元素在晶格中替代并避免明显的晶格畸变。其次,PtCu合金因为其低成本、特殊的几何效应、电子效应和多功能效应也被证明是CO氧化中有前景的催化剂。
此外PtCu合金在其他氧化反应中也表现出高的催化性能,如甲醇氧化、选择性氨氧化和多羟基醇氧化。尽管研究者们对PtCu合金进行了一些详细而深入的研究,但是大部分工作还是集中在合成-表征-性能测试这样的研究范式上,对催化剂活性位点的认知大部分也是停留在“静态”的观念上,并没有太多的去考虑催化剂在活化和反应条件下的动态结构演变。关于PtCu合金催化CO氧化反应中仍存在一些有争议和未解决的问题:首先,PtCu合金在整个CO氧化过程中是否能保持稳定?其次,在氧化气氛中PtCu合金的结构是如何演变的,铂和铜物种的氧化程度如何(考虑到金属Cu物种对氧的敏感性)?第三,缺乏先进的原位表征技术来探索PtCu合金催化剂在CO氧化反应过程中的主要反应机制是什么(M-vK还是L-H)?
1.
通过原位XAFS等表征方法揭示了Pt-Cu双金属催化剂在CO氧化反应过程中从PtCu合金到PtCu合金-CuO
x
的结构演变,在CO氧化反应过程中PtCu合金和CuO
x
发挥协同作用。
2.
在低温下,M-vK机制在CO氧化反应中占据主导地位(约63%),PtCu合金表面的CuO
x
可以提供活性氧物种与CO反应生成CO
2
。然而在高温下,L-H机制在CO氧化中起主导作用(约60%),CuO
x
和PtCu合金可以共同活化反应气氛中O
2
参与CO氧化反应。
MgO负载的铂铜双金属催化剂(PtCu/MgO)是通过共同浸渍法制备的,单金属Pt/MgO和Cu/MgO催化剂采用相同的方法合成作为对比样品。新鲜制备的PtCu/MgO样品的HAADF-STEM图像和相应的EDS mapping结果(图1)得到Pt和部分Cu元素以团簇形式在MgO载体上的同一区域内均匀分布,由于铜的负载量(6 wt.%)相对于铂的负载量(0.5 wt.%)较高,一部分铜物种孤立地均匀分散在MgO载体上。为了进一步确认PtCu/MgO中团簇的元素组成,相应的线扫结果显示团簇同时含有铂元素和铜元素,证明团簇为Pt
x
Cu
y
O
z
二元氧化物团簇。H
2
-TPR结果(图1e)也揭示了PtCu/MgO中铂和铜之间的强相互作用,PtCu/MgO样品在187 °C处有一个强的还原峰可归属为Pt-[O]
x
-Cu结构,这与PtO
x
(213 °C)和CuO
x
(209°C)物种的还原峰明显不同,表明铂和铜之间的相互作用可以显著提高催化剂的可还原性。对PtCu/MgO样品的H
2
-TPR谱图进行分峰拟合,发现在209 °C位置也有一还原峰可归因于CuO
x
团簇,说明部分Cu物种以孤立状态存在而不与Pt物种形成相互作用,此结果与上文PtCu/MgO的EDS mapping结果一致。因此,CuO
x
和Pt
x
Cu
y
O
z
团簇共存于PtCu/MgO样品中。XAFS表征技术被使用去进一步确认铂和铜更精确的电子状态和配位结构信息。在PtCu/MgO样品上拟合得到强的Pt-O壳层(R ≈ 1.98 Å和CN ≈ 5.5),Pt-O-Cu壳层(R ≈ 3.11 Å和CN ≈ 2.8)和Pt-O-O壳层,进一步证实了Pt
x
Cu
y
O
z
团簇的形成。同时,没有Pt-O-Pt壳层的存在表明PtCu/MgO中没有孤立的PtO
x
团簇。
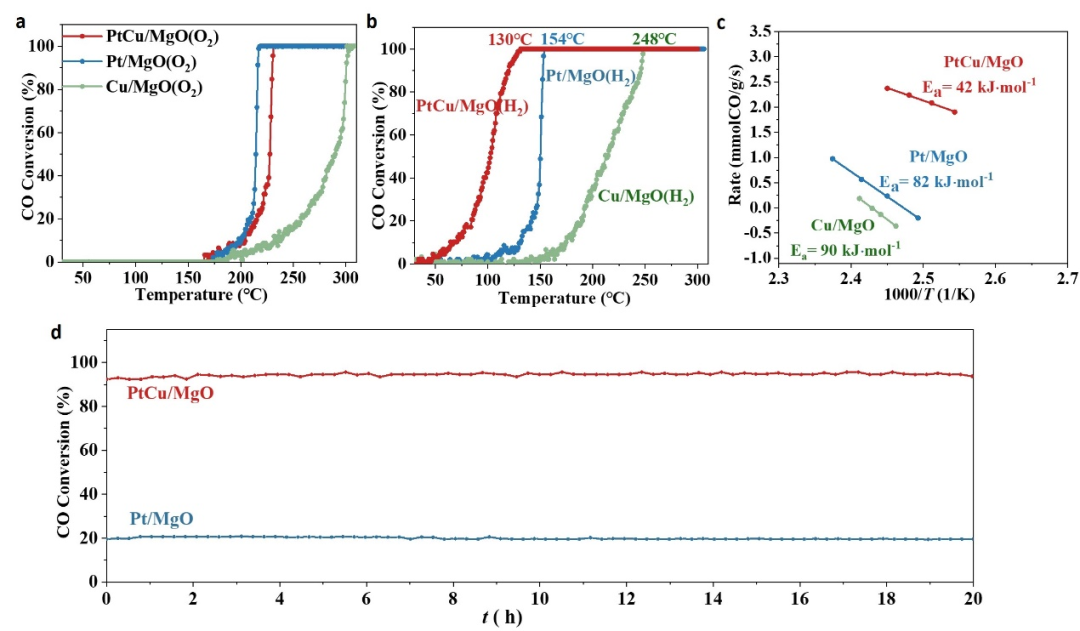
图2 PtCu/MgO催化剂在CO氧化反应的催化表现
在此工作中,当催化剂在O
2
气氛下进行预处理时,所有样品在催化CO氧化活性方面表现不佳,CO氧化完全转化温度大于200 °C。然而,经过500 °C的氢气预处理后,所有样品的活性显著提高。PtCu/MgO在130 °C下CO转化率达到100%,甚至在大约50 °C时就能有催化CO氧化活性。对于单金属Pt和Cu样品,分别是在154 °C和248 °C时才能实现CO完全转化,且在100°C以下的活性很低。这说明氢气还原不仅降低了铂和铜物种的氧化态,还可能调节了活性位点的结构。为了验证此假设,获取了相关的动力学数据(图2c)。PtCu/MgO催化剂的表观活化能(
E
a
)约为42 kJ·mol
-1
,远低于Pt/MgO(82 kJ·mol
-1
)和Cu/MgO(90 kJ·mol
-1
),表明它们活性位点结构或反应机制不同。此外,在模拟汽车尾气条件下(GHSV:190,000 mL·h
-1
·g
cat
-1
),对PtCu/MgO样品在150 °C下进行了长时间催化稳定性测试,发现催化剂在20小时内没有发生任何失活,转化率保持在约94%。同时,在相同测试条件下,单金属Pt催化剂在150 °C下也表现出良好的稳定性,但转化率仅有20%左右。
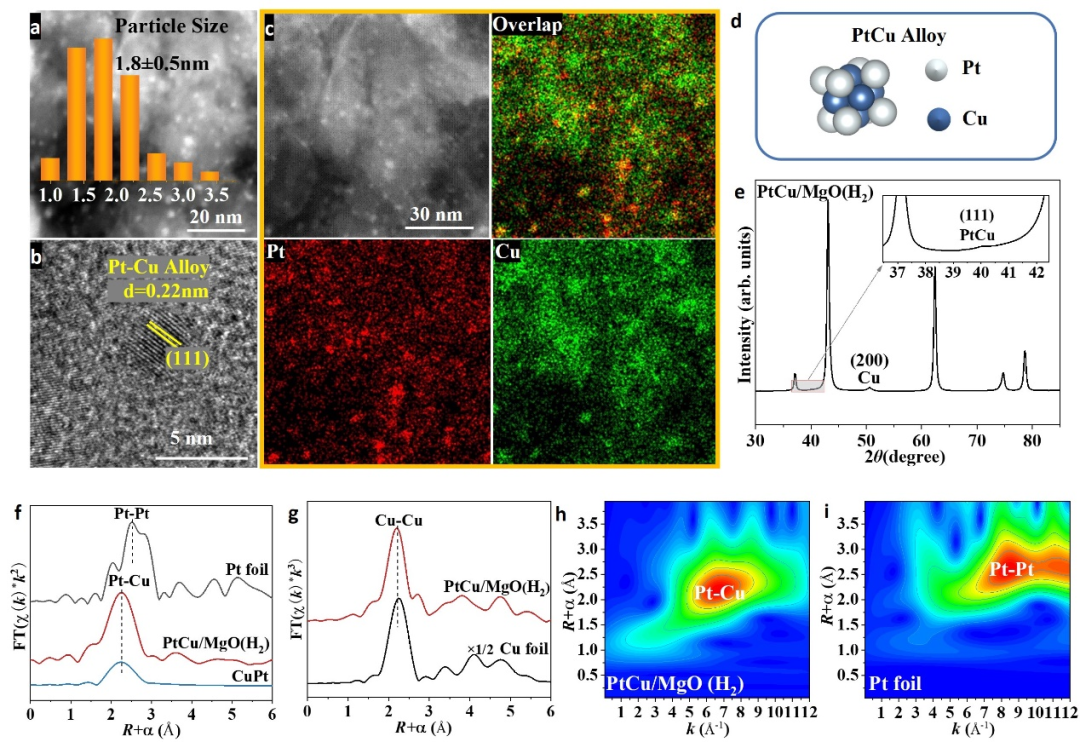
为了探究氢气活化后PtCu/MgO催化剂更精确的结构信息,对催化剂进行了深入表征(图3)。HAADF-STEM图像显示经过氢气还原后,PtCu/MgO中的活性位点平均颗粒尺寸保持在约1.8 nm左右,其中图3b中颗粒晶面间距为0.22 nm,可以被归属为PtCu合金(CuPt JCPDS 48-1549)的(111)晶面。与此同时,图3c的EDS mapping结果也证实了Pt元素和Cu元素分布的空间一致性。为了进一步确认PtCu合金的形成,进行了准原位同步辐射XRD和原位XAFS实验。PtCu/MgO经过氢还原后的XRD图(图3e)与MgO谱图相比显示出两个额外的位于40.1°和50.4°的峰,归属于PtCu合金的(111)晶面和金属Cu的(200)晶面。图3f 中PtCu/MgO(H
2
)的原位Pt L
3
边EXAFS显示出一个主要位于~2.60 Å的峰(
CN
≈ 11.8),其与Pt foil明显不同,并与PtCu合金的标准路径(mp-644311来自The Materials Project)一致,证明了PtCu合金的形成。图3g中PtCu/MgO(H
2
)的原位Cu K边EXAFS显示出一个主要的位于~2.59
Å的Cu-Cu壳层(
CN
≈ 6.3),表明孤立的CuO
x
团簇在氢气预处理后被还原为金属Cu颗粒。为了进一步认证PtCu合金的形成,对Pt foil、PtO
2
和PtCu/MgO(H
2
)的Pt L
3
边EXAFS进行了小波变换(WT)分析。Pt foil和PtO
2
的WT等高线图中,在位于10 Å
-1
和5 Å
-1
附近的强度最大值分别归因于Pt-Pt和Pt-O的贡献。相比之下,在PtCu/MgO(H
2
)的WT等高线图中,只观察到一个位于近7 Å
-1
处的强度最大值,归因于Pt-Cu的贡献。原位XANES结果显示,PtCu/MgO经过氢气还原后,Cu和Pt的平均氧化态均为0价。因此,HAADF-STEM、准原位同步辐射XRD和原位XAFS表征的结果验证了PtCu/MgO经过氢气还原后形成了PtCu合金。
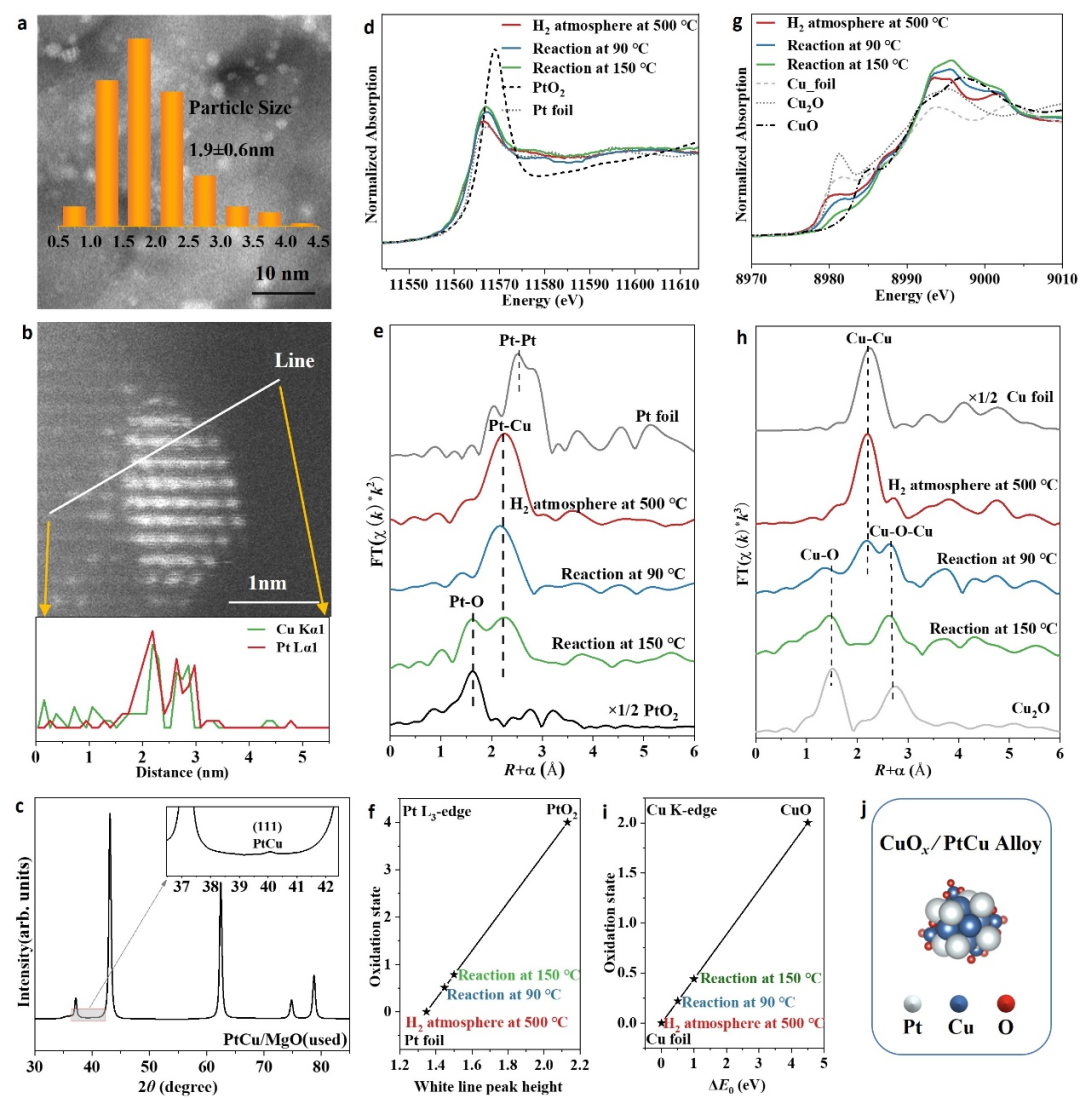
图4 CO氧化反应过程中PtCu/MgO催化剂的结构演变
由于CO氧化反应气氛中含有大量的O
2
,因此在反应过程中活性位点的配位结构特别是氧化态很可能会进一步演变。图4c的准原位同步辐射XRD图显示PtCu/MgO(used)样品仍存在归属于PtCu合金(111)晶面的位于40.1°的衍射峰,确认了CO氧化反应后PtCu/MgO中PtCu合金的稳定存在。此外,采用原位XAFS技术探究了活性位点精确的结构演变。图4e显示在CO氧化反应进行到90 °C时,Pt-Cu壳层保持稳定没有明显形成Pt-O壳层。随着反应温度升至150 °C,Pt物种被稍微氧化,出现了Pt-O壳,Pt价态为+0.5价,然而主要的Pt-Cu壳层仍然稳定存在。对于PtCu/MgO中的Cu物种,发现其在500 °C的氢气还原条件下可以被还原为零价的金属Cu。当CO氧化反应温度升到90 °C时,开始出现Cu-O和Cu-O-Cu壳层,表明CuO
x
物种的出现。当CO氧化反应温度升到150 °C时,金属Cu-Cu壳完全消失,铜的氧化价态为+0.4,表明PtCu合金表面上的Cu物种以及孤立Cu物种再分散和再氧化。
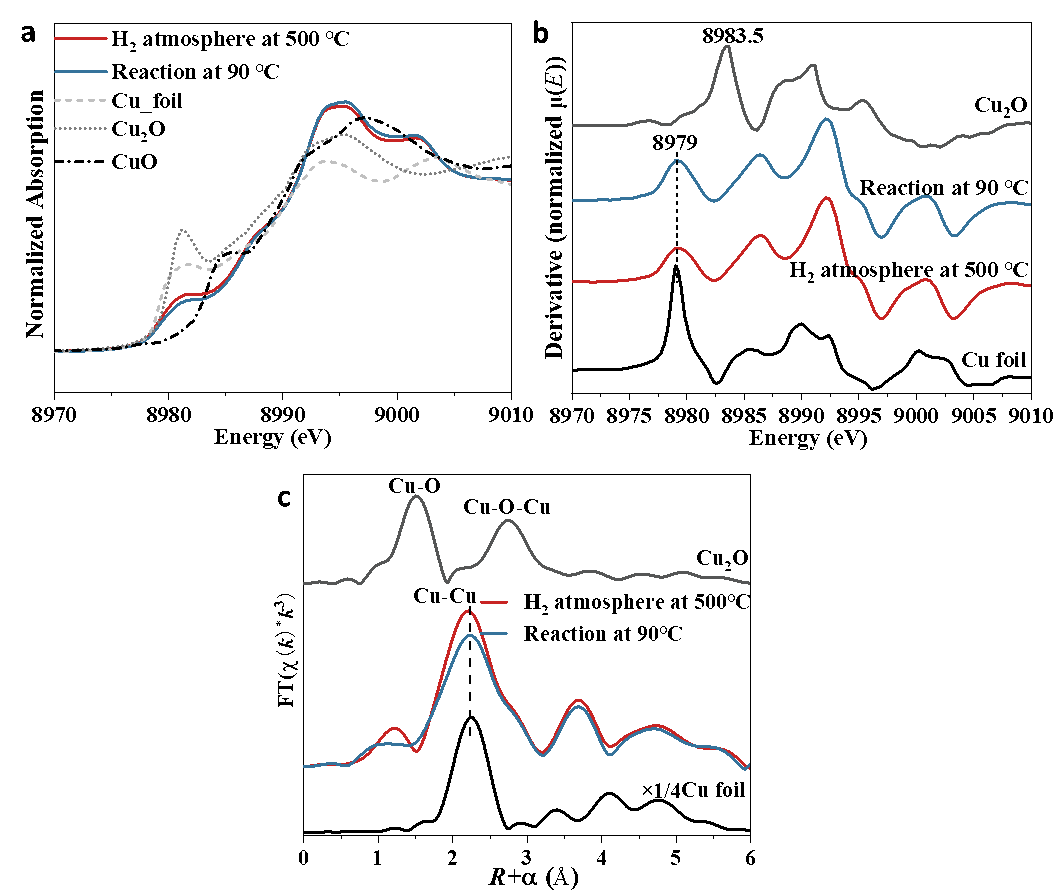
为了探究当CO氧化反应温度升到90 °C时形成的CuO
x
物种是来自PtCu合金表面还是孤立的金属Cu的再分散,对Cu/MgO样品进行了原位XAFS表征(图5),结果显示氢气还原后CuO
x
物种可以被还原为金属Cu,并且在CO氧化反应温度升到90 °C时仍保持金属态(Cu
0
)。这表明PtCu/MgO样品经过氢气活化后,当反应气体(1 vol.% CO/20 vol.% O
2
/He)引入后,PtCu合金中的Cu原子能迅速解离O
2
成为活性氧物种,同时在PtCu合金表面上形成CuO
x
物种。此外,发现Cu/MgO(used)样品中仍可以拟合出Cu-Cu壳层(
CN
≈ 0.7),表明将孤立的金属Cu颗粒完全分散为小的CuO
x
团簇需要更高的温度。因此,可以得出结论,在CO氧化反应过程中,PtCu/MgO的主要活性位点为PtCu合金-CuO
x
。
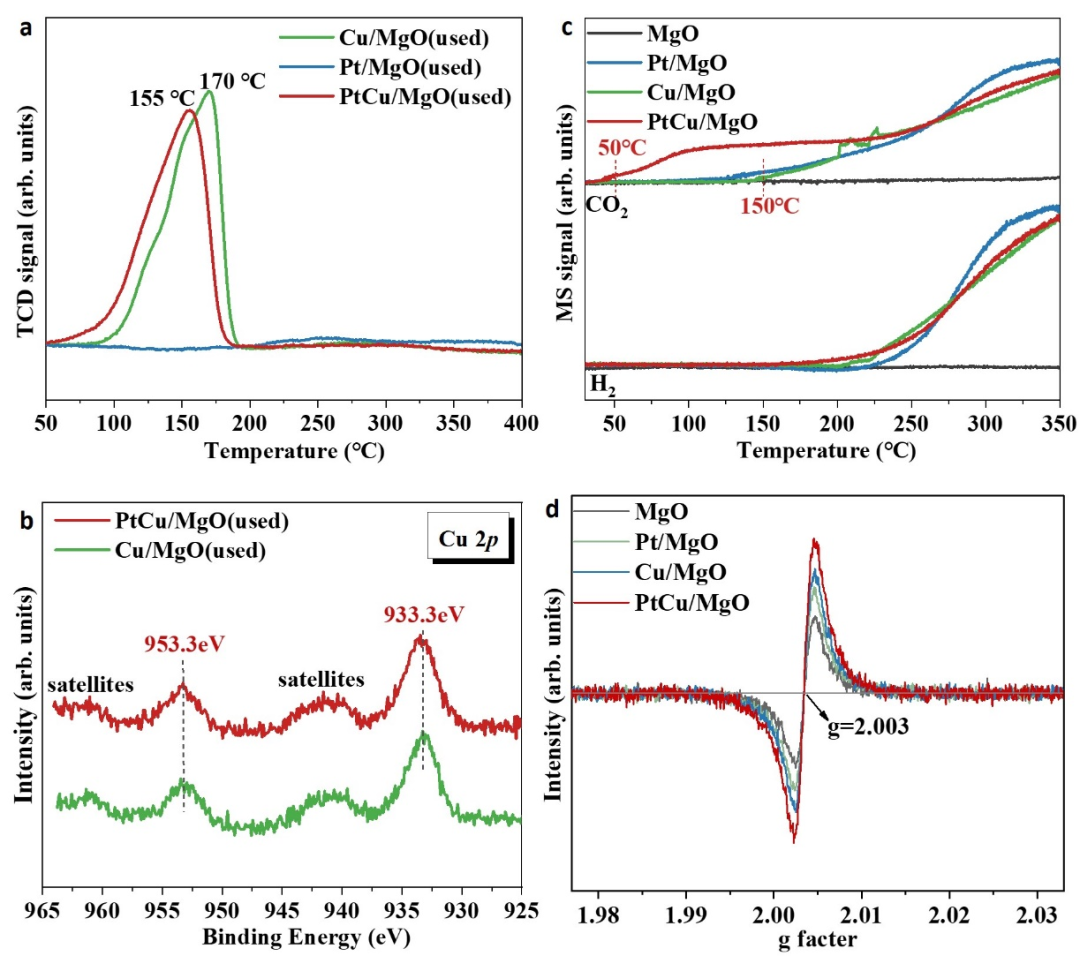
对CO氧化反应后的催化剂进行了原位H
2
-TPR实验(图6a),以检测反应后催化剂的可还原性。由于在H
2
预处理过程中,绝大部分铂物种被还原为Pt
0
,而铂在氧化性环境下没那么容易被快速氧化,因此CO氧化反应后的Pt/MgO样品,没有发现明显的还原峰。然而,对于反应后的Cu/MgO和PtCu/MgO样品,分别在170或155 °C处存在明显的还原峰,这被归因于铜氧化物的还原,表明在PtCu合金上有丰富的CuO
x
物种,其可还原性比Cu/MgO中的常规CuO
x
物种更高。同时,XPS结果(图6b)揭示了CO氧化后PtCu/MgO催化剂表面上铜的平均氧化态为+2价。此外,图6c中的原位CO-TPR结果还揭示了PtCu/MgO和Cu/MgO之间表面活性氧物种的差异。PtCu/MgO中的表面氧可以在约50 °C时与CO分子发生反应,与CO氧化反应“light off”曲线的起活温度非常一致。PtCu合金表面的CuO
x
物种可能通过Mars-van
Krevelen(M-vK)机制促进低温CO氧化(~50 °C),从而提高CO氧化活性。然而,Pt/MgO和Cu/MgO在较高温度(>
150 °C)下才检测到CO
2
的生成。这表明在低温下,孤立的CuO
x
物种对CO氧化活性几乎没有贡献。此外,对所有样品在230 °C-350 °C范围内的峰被归因于催化剂表面羟基的水煤气转化反应。图6d中的电子顺磁共振(EPR)结果显示所有样品在g值为2.003位置有明显的对称信号峰,归因于氧空位,发现CO氧化反应后的PtCu/MgO具有最丰富的氧缺陷,可能源自PtCu合金表面的CuO
x
物种。
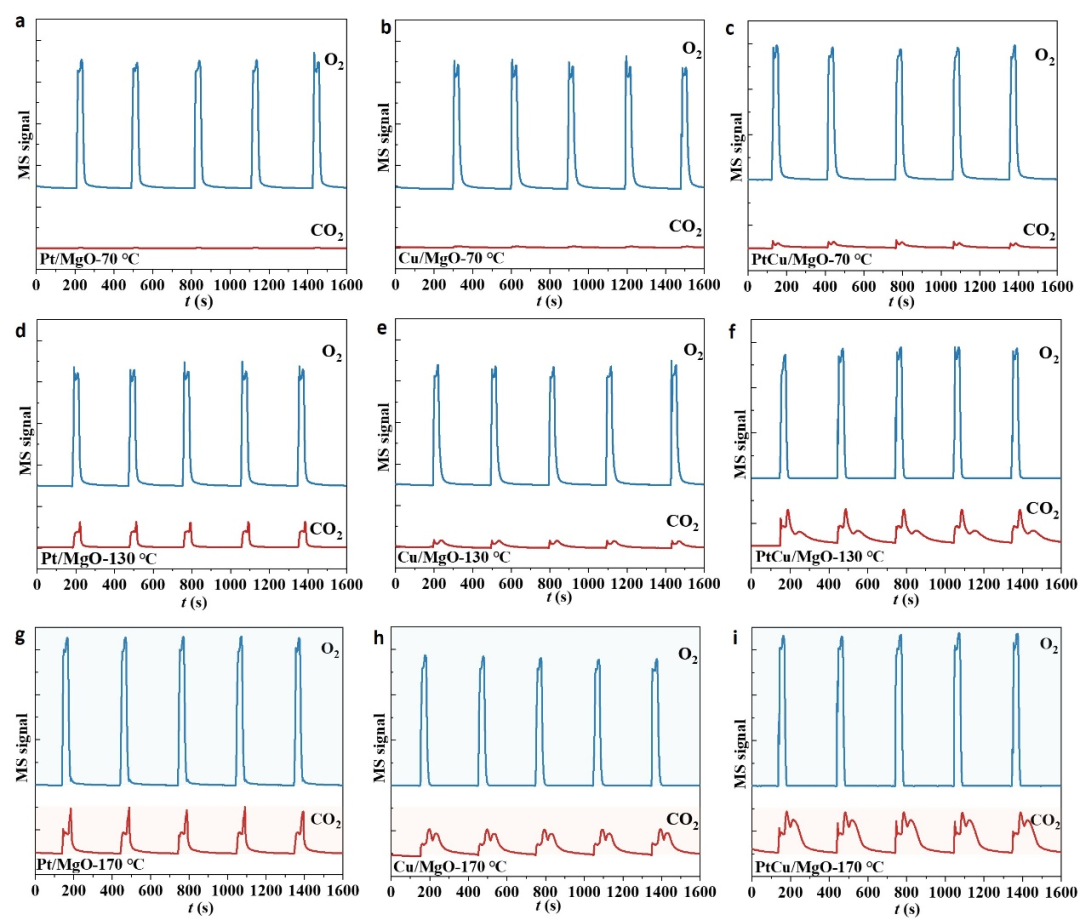
作者设计了O
2
脉冲实验来测试催化剂对氧气的活化能力(图7)。在70 °C时,PtCu/MgO能够活化O
2
生成CO
2
,而对于Pt/MgO和Cu/MgO,由于活化氧气的能力较差,几乎看不到明显的CO
2
信号。随着实验温度升高至130 °C,PtCu/MgO催化剂产生的CO
2
峰面积明显大于Pt/MgO和Cu/MgO,表明在130 °C时PtCu/MgO对O
2
的解离能力更好。还发现对于PtCu/MgO样品,当O
2
脉冲峰下降之后,仍然有额外的CO
2
生成,这可以归因于CO与PtCu合金表面具有良好的可再生性CuO
x
物种表面的活性氧反应。当O
2
脉冲实验在170 °C进行时,Cu/MgO也有额外的CO
2
生成。然而,Cu/MgO产生的CO
2
峰面积小于PtCu/MgO,表明PtCu合金表面的CuO
x
比孤立的铜氧化物具有更好的氧气活化能力。
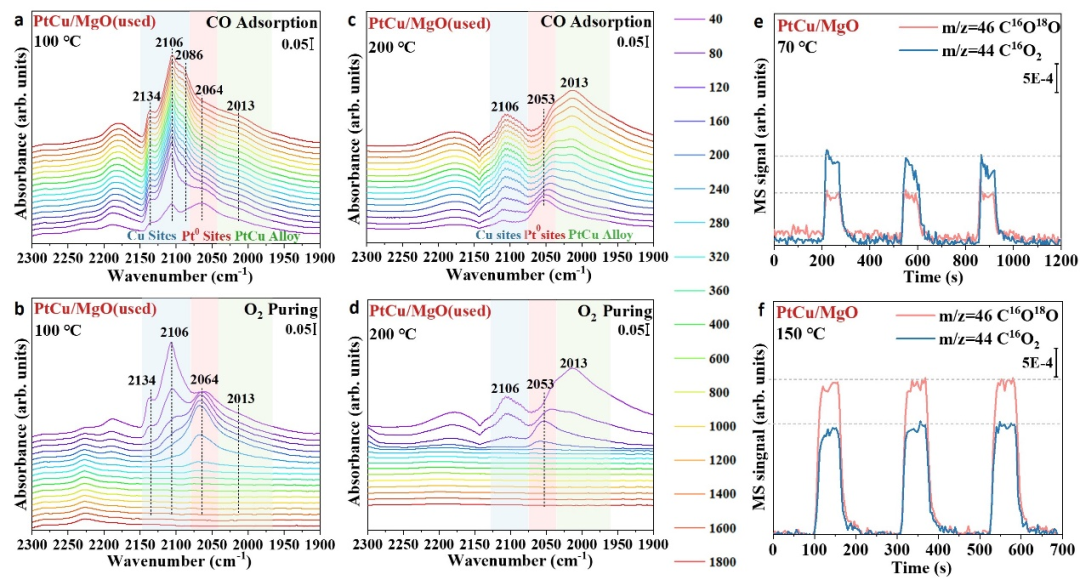
图8 PtCu/MgO催化剂在不同温度下的原位DRIFTS实验及
18
O
2
同位素标记实验
根据原位DRIFTS结果(图8a-d),在不同温度范围内,CuO
x
物种和PtCu合金在CO氧化活性中发挥着不同的作用。在低温(< 100 °C)下,CuO
x
物种可以通过其丰富的活性氧物种促进CO氧化反应。随着反应温度的升高PtCu合金也能够有效吸附CO分子并活化O
2
以促进CO氧化反应。对PtCu/MgO进行了
18
O
2
同位素标记实验(图8e-f),结果显示在不同的温度范围内,M-vK和L-H反应机制分别起主导作用。可以看到,当反应温度为70 °C时,表面的CuO
x
物种可以提供活性氧物种与CO分子反应生成C
16
O
2
。与此同时,CuO
x
中的氧离子(O
v
)可以解离气相的
18
O
2
产生活性的O
18
自由基,并促进
C
16
O
18
O
的进一步生成。根据质谱的CO
2
信号显示,在70 °C时,M-vK机制在CO氧化反应中占据主导地位(约63%)。当反应温度为150 °C时,随着CO在PtCu合金位点的吸附量增加以及气相O
2
在该位点上更容易被解离,催化剂可以通过L-H机制将CO分子和
18
O
2
转化为C
16
O
18
O。在这个温度下,L-H机制在CO氧化中起主导作用(约60%)。
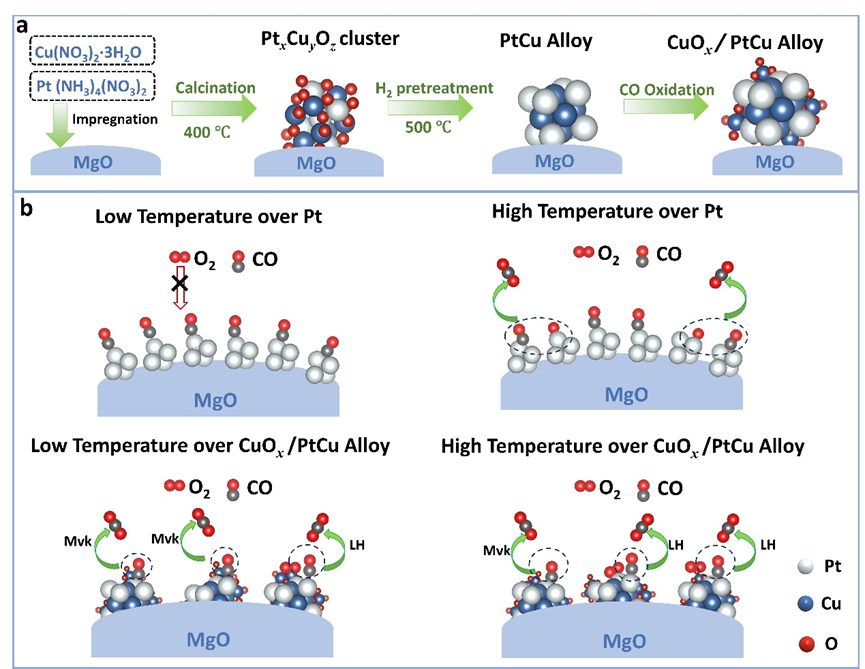
总的来说,通过共同浸渍的方法制备了MgO负载的Pt-Cu双金属催化剂,其与单金属Pt/MgO或Cu/MgO催化剂相比展示出良好的催化CO氧化活性。通过原位XAFS、准原位同步辐射XRD和STEM等多种表征方法,揭示了PtCu/MgO催化剂从Pt
x
Cu
y
O
z
二元氧化物团簇(空气煅烧后)到PtCu合金(H
2
活化后)再到PtCu合金-CuO
x
(CO氧化反应过程中)的结构演变,在CO氧化反应过程中PtCu合金和CuO
x
物种发挥协同作用。在低温下,M-vK机制在CO氧化反应中占据主导地位(约63%),PtCu合金表面的CuO
x
物种可以提供活性氧物种与CO反应生成CO
2
。然而在高温下,L-H机制在CO氧化中起主导作用(约60%),CuO
x
和PtCu合金可以共同活化气态O
2
参与CO氧化反应。
文献信息
:https://doi.org/10.1038/s41467-024-49968-6
李丽娜,
1979年生,中国科学院上海高等研究院研究员,上海光源用户辅助实验组组长,博士生导师。2001~2007年在华东师范大学攻读硕、博士学位,2007~2010年先后在同济大学、德国斯图加特大学从事博士后研究工作,2010年5月起任职于上海同步辐射光源,从事XAFS方法的实验设计及数据解析。主要研究方向为同步辐射方法在能源、化学、环境领域的应用。累计发表包括 Nature Communications、Applied Catalysis B 、Angew. Chem.、Environ. Sci. Technol 等期刊100余篇,他引2566次。














