肿瘤免疫专家很早就意识到免疫系统在对抗肿瘤时起到了关键性的作用,但是早期的尝试均不尽如人意,原因在于早期研究没能将免疫系统中关键的T细胞的杀伤能力充分激活。
追溯到1980年,人们通过将T细胞从病人身体中提取出来,体外培养,扩增,然后再重新注射回病人体内的方式来对抗肿瘤,这一方法成效甚微,因为大部分T细胞在重新注射回患者体内之后很快就失去活性。

June 和 Levine在90年代中期一直在尝试通过强化自身免疫,或者说使用强化的T细胞治疗HIV的研究,其所使用的理念和技术如今已经得到了认可。
过去几年,嵌合抗原受体的T细胞—或CAR-T—的概念已近家喻户晓,超过1000名白血病或淋巴瘤患者接受过相关的临床试验,其中绝大部分患者的存活时间超过了预期,近百人甚至痊愈。
CAR-T在白血病或淋巴瘤治疗领域的成果已经证明CAR-T理念和技术的正确,目前要做的就是将这一技术继续发展,使得其他类型的肿瘤患者也能收益。
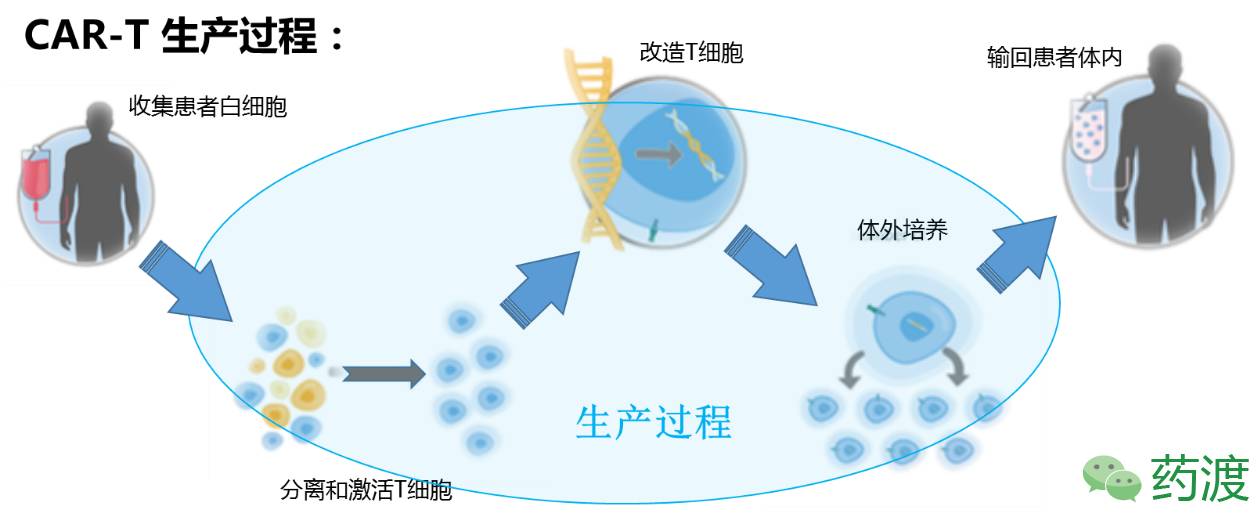
涡轮增压版T细胞
最初的设想其实很简单,就是如何增强T细胞的杀伤能力。通常,T细胞需要接收到树突状细胞给予的信号才能激发自身的杀伤能力,包括分化,产生大量针对同一靶点的相同个体,以及释放一种叫做细胞因子的化学物质,这种化学物质可以刺激机体产生更强烈的免疫反应,但是几天之后,T细胞就失去活性,身体就恢复到正常状态。
June和Levine在90年代中期试图通过体外培养T细胞的方法治疗HIV。当时面临的第一个挑战就是如何激活T细胞,理论上讲,将T细胞暴露在同样从患者体内取出的树突状细胞就可以实现激活。但是,树突状细胞的数量和质量在癌症或HIV患者体内差异很大,几乎无可操作性。最终,他们使用涂抹两种蛋白的微小磁粒来模拟并改善了这种刺激作用,这一方法目前成为被广泛应用于体外培养T细胞的技术。
重塑T细胞
机体在增强自身免疫能力对抗恶性细胞时需要面对两个挑战:第一,恶性细胞可能来源于自身细胞的畸变,而我们的免疫系统一般情况下不会对自身细胞进行攻击,这就使得大部分来源于自身的恶性细胞得以逃逸。第二,恶性细胞会使用各种手段躲避免疫系统的击杀,或者干扰免疫系统正常运行。
为了避免自身健康细胞受T细胞攻击,T细胞需要同时识别目标细胞表面上两个关键的分子才能进攻。第一个是一种蛋白复合物,MHC分子,由树突状细胞呈递给T细胞的抗原。第二个是共同刺激性配体,提供T细胞进攻指令。若想T细胞进攻,二者缺一不可。因此,恶性细胞有两种逃逸T细胞追杀的方法,阻止MHC产生,或呈递使T细胞“关”的共同刺激性配体。
在洞悉激活T细胞的自然途径之后,科学家们不禁自问,若T细胞可以从遗传水平得到改造,使其可以识别恶性细胞表面特有的信号,而无视是否有MHC? 若T细胞可以不再遵从其天生的“两步”进攻过程而直接对肿瘤进攻?而这些问题的答案,在CAR-T技术成功问世之前是没有人敢正面回答的。
解决的答案,从基因水平武装T细胞,通过安装人造分子(CAR),一次性解决识别和激活的问题。事实上,单克隆抗体结合T细胞刺激蛋白似乎是一种不错的选择,通过设计一种类单抗的CAR,将其一部分暴露于T细胞外,用于结合肿瘤细胞的受体,另一部分植于T细胞内,用于在结合肿瘤细胞之后产生足够的刺激。
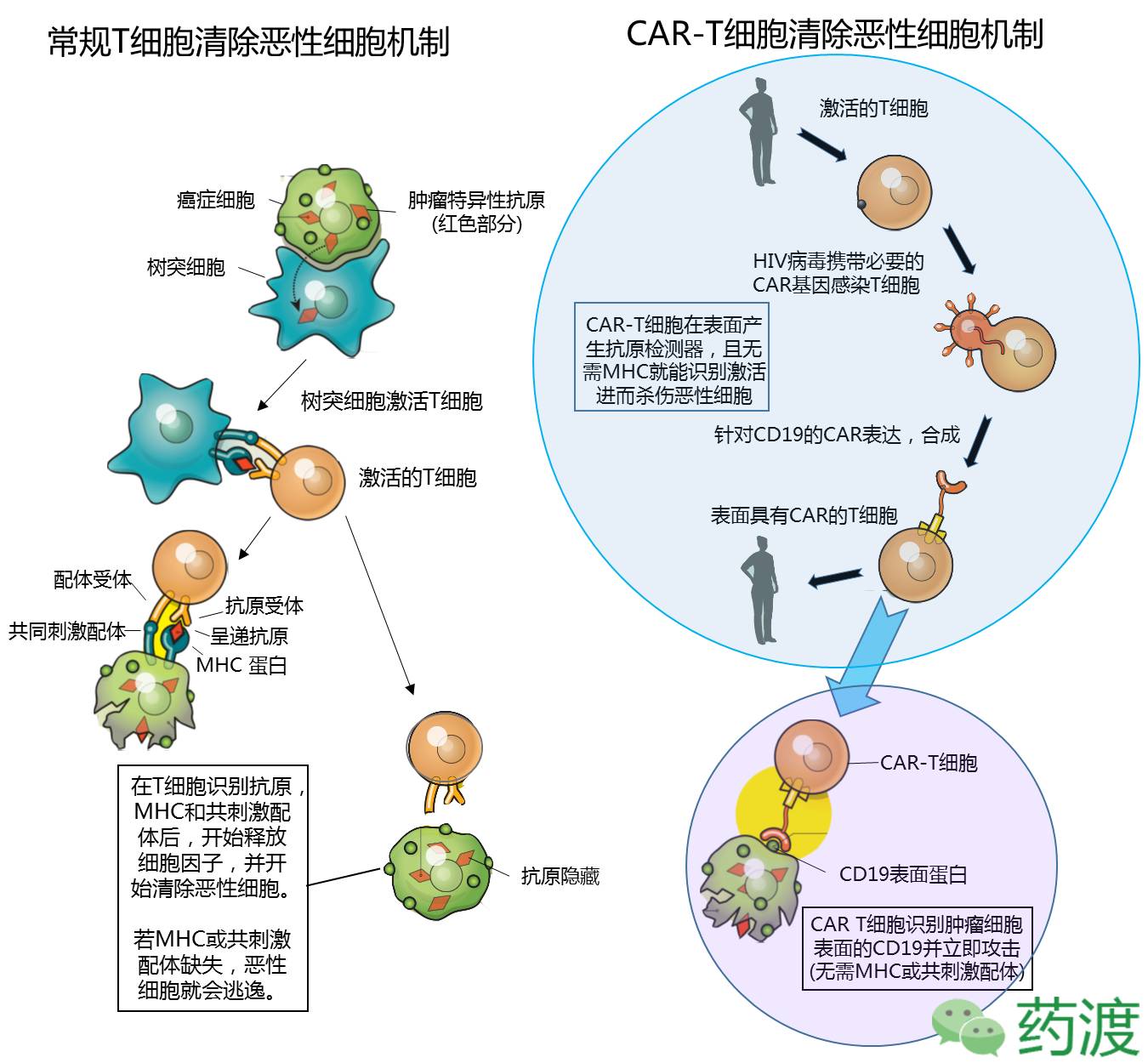
此时,问题的核心变成如何让T细胞产生所需的抗体激活分子(antibody-activator molecule),他们想到了使用HIV病毒(HIV病毒是一种专门入侵免疫系统的病毒,它可以将自身基因整合到T细胞的基因上),将HIV病毒上有害的部分替换为抗体激活嵌合体基因(antibody-activator chimera),然后用这种改造过的HIV病毒感染从患者体内提取的T细胞,就像特洛伊木马一样将必要的遗传信息带入T细胞内,并改造了T细胞,后代T细胞会在表面表达CAR。
实践检验
在90年代中期至2000年,June 和 Levine与他人合作不断完善了HIV对T细胞的改造技术,为之后的CAR-T技术奠定了基础。
之后,科学家们开始考虑应该把T细胞改造成什么样,改造之后的T细胞应该只攻击恶性细胞,而非健康细胞,但是恶性细胞都是由健康细胞演变而来的,他们几乎拥有相同的抗原,这就使得T细胞很难区分二者。
白血病和淋巴肿瘤都是由B细胞恶性增殖造成的,这种肿瘤细胞表面有种特殊的蛋白CD19,该蛋白仅在白血病和淋巴瘤肿瘤细胞表达,健康细胞不表达。这使得CD19成为了完美的靶点。
June 和 Levine首先在小鼠身上测试了理论的可行性,在得到肯定的结果后,于2010年初,他们挑选了3名其他治疗方法无效的晚期CLL患者进行实验。
第一个接受实验的是William Ludwig,有近十年的白血病病史,在2010年8月接受了改造T细胞的注射,但是在注射10天之后,出现了一系列剧烈的不良作用,发烧,低血压,呼吸困难。后来人们意识到这种不良作用是由于改造的T细胞产生过多细胞因子引起的。幸运的是William Ludwig最终还是挺了过来,一个月后,他的身体里已经没有白血病B细胞了,并且在6年间未出现复发的情况,其他两名受试者身上也出现了这样令人欣喜的结果。
经过这样改造的T细胞究竟多有活力?后期研究显示,改造的T细胞可以在患者的血液和骨髓中增殖。据估计,每个CAR-T细胞可以杀死1,000至93,000个肿瘤细胞。在初次注射一个月之后,将后代细胞从患者体内取出,发现这时候的T细胞依然可以在体外继续杀伤恶性细胞。
之后,由于缺乏经费,当局认为这样的实验危险太高,项目不得不暂时搁置。June 和 Levine将已有临床研究发表在国际顶尖杂志上,并得到了重视。
之后通过各方努力,以及一些公司确实看到了这一技术的应用前景,June 和 Levine开始着手开始新的临床试验,在制药企业诺华(Novartis)的帮助下,他们开始对儿童患者进行实验,并最终于今年成功上市全球首款CAR-T治疗方法,另外一家很可能获FDA批准的是Kite。
目前,CAR-T疗法所面临的主要挑战:1) 不良反应很强,主要是细胞因子引起的一系列不良反应。2) 需要找到除了CD19之外的靶点,才能治疗更多种类的肿瘤。虽然进展很缓慢,失败,倒退都在所难免,但是谁又能说未来不是光明的呢?
1. Marcela V. Maus et al. in Annual Review of Immunology, Vol. 32, pages 189–225; 2014.
2. a.S. L. Maude et al. in New England Journal of Medicine, Vol. 371, No. 16, pages1507–1517; October 16, 2014.