作者丨ZX
编辑丨夏獭
大家都还记得自己当初是如何开始对神经科学感兴趣的嘛?我记得我当初还是一名大二的学生,偶然一天在TED上看到了
Sebastian Seung
题为‘I am my connectome‘的演讲,感慨脑的神秘与精巧,从此便一往无前地入了‘神经科学的坑’,并且开始关注连接组,要研究连接组就绕不开全脑成像,今天我就在这里讲一讲全脑成像的那些事。Sebastian Seung将神经网络比喻为颅骨内的悲喜森林,但我觉得神经网络更像是星空,每一个神经元都是夜空中最亮的星。要想弄清楚这样一个星辰闪耀的复杂体系,对整个神经网络进行成像并重构是必不可少的。
脑结构的研究是跨越多个尺度的,从纳米级别的突触囊泡,到微米级别的神经元,再到毫米级别脑区,最后到整个全脑,对应的成像方法也不同。目前有宏观水平的核磁共振成像,介观和微观水平上的光学显微镜成像,以及超微观水平上的电子显微镜成像。
核磁共振
的空间分辨率较低,我们通过核磁共振获得的信息实在太过粗放。
电子显微镜
的分辨率非常高,可以看到很精细的结构。16年Harvard的William Lichtman团队在《cell》发表了他们利用电子显微镜重构出了小鼠外侧膝状体的400多个神经元,达到了4x6x28nm的空间分辨率,一个突触内的囊泡大概是几十个纳米,树突上一个树突棘的长大概是0.5~1.0um,也就是说这种方法可以很清楚的看到树突的结构,但这种方法对应着巨大的工作量以及巨大的数据量,用这种方法进行全脑范围内的成像是很困难的。
光学显微镜
作为一个折中的选择就凸显了它的优势,这几年基于各种光学显微镜的全脑成像方法快速发展了起来。另外,依托于荧光蛋白的
神经元标记方法
非常丰富也非常便利,这就使得光学成像方法具有了更大的优势。下面我将按照不同类型的光学显微镜来介绍一下现有的一些全脑成像技术。
2012年,TissueVision公司联合冷泉港以及HHMI提出了
基于双光子的STP(serial two-photon)全脑成像系统
。整个系统的配置如图1所示。它是利用双光子显微镜对样品进行逐层扫描,并配有一个振动切片机,将样品用琼脂糖包埋,采用边切边拍的策略。
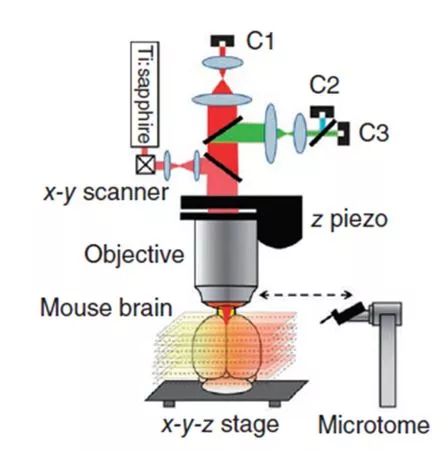
图1 STP(serial two-photon)全脑成像系统
虽然较激光共聚焦显微镜相比,双光子显微镜在成像深度上有了极大改善,但仍旧不足以穿过整个脑组织,所以仍需要适当进行切片。为了避免切片带来的组织表面的遗失和变形,每次切片都会保留一部分已经完成成像的组织。该系统是以50微米的间隔层扫,决定了其轴向(z)的分辨率最大只能达到50微米。扫260层即可完成全脑的扫描。用10倍镜以2微米,1微米的横向(x-y)分辨率扫描全脑所需要的时间分别约为6.5小时和8.5小时。用20倍镜以1微米,0.5微米的横向(x-y)分辨率扫描全脑所需要的时间分别约为15.5小时和24小时。该系统具有较高的成像速度,但最大的问题就是轴向分辨率低。轴向分辨率和成像速度是一对矛盾,要想快速成像就难免要牺牲分辨率。不过这样一个分辨率级别的成像系统已经可以获得很多数据并揭示很多问题了。Allen脑科学研究中心用表达EGFP的AAV标记鼠脑,采用STP的方法,用20倍的水镜以0.35微米的横向分辨率和100微米的轴向间隔连续成像18.5小时获得了全脑的数据,数据量大概为750GB。他们通过这种方法绘制出了区域间的连接图谱。
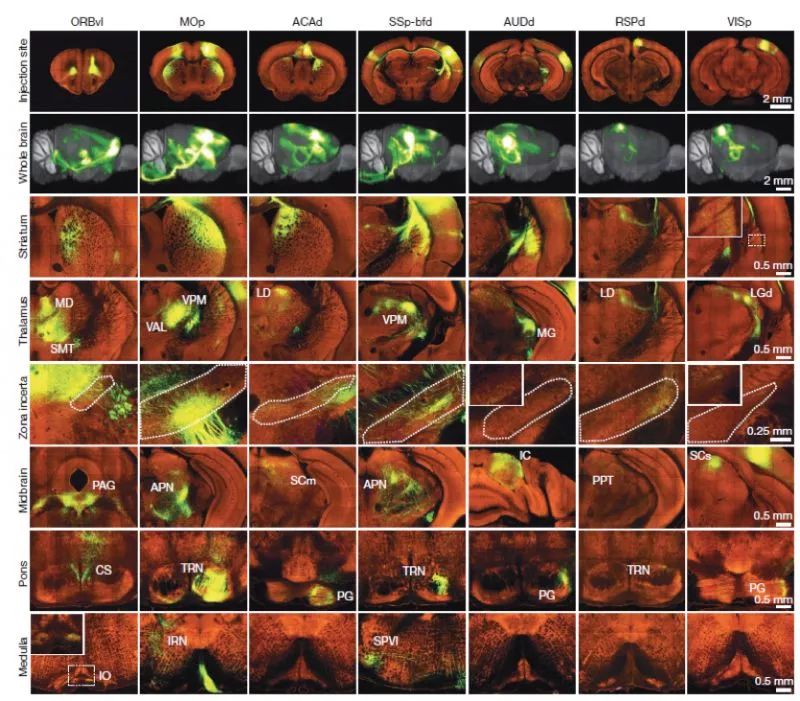
图2 Allen STP 成像结果示意图
华科的骆清铭老师是国内做全脑成像的领军人物。他们团队2010年在Science上发表了
显微光学切片断层成像系统(Micro-Optical Sectioning Tomography)
,简称MOST。后续他们又推出了荧光光学切片断层成像系统(Fluorescent micro-Optical Sectioning Tomography),简称fMOST。MOST系统如图2所示,主要是由一个明场显微镜和一个显微切片机组成。显微镜的镜头是一个40倍的水镜,采集装置为一个线扫描的CCD。显微切片机采用的是金刚石的刀片。他们用高尔基染色的方法标记神经元,再使用Spurr明胶来包埋样品,使样品的质地可以允许切得足够的薄。整个系统采用的也是边切片边成像的策略,但与STP系统不同的是,MOST是对切下来的位于刀片上的薄片进行成像。STP系统实际上是利用光学原理来实现层扫,而MOST系统层扫是依赖于物理切片。MOST系统以0.5微米的横向分辨率,1微米的轴向分辨率(切片的厚度)需要242小时完成对全脑的扫描,获得超过8TB的数据。
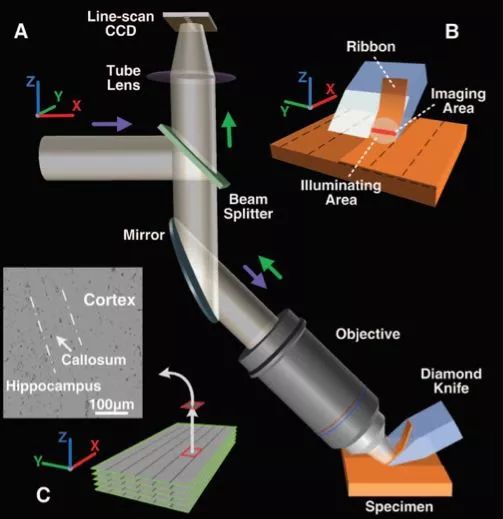
图3 MOST成像系统
fMOST系统与MOST系统相比,区别在于fMOST系统中的显微镜是一台荧光共聚焦显微镜,以实现对荧光标记的样品进行高分辨率成像。比较特别的是,这台荧光共聚焦显微镜利用声光偏振器(AOD)作为扫描器,比起机械扫描器,它更稳定,更适合长时间的成像。由于fMOST的成像对象是荧光样品,所以包埋方式也有所改变,采用的是可以保存荧光信号的树脂包埋。与STP相比,fMOST在分辨率上有绝对优势,但对应着更长的成像时间和更大数据量。
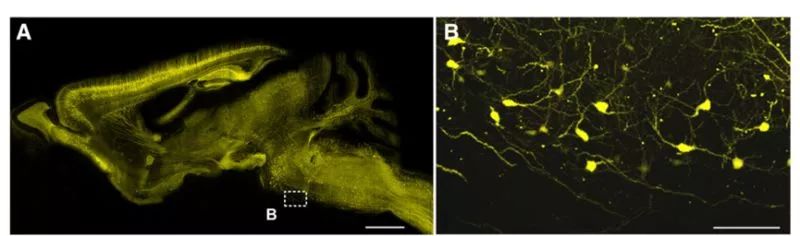
图4 fMOST 成像结果示意图
另外一种用来进行全脑成像的方法是
透明脑结合激光片层扫描显微镜
。对于较厚较大的组织成像的困难是由于散射光无法穿过组织对较深的位置进行成像,前面两种方法都采用了切片的方法来解决这个问题,另外一种解决办法就是将组织变的透明。透明的原理是通过均匀组织的折射率来减少散射。目前存在的透明方法主要可以分为四类。一类是依赖
有机溶剂
的方法,包括3DISCO、iDICSO、uDISCO等。这类方法会脱去组织中的水和脂质,再用有机溶液来均匀折射率。一类是使
溶液简单的浸入
脑子的方法,包括ClearT、SeeDB、FRUIT等。大多数简单浸泡的方法是通过使用高折射率的溶液取代组织内部和周围的液体来匹配组织的平均折射率。另一类基于
水合作用
的透明方法,这类方法是对组织进行脱脂并通过水合作用降低组织的折射率。这类方法有ScaleS、CUBIC。还有一类使用
水凝胶
的方法,如CLARITY等,这种方法是先用组织-水凝胶混合体保证全脑内的细胞骨架蛋白及其他蛋白保持在固定的位置,然后再几乎脱掉组织全部的脂质。将透明的组织利用
激光片层扫描显微镜进行成像,可以快速地获得全脑地图像信息。
激光片层扫描显微镜的原理(图5)简单来讲是使用一束薄片光从侧面照射样品并激发这一层的荧光信号,在样品的上方垂直于光路的方向上有一相机来采集信号,通过移动光片或移动样品使样品的不同层被激发,这样就实现了荧光样品的三维层析成像。为了达到更好更快的成像效果以及适应各种类型的样品,目前有很多不同版本的激光片层扫描显微镜,例如数字扫描激光片层荧光显微镜(DSLM),多视野激光片层扫描显微镜(SiMView)等等。目前,结合不同透明脑技术和不同激光片层扫描显微镜的全脑成像系统也有很多,就不再一一详细介绍,只举两个例子。16年,斯坦福的一家实验室在《cell》利用优化的iDISCO+和激光片层扫描显微镜技术对全脑进行成像,以4.06微米的横向分辨率和3微米的轴向分辨率一个小时可以完成对半个小鼠脑组织的成像。同样是16年,年德国的一家实验室在《Nature Method》上发表的利用uDISCO和激光片层扫描显微镜以0.5-2微米的横向分辨率以及4微米的轴向分辨率完成了对小鼠全身所有神经结构的成像与重构(图6)。
17年,日本大阪大学的一个团队在《neuron》发表了
基于转盘共聚焦显微镜的FAST全脑成像系统
。共聚焦显微镜是通过一个针孔来实现逐点扫描,而转盘共聚焦显微镜有一个转盘,转盘上有螺旋排列的许许多多个针孔,可以进行多点扫描,通过转盘的转动使针孔位置随之改变,从而实现对样品的完整扫描,这样大大提高了成像速度。FAST采用了和STP相似的切片策略。如图7所示为FAST的成像系统,有一个螺旋针孔阵列的转盘,一个水镜,水镜的转动靠一个陶瓷电压阀(piezo actuator)驱动。
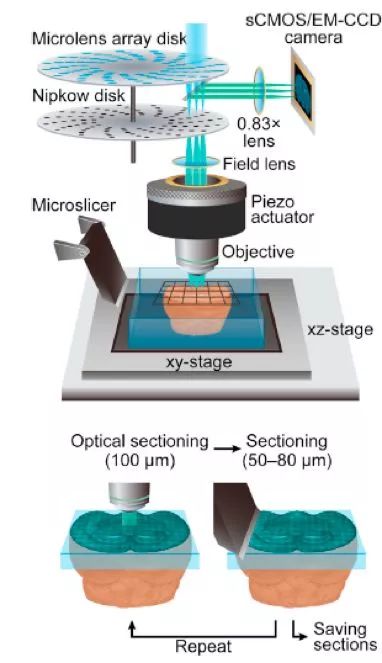
图7 FAST成像系统
信号采集由2048x2048像素的sCMOS相机或1024x1024像素的EM-CCD相机完成。样品的移动通过一个x-y平移台实现。另外,还有一台显微切片机进行切片。每完成100微米厚度的成像,就从上表面切掉50-80微米的样品,不断重复。FAST可以2.4h以0.7微米的横向分辨率和5微米的轴向分辨率完成对一个完整鼠脑的成像,大约产生1T的原始数据。
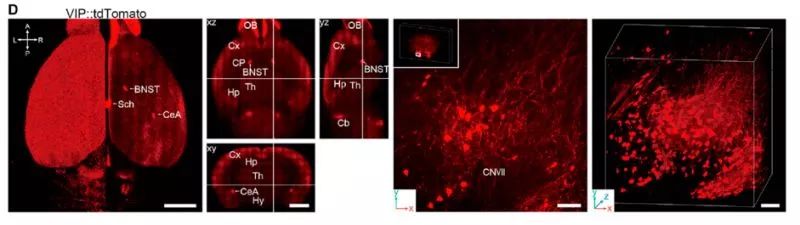
图8 FAST成像结果示例
我们可以看到目前基于光学显微镜的全脑成像技术非常多样,这些方法不能简单地比较好坏,它们都有各自的优点也有各自的缺点。方法的出现和发展都是为了解决实际问题,所以最重要的是我们根据自己的需求找到合适的方法或是在现有的方法上再进行优化。
参考文献
Morgan J L, Berger D R, Wetzel A W, et al. The Fuzzy Logic of Network Connectivity in Mouse Visual Thalamus[J]. Cell, 2016, 165(1):192-206.
Pan C, Cai R, Quacquarelli F P, et al. Shrinkage-mediated imaging of entire organs and organisms using uDISCO[J]. Nature Methods, 2016, 13(10):859-867.
Seiriki K, Kasai A, Hashimoto T, et al. High-Speed and Scalable Whole-Brain Imaging in Rodents and Primates.[J]. Neuron, 2017, 94(6):1085.
Kim S Y, Chung K, Deisseroth K. Light microscopy mapping of connections in the intact brain[J]. Trends in Cognitive Sciences, 2013, 17(12):596.
Oh S W, Harris J A, Ng L, et al. A mesoscale connectome of the mouse brain.[J]. Nature, 2014, 508(7495):207-14.
Li A, Gong H, Zhang B, et al. Micro-optical sectioning tomography to obtain a high-resolution atlas of the mouse brain.[J]. Science, 2010, 330(6009):1404-1408.
Gong H, Zeng S, Cheng Y, et al. Continuously tracing brain-wide long-distance axonal projections in mice at a one-micron voxel resolution[J]. Neuroimage, 2013, 74(7):87.
Ragan T, Kadiri L R, Venkataraju K U, et al. Serial two-photon tomography for automated ex vivo mouse brain imaging[J]. Nature Methods, 2012, 9(3):255-8.
Renier N, Adams E, Kirst C, et al. Mapping of Brain Activity by Automated Volume Analysis of Immediate Early Genes[J]. Cell, 2016, 165(7):1789-1802.
“脑人言”是公益的
脑科学原创科普团队
,由海内外一线科研人员组成,专注于
神经科学、认知科学和脑机接口等
领域的科学知识和思想的传播。关注请长按上方二维码;投稿、合作、转载请联系:
linro1996
;加入作者团队请联系:
chinatang2010
。





