BioArt按
:
寨卡病毒是一种蚊媒黄病毒,
寨卡病毒病患者的症状可能包括轻微发热、皮疹、结膜炎、肌肉和关节疼痛、浑身虚弱或头痛等。
自2013年以来,ZIKV首先在法属波利尼西亚暴发,随即迅速蔓延至南美,引起了全球广泛关注。
2016年2月,WHO宣布寨卡病毒为全球紧急公共卫生事件。
然而,目前仍没有可有效防治ZIKV感染的疫苗或药物,且目前的研究主要集中在抗ZIKV的小分子药物和抗体药物。而多肽类药物以比小分子药物更为安全,比抗体药物成本较低的优势成为目前新兴的药物研究方向之一。
7月25日,复旦大学基础医学院、附属公共卫生临床中心
姜世勃
、
陆路
研究团队与军事医学科学院微生物流行病研究所
秦成峰
团队合作在
Nature Communications
杂志上发表了题为“A peptide-based viral inactivator inhibits Zika virus infection in pregnant mice and fetuses”的研究论文,
在多肽类抗寨卡病毒药物研究中取得新进展,其所设计的多肽类病毒灭活剂可有效地杀灭寨卡病毒,阻止其感染孕鼠及其胎儿,这一发现为防治寨卡病毒感染的药物研究提供了新的思路。

论文解读:
寨卡病毒(Zika virus,ZIKV),是一种蚊媒传播的黄病毒科黄病毒属,有包膜,单股正链的RNA病毒,于1947年首次在乌干达的恒河猴体内分离得到。2007年以前,ZIKV 只零星感染人类,而从 2007年开始,出现 ZIKV爆发感染。 截止到2017年3月份,全球约80多个国家或部落报道了ZIKV的蚊媒传播感染【1】。
寨卡病毒传播图(图片来源于网络)
ZIKV感染人类,通常情况下只引起低热、斑丘疹、关节疼痛、结膜炎等症状,但其感染孕妇,可能导致胎儿脑部先天性发育畸形,产生小头症;ZIKV感染也是古兰-巴雷综合征(Guillain-Barr低热、斑丘疹、关节疼,GBS)诱发原因之一。并且,2016年来自中国农业大学李向东教授和中国科学院微生物研究所高福院士课题组合作在
Cell
上发表文章证明,ZIKV感染雄性小鼠,会导致其睾丸受损,甚至不育【2】。
然而,目前仍没有可有效防治ZIKV感染的疫苗或药物,且目前的研究主要集中在抗ZIKV的小分子药物和抗体药物。而多肽类药物以比小分子药物更为安全,比抗体药物成本较低的优势成为目前新兴的药物研究方向之一。
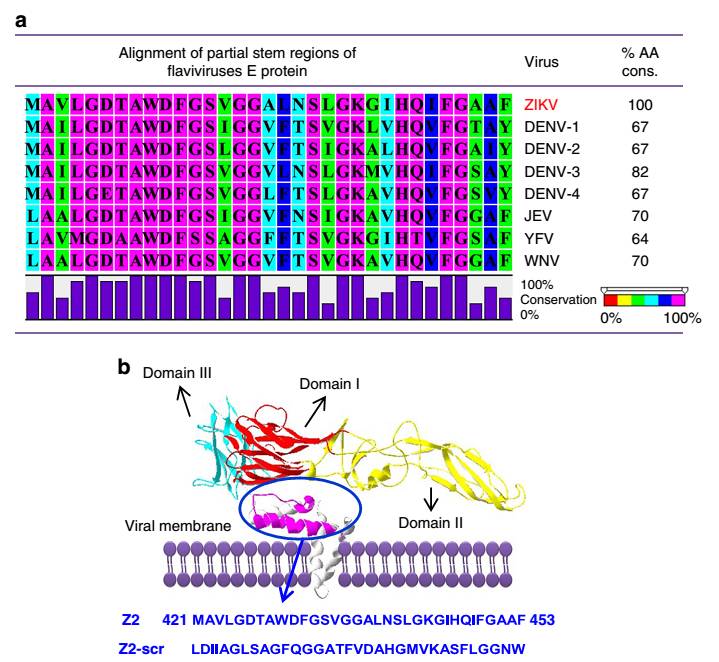
姜世勃陆路团队在对ZIKV E蛋白的序列分析和研究后,成功地研发出了一个能够灭活ZIKV的多肽候选药物(Z2)(
上图
)。他们发现该多肽能与ZIKV的表面蛋白结合,扰乱病毒表面稳态,导致病毒表面穿孔,病毒基因组释放,最终使病毒失去感染活性。体外细胞模型及体内动物模型上的实验结果显示Z2多肽可较好地抑制ZIKV的感染。他们还发现Z2多肽具有穿透胎盘屏障的能力,不仅能够降低ZIKV感染孕鼠血清中的病毒滴度,还能显著降低胎盘和胎儿ZIKV的感染率,阻止ZIKV的垂直传播。此外,
该多肽灭活剂对孕鼠及胎鼠均表现出较好的安全性,有望发展为可防治ZIKV感染的新型药物,尤其适用于ZIKV感染的高危人群——孕妇。
对MERS病毒具有高抑制活性的全人源单克隆抗体(m336)。该抗体是目前针对MERS 病毒最好的候选治疗药物之一,具有极强的病毒中和活性。并且此前,该团队已研发出具有国际领先水平的抗MERS多肽抑制剂(HR2P-M2),能有效地保护动物免受致死剂量的MERS-CoV攻击,明显降低已感染动物肺部的病毒载量。
特别值得一提的是,该研究是姜世勃陆路团队继研制
对MERS(Middle East respiratory syndrome,中东呼吸症)
病毒
具有高抑制活性的全人源单克隆抗体(m336)之后
在新发突发传染病的防治对策研发领域的又一新成果【3】,其在去年世界卫生组织将南美地区发生的寨卡病毒“暴发式传播”(explosive pandemic)判定为“国际关注的突发公共卫生事件”后较短时间内攻关完成,标志着复旦大学基础医学院在该领域的人才团队及创新技术等方面具有明显的优势,未来将继续为我国及全球应对重大新发突发传染病的威胁做出贡献。

复旦大学分子病毒学教育部/卫生部重点实验室姜世勃教授团队。图片来源于复旦大学官网
据悉,复旦大学基础医学院
于玉凤
、军事医学科学院微生物流行病研究所
邓永强
和上海市公共卫生临床中心
邹鹏
是该论文的共同第一作者,复旦大学
陆路
研究员、
姜世勃
教授及军事医学科学院微生物流行病研究所
秦成峰
教授是该论文的共同通讯作者。该课题获得了国家高技术研究发展计划(863计划)、国家重点研发计划生物安全专项、国家自然科学基金等项目的资助。
参考资料:
1、http://www.who.int/emergencies/zika-virus/en
2、Ma, Wenqiang, et al. "Zika virus causes testis damage and leads to male infertility in mice."
Cell
167.6 (2016): 1511-1524.
3、Lu, Lu, et al. "Structure-based discovery of Middle East respiratory syndrome coronavirus fusion inhibitor."
Nature communications
5 (2014): 3067.

姜世勃
,教授,
现任复旦大学基础医学院医学分子病毒学教育部/卫生部重点实验室教授、病原微生物研究所所长
,国家“千人计划”学者。1988-1990年在美国纽约洛克菲勒大学做博士后研究,1990-2010年在纽约血液中心LFK研究所担任助理研究员、副研究员、研究员和研究室主任。曾是武汉大学、复旦大学、第一军医大学、第四军医大学、中国军事医学科学院的客座教授, 中国科学院的海外评审专家、南方医科大学抗病毒中心荣誉主任和特聘教授。
The Lancet
编辑顾问,
Retrovirology、PloS ONE、Microbes and Infection、Emerging Microbes and Infection、The Open AIDS Journal
杂志编辑委员会成员,曾为六十多家英文杂志审稿。主要从事抗病毒药物及疫苗研究,在国际上开辟了研发抗病毒多肽药物及病毒融合/进入抑制剂的全新领域。已发表230多篇SCI论文,总影响因子1,150点 (篇均5.0),其中包括
Nature、 Nature Medicine、Nature Review Microbiology、Lancet、Cell、JEM、PNAS
等,被引用5,500多次,h指数为40。已申请美国专利23项和中国专利8项(其中两项已成功转让和开发),作为PI获得美国NIH研究基金项目八项近两千万美元、中国自然科学基金海外青年学者合作研究基金(杰青B类)及其它的国家级和部级研究基金项目八项。

陆路
,博士,现任复旦大学基础医学院病原生物系及医学分子病毒学教育部/卫生部重点室研究员、博士生导师。清华大学生物学博士,美国纽约血液中心LFK研究所博士后。2011年作为复旦大学引进人才任副研究员,青年PI,2015年任研究员,博士生导师。长期从事“病毒入侵机制、抗病毒药物及疫苗和新型防治策略”的研究。在国际学术期刊(如
Nature Communications. Clin. Infect. Dis., Retrovirology,J. Virol. , J Antimicrob Chemother., J. Biol. Chem., Vaccine
等刊物)上发表SCI论文59篇,总影响因子超过210,其中IF>10 分的1篇,IF>5分的共21篇(投稿当年)。申请美国专利1项,国家专利9项,其中国际PCT专利2项,目前已获得授权专利3项(美国专利1项),其中3项中国专利均已转让,2项已实施形成产品。作为项目负责人开展的课题包括国家863青年科学家项目、自然科学基金面上项目、自然科学基金青年基金、国家十二五传染病重大专项(子课题负责人)、上海市“浦江人才”计划、“晨光计划”等。现已入选教育部科研基金与科研奖励评审专家,中国微生物学会病毒学专业委员会青年委员,上海市 “浦江人才”及青年骨干“晨光”培养计划。

秦成峰
,军事医学科学院微生物流行病研究所病原微生物生物安全国家重点实验室研究员,病毒室主任,国家“优青”。
2001年本科毕业于武汉大学生命科学学院,在军事医学科学院获博士学位,曾获ADVAC Fellowship赴法国交流。主要从事虫媒黄病毒致病机制研究,先后作为通讯获共同通讯作者在
Immunity、Cell Stem Cell、Cell Host Microbe、eLife、PNAS、Nature Communications
等杂志发表论文多篇。2016年获英国皇家学会“牛顿高级学者”,2015年获国家优青基金资助,2014年获(原)总后勤部科技新星。曾获爱德华詹纳疫苗学会青年科学家(2016)、中国微生物学会“梅里埃优秀青年科学家奖”、“埃博拉出血热疫情防控先进个人”等。兼任
Scientific Reports、npj Vaccines、BMC Infectious Diseases
等杂志编委。


BioArt,一心
关注生命科学,只为
分享更多有种、有趣、有料的信息。
关注请长按上方二维码。投稿、合作、转载授权事宜请联系微信ID:
fullbellies
或邮箱:
[email protected]
。





